a)Hãy tính số mol của:5,4g Al;16g So3; 0,8g H2 ; 3.1023phân tửH2
b) Hãy tính khối lượng của : 4,48 l (SO2)( đktc); 0,8 molCO2
c) Hãy tính thể tích : 6,6g CO2(đktc) ; 0,15 mol khí ni tơ
1, Hãy tính
a/ Số mol của: 5,4g Al, 8g CuO, 16g Fe2O3
b/ Thể tích khí ở đktc của: 0,25 mol CO2, 0,175mol H2 1,5mol N2
2: Tính khối lượng mỗi nguyên tố có trong :
a. 0,5 mol Al2O3
b. 2,2 g CO2
1.
\(a,n_{Al}=\dfrac{5,4}{27}=0,2(mol)\\ n_{CuO}=\dfrac{8}{80}=0,1(mol)\\ n_{Fe_2O_3}=\dfrac{16}{160}=0,1(mol)\\ b,V_{CO_2}=0,25.22,4=5,6(l)\\ V_{H_2}=0,175.22,4=3,92(l)\\ V_{N_2}=1,5.22,4=33,6(l)\)
2.
\(a,n_{Al}=0,5.2=1(mol);n_{O}=0,5.3=1,5(mol)\\ \Rightarrow m_{Al}=1.27=27(g);m_{O}=1,5.16=24(g)\\ b,n_{CO_2}=\dfrac{2,2}{44}=0,05(mol)\\ \Rightarrow m_C=0,05.12=0,6(g);m_O=0,05.2.16=1,6(g)\)
Hãy tính:
a) Số mol của : 28g Fe 64g Cu 5,4g Al.
b) Thể tích khí (đktc) của 0,175 mol CO2; 1,25 mol H2; 3 mol N2.
c) Số mol và thể tích của hỗn hợp khí (dktc) gồm có 0,44g CO2 0,04g H2 và 0,56g N2.
a)
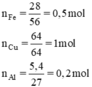
b) VCO2 = 22,4 .0,175 = 3,92l.
VH2 = 22,4 .1,25 = 28l.
VN2 = 22,4.3 = 67,2l.
c) Số mol của hỗn hợp khí bằng tổng số mol của từng khí.
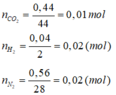
nhh = nCO2 + nH2 + nN2 = 0,01 + 0,02 + 0,02 = 0,05 mol
Vhh khí = (0,01 + 0,02 + 0,02) . 22,4 = 1,12l.
a)Tính số mol của S có trong 16g lưu huỳnh
b)Tính số mol Al có trong 5,4g nhôm
c)Tính số mol Fe2O4 CÓ TRONG 6,96g ooxxit sắt từ
d)Tính soos mol CO2 có trong 4,4g cacbonnic
n=\(\dfrac{m}{M}\)
nS = \(\dfrac{16}{32}\)= 0,5 mol
nAl = \(\dfrac{5,4}{27}\)= 0,2 mol
nFe3O4 = \(\dfrac{6,96}{232}\)= 0,03 mol
nCO2 = \(\dfrac{4,4}{44}\)= 0,1 mol
Hãy tính
a) Số mol của : 28g Fe ; 64g Cu ; 5,4g Al
b) Thể tích khí (đktc) của : 0,75 mol Co2 ; 1,25 mol H2 ; 3mol N2
júp mình với nha![]()
a)
n(Fe)=28/56=0.5 mol
n(Cu)=64/64=1 mol
n(Al)=5.4/27=0.2 mol
b)
V(CO2)=0.175*22.4=3.92 lít
V(H2)=1.25*22.4=28 lít
V(N2)=3*22.4=67.2 lít
c)
n(CO2)=0.44/44=0.01 mol
n(H2)=0.04/2=0.02 mol
n(N2)=0.56/28=0.02 mol
V(hh)= (0.01+0.02+0.02)*22.4=1.12 lít
n Fe = 28/56= 0,5 mol
n cu = 6,4 / 64= 0,1 mol
n Al = 5,4 / 27 =0,2 mol
V CO2 = 0,75 . 22,4 =16,8 l
V H2 = 1,25 . 22,4 = 28 l
V N2 = 3 . 22,4 =67,2 l
Hãy tính số mol của 28g sắt 5,4g nhôm
nFe = 28/56 = 0,5 (mol)
nAl = 5,4/27 = 0,2 (mol)
nFe = mFe : MFe = 28 : 56 = 0,5 (mol)
nAl = mAl : MAl = 5,4 : 27 = 0,2 (mol)
nFe = \(\frac{28}{56}=0,5\left(mol\right)\)
nAl = \(\frac{5,4}{27}=0,2\left(mol\right)\)
Hãy tính số mol của 28g sắt 5,4g nhôm
nFe = 28/56 = 0,5 (mol)
nAl = 5,4/27 = 0,2 (mol)
nFe = mFe : MFe = 28 : 56 = 0,5 (mol)
nAl = mAl : MAl = 5,4 : 27 = 0,2 (mol)
Hãy tính số mol của 28g sắt 5,4g nhôm
nFe = mFe : MFe = 28 : 56 = 0,5 (mol)
nAl = mAl : MAl = 5,4 : 27 = 0,2 (mol)
Cho 5,4g nhôm (Al) tác dụng với axit clohidric thu được nhôm clorua và khí hidro .Hãy: a) tính số gam nhôm clorua thu được b) tính thể tích khí hidro (dktc) thoát ra
\(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,2 0,3 ( mol )
\(m_{AlCl_3}=n_{AlCl_3}.M_{AlCl_3}=0,2.133,5=26,7g\)
\(V_{H_2}=n_{H_2}.22,4=0,3.22,4=6,72l\)
2Al+6HCl->2AlCl3+3H2
0,2----0,6-----0,2------0,3
n Al=\(\dfrac{5,4}{27}\)=0,2 mol
=>m Alcl3=0,2.133,5=26,7g
=>VH2=0,3.22,4=6,72l
Cho 5,4g Al phản ứng hoàn toàn với 200ml dung dịch HCl
a, Viết phương trình phản ứng
b, Tính thể tích khí H\(_2\) sinh ra (đktc)
c, Tính nồng độ mol của dung dịch HCl đã dùng
a) \(Pt:2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b) \(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(Theopt:n_{H_2}=\dfrac{3}{2}n_{Al}=0,3mol\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72lít\)
c) \(Theopt:n_{HCl}=3n_{Al}=0,6mol\)
\(\Rightarrow C_Mdd_{HCl}=\dfrac{0,6}{0,2}=3M\)
cho 5,4g nhôm Al tác dụng vừa đủ với 200ml dd HCl
a)Tính nồng độ mol của axit HCl
b)Xác định thể tích khí tạo thành ở điều kiện chuẩn
c)Tính nồng độ mol chất tan có trong dd sau, phản ứng biết thể tích dd thay đổi không đáng kể
a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2-->0,6----->0,2---->0,3
=> \(C_{M\left(HCl\right)}=\dfrac{0,6}{0,2}=3M\)
b) VH2 = 0,3.24,79 = 7,437 (l)
c) \(C_{M\left(AlCl_3\right)}=\dfrac{0,2}{0,2}=1M\)