Dung dịch X được tạo ra từ 2 muối gồm các ion: Al3+, Fe2+, SO42-, Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư, thu đucợ 6,46 gam kết tủa. Phần 2 đem tác dụng với dung dịch NaOH dư, thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 1,6 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn và trong dung dịch X có 0,3 mol Cl-. Tính khối lượng muối trong dung dịch X.

Những câu hỏi liên quan
Dung dịch X được tạo ra từ 2 muối gồm có các ion: Al3+, Fe2+, SO42-, Cl- . Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng vói dung dịch Ba(OH)2 dư, thu được 6,46 gam kết tủa. Phần 2 đem tác dụng với dung dịch NH3 dư, thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong dung dịch X gần nhất có thể là A. 17,5 g. B. 5,96 g. C. 3,475 g. D. 8,75 g.
Đọc tiếp
Dung dịch X được tạo ra từ 2 muối gồm có các ion: Al3+, Fe2+, SO42-, Cl- . Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng vói dung dịch Ba(OH)2 dư, thu được 6,46 gam kết tủa. Phần 2 đem tác dụng với dung dịch NH3 dư, thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong dung dịch X gần nhất có thể là
A. 17,5 g.
B. 5,96 g.
C. 3,475 g.
D. 8,75 g.
Gọi x, y, z lần lượt là số mol Al3+ , Fe2+, SO42- trong dung dịch X. Ta có: nCl- = 3x + 2y - 2z (bảo toàn điện tích)
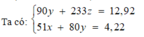
m = 162,5x + 127y + 25z
⇒ 7,58 <m< 14,83
Đáp án D
Đúng 0
Bình luận (0)
Dung dịch X được tạo ra từ 2 muối gồm có các ion Al3+, Fe2+,
S
O
4
2
-
, Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư thu được 6,46 gam kết tủa. Phần 2 đem tác dung với dung dich NH3 dư thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong X có...
Đọc tiếp
Dung dịch X được tạo ra từ 2 muối gồm có các ion Al3+, Fe2+, S O 4 2 - , Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư thu được 6,46 gam kết tủa. Phần 2 đem tác dung với dung dich NH3 dư thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong X có thể là
A. 3,475 gam
B. 5,96 gam
C. 8,75 gam
D. 17,5 gam
Dung dịch X được tạo ra từ 2 muối gồm có các ion Al3+, Fe2+, Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư thu được 6,46 gam kết tủa. Phần 2 đem tác dung với dung dich NH3 dư thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong X có thể là: A. 3,475 gam B. 5,96 gam C. 8,75 gam D. 17,5 gam
Đọc tiếp
Dung dịch X được tạo ra từ 2 muối gồm có các ion Al3+, Fe2+, Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư thu được 6,46 gam kết tủa. Phần 2 đem tác dung với dung dich NH3 dư thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong X có thể là:
A. 3,475 gam
B. 5,96 gam
C. 8,75 gam
D. 17,5 gam
Chia 1 lit dung dịch X có chứa các ion: H+,Al3+,SO42−và Cl− 0,1M, thành hai phần bằng nhau. Nhỏ từ từ đến dư dung dịch NaOH vào phần 1, kết quả thí nghiệm được biểu diễn trên đồ thị sau: Mặt khác cho 300 ml dung dịch Ba(OH)2 0,6M tác dụng với phần 2, thu được kết tủa Y và dung dịch Z. Khối lượng kết tủa Y là (biết các phản ứng xảy ra hoàn toàn) A. 56,76 gam B. 47,40 gam C. 52,06 gam D. 45,06 gam
Đọc tiếp
Chia 1 lit dung dịch X có chứa các ion: H+,Al3+,SO42−và Cl− 0,1M, thành hai phần bằng nhau. Nhỏ từ từ đến dư dung dịch NaOH vào phần 1, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
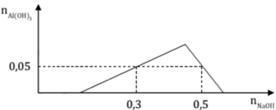
Mặt khác cho 300 ml dung dịch Ba(OH)2 0,6M tác dụng với phần 2, thu được kết tủa Y và dung dịch Z. Khối lượng kết tủa Y là (biết các phản ứng xảy ra hoàn toàn)
A. 56,76 gam
B. 47,40 gam
C. 52,06 gam
D. 45,06 gam
Đáp án B
Gọi số mol H + , A l 3 + , S O 4 2 - trong mỗi phần là x, y, z
Tại A, khi nhỏ một lượng 0,3 mol NaOH, ta có:
0,3 = x + 0,05.3 → x = 0,15 mol
Áp vào điểm B, khi nhỏ một lượng 0,5 mol NaOH, ta có quá trình hòa tan khi kết tủa đạt cực đại xuống còn 0,05 mol kết tủa là: n ↓ = 4 n A l 2 + - n O H - mol (do trung hoà axit, n O H - dung cho kết tủa chỉ là: 0,5 – 0,15 = 0,35 mol)
→ 4.y = 0,35 + 0,05 → y = 0,1 mol
Bảo toàn điện tích suy ra dung dịch X gồm: H + 0 , 15 m o l A l 2 + 0 , 1 m o l S O 4 2 - 0 , 2 m o l C l - 0 , 05 m o l
Khi nhỏ Ba(OH)2 vào dung dịch X thì mất 0,075mol Ba(OH)2trung hòa lượng H+, còn lại 0,105 mol Ba(OH)2tác dụng với Al3+
Vậy nAl(OH)3 = 0,21 :3 = 0,07 mol
m↓ = 0,07.78 + 0,18,233 = 47,4 gam
Đúng 0
Bình luận (0)
Chia 1 lit dung dịch X có chứa các ion: H+,Al3+,SO42−và Cl− 0,1M, thành hai phần bằng nhau. Nhỏ từ từ đến dư dung dịch NaOH vào phần 1, kết quả thí nghiệm được biểu diễn trên đồ thị sau: Mặt khác cho 300 ml dung dịch Ba(OH)2 0,6M tác dụng với phần 2, thu được kết tủa Y và dung dịch Z. Khối lượng kết tủa Y là (biết các phản ứng xảy ra hoàn toàn) A. 56,76 gam B. 47,40 gam C. 52,06 gam D. 45,06 gam
Đọc tiếp
Chia 1 lit dung dịch X có chứa các ion: H+,Al3+,SO42−và Cl− 0,1M, thành hai phần bằng nhau. Nhỏ từ từ đến dư dung dịch NaOH vào phần 1, kết quả thí nghiệm được biểu diễn trên đồ thị sau: Mặt khác cho 300 ml dung dịch Ba(OH)2 0,6M tác dụng với phần 2, thu được kết tủa Y và dung dịch Z. Khối lượng kết tủa Y là (biết các phản ứng xảy ra hoàn toàn)
A. 56,76 gam
B. 47,40 gam
C. 52,06 gam
D. 45,06 gam
Gọi số mol H + , Al 3 + , SO 4 2 - trong mỗi phần là x, y, z
Tại A, khi nhỏ một lượng 0,3 mol NaOH, ta có:
0,3 = x + 0,05.3 → x = 0,15 mol
Áp vào điểm B, khi nhỏ một lượng 0,5 mol NaOH, ta có quá trình hòa tan khi kết tủa đạt cực đại xuống còn 0,05 mol kết tủa là:
n ↓ = 4 n Al 3 + - n OH - = 0 , 05 mol (do trung hoà axit, n OH - dung cho kết tủa chỉ là: 0,5 – 0,15 = 0,35 mol)
→ 4.y = 0,35
+ 0,05 → y = 0,1 mol
Bảo toàn điện tích suy ra dung dịch X gồm:
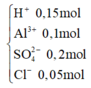
Khi nhỏ Ba(OH)2 vào dung dịch X thì mất 0,075mol Ba(OH)2trung hòa lượng H+, còn lại 0,105 mol Ba(OH)2tác dụng với Al3+
Vậy nAl(OH)3 = 0,21 :3 = 0,07 mol
m↓ = 0,07.78 + 0,18,233 = 47,4 gam
Đáp án B
Đúng 0
Bình luận (0)
các bạn giúp mình bài này nhé: dung dịch X tạo ra từ 2 muối với các ion:Al3+,Fe2+,SO42-,Cl-. chia dung dịch X thành 2 phần bằng nhau. phần 1 đem tác dụng với dd Ba(OH)2 dư thu được 6,46g kêt tủa. phần 2 đem tác dụng với dd NH3 dư, thu đươc kết tủa nung trong không khí đến khối lượng không đổi thu được hỗn hợp 2,11g chất rắn. các phản ứng xảy ra hoàn toàn. khối lượng muối trong dd X có thể là:A.5,96g B. 3,475g C.17,5g D. 8,75g
Đọc tiếp
các bạn giúp mình bài này nhé: dung dịch X tạo ra từ 2 muối với các ion:Al3+,Fe2+,SO42-,Cl-. chia dung dịch X thành 2 phần bằng nhau. phần 1 đem tác dụng với dd Ba(OH)2 dư thu được 6,46g kêt tủa. phần 2 đem tác dụng với dd NH3 dư, thu đươc kết tủa nung trong không khí đến khối lượng không đổi thu được hỗn hợp 2,11g chất rắn. các phản ứng xảy ra hoàn toàn. khối lượng muối trong dd X có thể là:
A.5,96g B. 3,475g C.17,5g D. 8,75g
Gọi a,b,c,d là số mol mỗi ion ở từng phần.
ta lập đc hệ:
51a+80b=2,11
90b+233c=6,46
3a+2b=2c+d
từ đó ta suy ra đc:
m/2=133,5a+127b+25c
Thế các gia trị của m trong đáp án ta chọn được D
Đúng 0
Bình luận (0)
vì K+ và Na+ nên viết p.tử không chuẩn
a) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước vì nộng độ H+trong dd mới tạo thành nhỏ nên sẽ tác dụng từng nấc(vì chỉ từng giọt).lượng H+ chưa dư khi tác dụng với CO32- nên không thể tác dụng tiếp với HCO3- dẫn đến không có hiện tượng
H++CO32- -->HCO3-
b) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước. H+ tác dụng với CO32- còn dư tác dụng với 1 phần HCO3- tạo CO2 khí ko màu dd còn HCO3- tác dụng với OH- tạo CO32- td Ba2+ tạo kt trắng BaCO3
CO32-+H+-->HCO3-
HCO3-+H+-->H2O+CO2
HCO3-+OH-+Ba2+-->BaCO3+H2O(dư nên khi vậy ko dư ghi tỉ lệ Ba2+:OH-=1:2)
c)cho từ từ CO32- và HCO3- vào H+ thì pứ xảy ra đồng thời tạo đều tạo khí CO2 vì khi cho vào thì mt có nồng độ H+ lớn nên pứ xảy ra theo 2 nấc đồng thời
CO32-+2H+-->H2O+CO2
HCO3-+H+-->H2O+CO2
Đúng 0
Bình luận (1)
vì K+ và Na+ nên viết p.tử không chuẩn
a) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước vì nộng độ H+trong dd mới tạo thành nhỏ nên sẽ tác dụng từng nấc(vì chỉ từng giọt).lượng H+ chưa dư khi tác dụng với CO32- nên không thể tác dụng tiếp với HCO3- dẫn đến không có hiện tượng
H++CO32- -->HCO3-
b) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước. H+ tác dụng với CO32- còn dư tác dụng với 1 phần HCO3- tạo CO2 khí ko màu dd còn HCO3- tác dụng với OH- tạo CO32- td Ba2+ tạo kt trắng BaCO3
CO32-+H+-->HCO3-
HCO3-+H+-->H2O+CO2
HCO3-+OH-+Ba2+-->BaCO3+H2O(dư nên khi vậy ko dư ghi tỉ lệ Ba2+:OH-=1:2)
c)cho từ từ CO32- và HCO3- vào H+ thì pứ xảy ra đồng thời tạo đều tạo khí CO2 vì khi cho vào thì mt có nồng độ H+ lớn nên pứ xảy ra theo 2 nấc đồng thời
CO32-+2H+-->H2O+CO2
HCO3-+H+-->H2O+CO2
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Có 100 ml dung dịch X gồm NH4+, K+, CO32- ; SO42-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 2,24 lít (đktc) khí NH3 và 66,3 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Tính giá trị của m
Đọc tiếp
Có 100 ml dung dịch X gồm NH4+, K+, CO32- ; SO42-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 2,24 lít (đktc) khí NH3 và 66,3 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Tính giá trị của m
- Phần 1:
\(n_{NH_4^+}=n_{NH_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(197n_{CO_3^{2-}}+233n_{SO_4^{2-}}=66,3\left(1\right)\)
- Phần 2:
\(n_{CO_3^{2-}}=n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Thay vào (1) ⇒ nSO42- = 0,2 (mol)
BT điện tích trong 50ml dd, có: nNH4+ + nK+ = 2nCO32- + 2nSO42-
⇒ mK+ = 2.0,1 + 2.0,2 - 0,1 = 0,5 (mol)
⇒ m = 2.(0,1.18 + 0,1.60 + 0,2.96 + 0,5.39) = 93 (g)
Đúng 3
Bình luận (0)
Dung dịch X chứa các ion: Fe3+, SO42−, NH4+, Cl-. Chia dung dịch X thành 2 phần bằng nhau: - Phần 1 tác dụng với lượng dư dung dịch NaOH, đun nóng thu được 0,672 lít khí (ở đktc) và 1,07 gam kết tủa - Phần 2 tác dụng với lượng dư dung dịch BaCl2, thu được 4,66 gam kết tủa. Tổng khối lượng muối khan thu được khi cô cạn ½ dung dịch X là (quá trình cô cạn chỉ có nước bay hơi) A. 3,73 gam B. 7,04 gam C. 7,46 gam D. 3,52 gam
Đọc tiếp
Dung dịch X chứa các ion: Fe3+, SO42−, NH4+, Cl-. Chia dung dịch X thành 2 phần bằng nhau:
- Phần 1 tác dụng với lượng dư dung dịch NaOH, đun nóng thu được 0,672 lít khí (ở đktc) và 1,07 gam kết tủa
- Phần 2 tác dụng với lượng dư dung dịch BaCl2, thu được 4,66 gam kết tủa. Tổng khối lượng muối khan thu được khi cô cạn ½ dung dịch X là (quá trình cô cạn chỉ có nước bay hơi)
A. 3,73 gam
B. 7,04 gam
C. 7,46 gam
D. 3,52 gam
Đáp án A
Phần 1:
NH4++ OH- →NH3+ H2O
0,03← 0,03
Fe3++ 3OH-→ Fe(OH)3
0,01 0,01
Phần 2:
Ba2++ SO42- →BaSO4
0,02 0,02
Theo ĐLBT ĐT thì nCl-= 0,02 mol
Tổng khối lượng các muối khan thu được là: (0,03.18+ 0,01.56+ 0,02.96+ 0,02.35,5) = 3,73 gam
Đúng 0
Bình luận (0)
Có 100ml dung dịch X gồm: NH4+, K+, CO32-, SO42-. Chia dung dịch X làm 2 phần bằng nhau: -Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư thu được 6,72 lít khí NH3 (đktc) và 43 gam kết tủa. -Phần 2 cho tác dụng với lượng dư dung dịch HCl thì thu được 2,24 lít khí CO2 (đktc). Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là: A. 24,9 B. 44,4 C. 49,8 D. 34,2
Đọc tiếp
Có 100ml dung dịch X gồm: NH4+, K+, CO32-, SO42-. Chia dung dịch X làm 2 phần bằng nhau:
-Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư thu được 6,72 lít khí NH3 (đktc) và 43 gam kết tủa.
-Phần 2 cho tác dụng với lượng dư dung dịch HCl thì thu được 2,24 lít khí CO2 (đktc).
Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 24,9
B. 44,4
C. 49,8
D. 34,2
Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam
Đúng 0
Bình luận (0)















