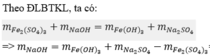: Cho 20 gam sắt(III) sunfat [Fe2(SO4)3] tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit Fe2(SO4)3 và 21,3 gam natri sunfat Na2SO4. Tính khối lượng natri hiđroxit tham gia phản ứng.

Những câu hỏi liên quan
Cho 20 gam sắt(III) sunfat Fe2(SO4)3 tác dụng với natri hiđroxit NaOH, thu được 10,7 gam sắt(III) hiđroxit Fe(OH)3 và 21,3 gam natri sunfat Na2SO4. Số mol natri hiđroxit tham gia vào phản ứng là :A. 0,5 mol. B. 9,4 mol. C. 12 mol. D. 0.3 mol.
Đọc tiếp
Cho 20 gam sắt(III) sunfat Fe2(SO4)3 tác dụng với natri hiđroxit NaOH, thu được 10,7 gam sắt(III) hiđroxit Fe(OH)3 và 21,3 gam natri sunfat Na2SO4. Số mol natri hiđroxit tham gia vào phản ứng là :
A. 0,5 mol.
B. 9,4 mol.
C. 12 mol.
D. 0.3 mol.
Theo ĐLBTKL:
\(m_{Fe_2\left(SO_4\right)_3}+m_{NaOH}=m_{Fe\left(OH\right)_3}+m_{Na_2SO_4}\)
=> \(m_{NaOH}=10,7+21,3-20=12\left(g\right)=>n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\)
=> D
Đúng 2
Bình luận (0)
Cho 20 gam sắt(III) sunfat
F
e
2
S
O
4
3
tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit
F
e
2
S
O
4
3
v...
Đọc tiếp
Cho 20 gam sắt(III) sunfat F e 2 S O 4 3 tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit F e 2 S O 4 3 và 21,3 gam natri sunfat N a 2 S O 4 Tính khối lượng natri hiđroxit tham gia phản ứng.
Cho 20 gam sắt III sunfat
F
e
2
S
O
4
3
tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit
F
e
(
O
H
)
3
và 21,3 gam natri sunfat
N
a
2
S
O
4
. Xác định...
Đọc tiếp
Cho 20 gam sắt III sunfat F e 2 S O 4 3 tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit F e ( O H ) 3 và 21,3 gam natri sunfat N a 2 S O 4 . Xác định khối lượng natri hidroxit tham gia vào phản ứng.
Sơ đồ
Sắt (III) sunfat + Natri hidroxit → Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có
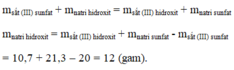
Đúng 0
Bình luận (0)
Cho 20 gam sắt Lil sunfat Fe2(So4)3 tác dụng với Natri Hidroxit NaOHthu được 10,7 gam sắt Lil Hidroxit Fe(OH) 3 và 21,3 gam Natri Sunfat Na2So4 xác định khối lượng Natri Hidroxit tham gia phản ứng
Theo định luật bảo toàn khối lượng:
\(m_{Fe_2\left(SO_4\right)_3}+m_{NaOH}=m_{Fe\left(OH\right)_3}+m_{Na_2SO_4}\)
\(\Leftrightarrow20+m_{NaOH}=10,7+21,3\)
\(\Leftrightarrow m_{NaOH}=10,7+21,3-20=12\left(g\right)\)
Đúng 0
Bình luận (2)
Cho phản ứng hóa học: Sắt (III)sunfat + natri hiđroxit → … + natri sunfat. Phương trình hóa học biểu diễn phản ứng hóa học trên là
A Fe2(SO4)3 + 6NaOH → 2Fe(OH)3 + 3Na2SO4
B Fe(SO4)2 + NaOH → FeOH + Na(SO4)2
C Fe2(SO4)3 + NaOH → Fe2(OH) + Na(SO4)3
D FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
\(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow Fe\left(OH\right)_3+3Na_2SO_4\\ \Rightarrow A\)
Đúng 2
Bình luận (0)
biểu diễn phản ứng hóa học trên là
A Fe2(SO4)3 + 6NaOH → 2Fe(OH)3 + 3Na2SO4
B Fe(SO4)2 + NaOH → FeOH + Na(SO4)2
C Fe2(SO4)3 + NaOH → Fe2(OH) + Na(SO4)3
D FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
Đúng 1
Bình luận (2)
đốt cháy hoàn toàn m gam chất X dùng 4,48 lít O2(đktc) thu được 2,24 lít CO2(đktc) và 3,6 gam H2O xác định X
2/cho 20gam sắt(III)sunfat Fe2(SO4)3 tác dụng với NaOH thu được 10,7 gam Fe(oh)3 và 21,3 gam Na2SO4 xác định Naoh tham gia vào phản ứng
1, Ta có: nO2= \(\dfrac{4,48}{22,4}=0,2\) mol
nCO2= \(\dfrac{2,24}{22,4}=0,1\) mol
Theo ĐLBTKL:
mX+mO2=mCO2+mH2O
=> mX= 0,1.44+3,6-0,2.32
=> mX= 1,6
Đúng 0
Bình luận (0)
2. PTHH: \(Fe_2\left(SO_4\right)_3+6NaOH-->3Na_2SO_4+2Fe\left(OH\right)_3\)
Áp dụng ĐLBTKL:
\(m_{Fe_2\left(SO_4\right)_3}+m_{NaOH}=m_{Na_2SO_4}+m_{Fe\left(OH\right)_3}\)
<=> \(m_{NaOH}=\) 10,7 + 21,3 - 20 = 12 (gam)
Đúng 0
Bình luận (0)
1.\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(m_{O_2}=n_{O_2}.M_{O_2}=0,2.32=6,4\left(g\right)\)
\(n_{CO_2}=\dfrac{V_{CO_2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(m_{CO_2}=n_{CO_2}.M_{CO_2}=0,1.44=4,4\left(g\right)\)
Áp dụng ĐLBTKL:
MX+mO2=mCO2+mH2O
=>MX=(mCO2+mH2O)-mO2=(4,4+3,6)-6,4=1,6(g)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Câu 1: Lập phương trình hóa học các phản ứng sau: a) Bari tác dụng với oxi tạo ra Bari oxit b) Sắt (III) hidroxit tác dụng axit sunfuric tạo ra Sắt (III) sunfat và nước. c) Kẽm clorua tác dụng với Natri hiđroxit tạo ra Kẽm hiđroxit và Natri clorua. d) Natri cacbonat tác dụng axit clohđric tạo ra Natri clorua, khí Cacbon đioxxit và nước.
Bài 1 :
a) Pt : 2Ba + O2 → (to) 2BaO
b) Pt : 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
c) Pt : ZnCl2 + 2NaOH → Zn(OH)2 + 2NaCl
d) Pt : Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Chúc bạn học tốt
Đúng 4
Bình luận (0)
.Cho sắt (III) clorua FeCl3 tác dụng với 5,5 gam kali hidroxit thu được 7 gam sắt (III) hiđroxit Fe(OH)3 và 8,25 kali clorua. Khối lượng FeCl3 đã tham gia vào phản ứng trên *
A 9,7gam
B 9 gam
C 9,5 gam
D 9,75gam
Bảo toàn KL: \(m_{FeCl_3}+m_{KOH}=m_{Fe\left(OH\right)_3}+m_{KCl}\)
\(\Rightarrow m_{FeCl_3}=7+8,25-5,5=9,75\left(g\right)\)
Chọn D
Đúng 0
Bình luận (0)
: Cho 2,3 gam natri tác dụng hết với 100 gam nước thu được dung dịch natri hiđroxit và thoát ra 0,1 gam khí hiđro.
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng dung dịch natri hiđroxit thu được.
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
Bảo toàn khối lượng :
\(m_{Na}+m_{H_2O}=m_{NaOH}+m_{H_2}\)
\(m_{NaOH}=2.3+100-0.1=102.2\left(g\right)\)
Đúng 1
Bình luận (0)