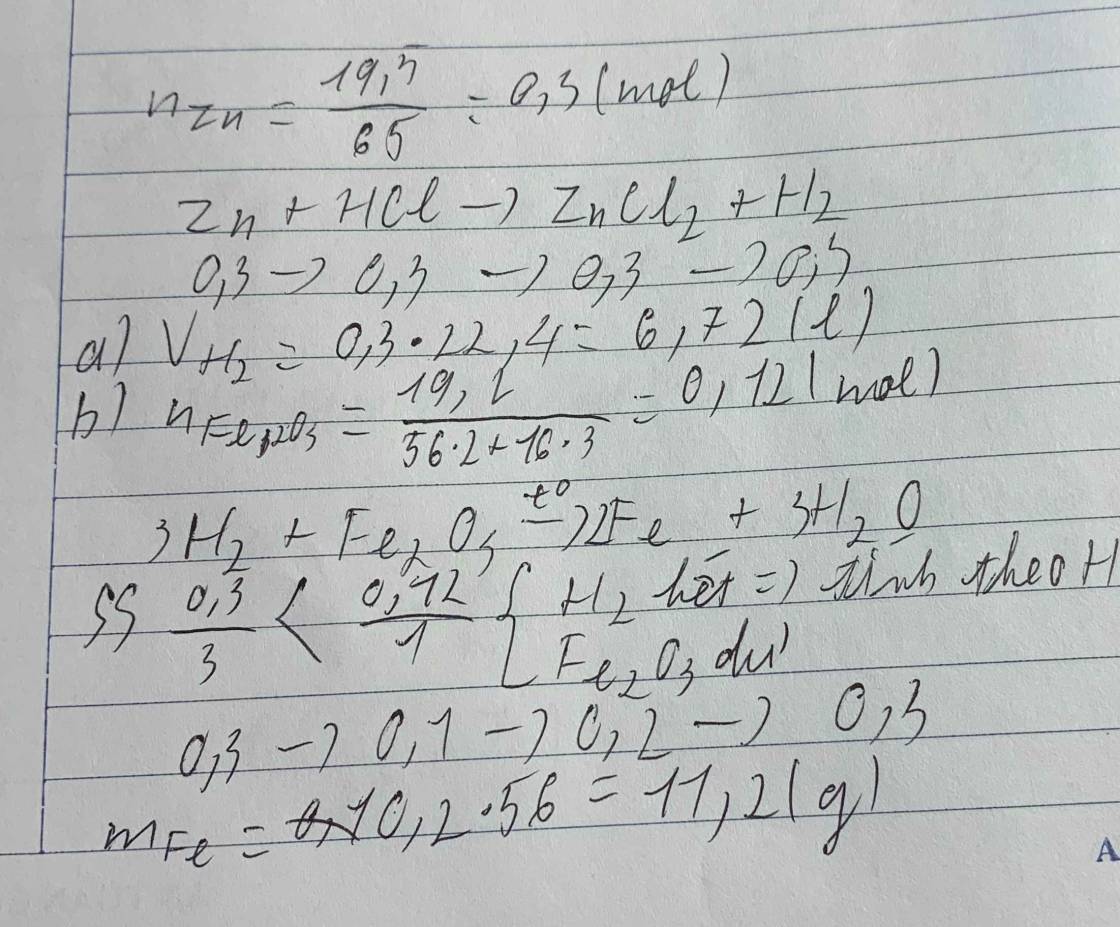Oxit nào tác dụng với khí H2, CO ở nhiệt độ cao ?

Những câu hỏi liên quan
Cho các chất sau: S, CaO, Na, P2O5, Al2O3 , PbO, Fe2O3 , C.
a/ - Chất nào tác dụng được với nước ở nhiệt độ thường? - Oxit nào tác dụng được với H2 ở nhiệt độ cao ? - Chất nào tác dụng được với O2 ở nhiệt độ thường ? ở nhiệt độ cao?
b/ Viết các PTHH đó?
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(PbO+H_2\xrightarrow[]{t^o}Pb+H_2O\)
\(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
\(S+O_2\xrightarrow[]{t^o}SO_2\)
\(4Na+O_2\rightarrow2Na_2O\)
\(C+O_2\xrightarrow[]{t^o}CO_2\)
Đúng 3
Bình luận (0)
Kim loại X tác dụng với H2SO4 loãng cho khí H2. Mặt khác, oxit của X bị khí H2 khử thành kim loại nhiệt độ cao. X là kim lại nào?
A. Fe.
B. Al.
C. Mg.
D. Cu.
Al2O3, MgO không bị H2 khử ở nhiệt độ cao ⇒ Loại B, C.
Cu không tác dụng với dung dịch H2SO4 loãng ⇒ Loại D.
X có thể là Fe:
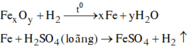
Đáp án A.
Đúng 0
Bình luận (0)
Kim loại X tác dụng với H2SO4 loãng cho khí H2. Mặt khác‚ oxit của X bị H2 khử thành kim loại ở nhiệt độ cao. X có thể là
A. Fe.
B. Cu.
C. Al.
D. Mg
Chọn A
X tác dụng với H2SO4 loãng tạo H2 → X là kim loại đứng trước H → Loại Cu
Oxit của X bị H2 khử → X phải đứng sau Al → Loại Mg và Al.
Đúng 0
Bình luận (0)
Khử hoàn toàn m gam Fe2O3 ở nhiệt độ cao bằng khí CO, lượng Fe thu được sau phản ứng cho tác dụng hoàn toàn với dung dịch axit HCl. Nếu dùng lượng khí H2 vừa thu được để khử oxit của một kim loại R (hoá trị II) thành kim loại thì khối lượng oxit bị khử cũng bằng m gam.a. Viết các phương trình hoá học.b. Tìm công thức hóa học của oxit
Đọc tiếp
Khử hoàn toàn m gam Fe2O3 ở nhiệt độ cao bằng khí CO, lượng Fe thu được sau phản ứng cho tác dụng hoàn toàn với dung dịch axit HCl. Nếu dùng lượng khí H2 vừa thu được để khử oxit của một kim loại R (hoá trị II) thành kim loại thì khối lượng oxit bị khử cũng bằng m gam.
a. Viết các phương trình hoá học.
b. Tìm công thức hóa học của oxit
a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3 CO_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$RO + H_2 \xrightarrow{t^o} R + H_2O$
b)
Coi m = 160(gam)$
Suy ra: $n_{Fe_2O_3} = 1(mol)$
Theo PTHH :
$n_{RO} = n_{H_2} = n_{Fe} = 2n_{Fe_2O_3} = 2(mol)$
$M_{RO} = R + 16 = \dfrac{160}{2} = 80 \Rightarrow R = 64(Cu)$
Vậy oxit là CuO
Đúng 3
Bình luận (2)
Cho các chất sau:K,P,BaO,CuO,Fe2O3,Al,SO3,CO a.chất nào tác dụng với O2 ở nhiệt độ thường?Nhiệt độ cao? Chất nào tác dụng với H2 ở nhiệt độ thích hợp? Chất nào tâc dụng với H2O ở nhiệt độ thường b.Viết phương trình hoá học và ghi lại loại phản ứng đã học
4K+O2-to>2K2O (hóa họp )
4P+5O2-to>2P2O5 (hóa họp )
4Al+3O2-to>2al2O3 (hóa họp )
2CO+O2-to>2CO2 (hóa họp )
-
CuO+H2-to>Cu+H2O (oxi hóa khử )
Fe2O3+3H2-to2>Fe+3H2O (oxi hóa khử)
-
2K+2H2O->2KOH+H2 (thế )
BaO+H2O->Ba(OH)2(hóa họp )
SO3+H2O->H2SO4 (hóa họp )
Đúng 3
Bình luận (1)
Oxit nào dưới đây không tác dụng với H2 ở nhiệt độ thích hợp?
A. CaO B. CuO
C. FeO D. ZnO
Xem thêm câu trả lời
Cho 1,5 g một oxit sắt tác dụng với khí H2 nhiệt độ cao thu được 1,05 g sắt. Tim CTHH của oxit sắt
Số mol sắt thu được là 1,05/56=0,01875 (mol).
Số mol oxi trong oxit sắt là (1,5-1,05):16=0,028125 (mol).
Gọi CTHH của oxit sắt là FexOy.
x:y=0,01875:0,028125=2:3.
Vậy oxit sắt cần tìm là Fe2O3.
Đúng 1
Bình luận (0)
\(Fe_xO_y+yH_2->xFe+yH_2O\)
\(nFe=\dfrac{1,05}{56}=0,01875\left(mol\right)\)
Bảo toàn Fe : \(\dfrac{1}{x}nFe=nFe_xO_y=\dfrac{0,01875}{x}\left(mol\right)\)
Ta có :
\(\dfrac{0,01875}{x}.\left(56x+16y\right)=1,5\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(\Rightarrow CTHH:Fe_2O_3\)
Đúng 1
Bình luận (0)
Cho 19,5 g kẽm tác dụng hết với dung dịch axit clohiđric. a. Tính thể tích khí H2 sinh ra (ở đktc). b. Nếu dùng thể tích H2 trên để khử 19,2 g sắt (III) oxit ở nhiệt độ cao thì thu được bao nhiêu gam sắt
Cho 180g sắt (III) oxit Fe2O3 tác dụng vừa đủ với 70g cacbon oxit CO ở nhiệt độ cao, thu được sắt Fe và 110g khí cacbonic CO2. Khối lượng sắt thu được là : A. 40g B. 80g C. 120g D. 140g Giúp mình đi mà .
Bảo toàn KL: \(m_{Fe_2O_3}+m_{CO}=m_{Fe}+m_{CO_2}\)
\(\Rightarrow m_{Fe}=180+70-110=140\left(g\right)\)
Chọn D
Đúng 1
Bình luận (0)
Người ta dẫn khí H2 dư vào bình chứa 34.8 gam oxit sắt ở nhiệt độ cao thu được chất rắn A chỉ chứa sắt.Cho A tác dụng hết với dung dịch HCl sinh ra 10.08 Lít H2 đo ở đktc. Biết rằng phản ứng xảy ra hoàn toàn, tìm công thức hoá của oxit sắt.
\(Fe_xO_y\)
\(n_{Fe_2O_n}=\dfrac{34,8}{56x+16n}\)
\(Fe_xO_y+yH_2\rightarrow\left(t^o\right)xFe+yH_2O\)
\(\dfrac{34,8}{56x+16y}\) -----> \(\dfrac{34,8x}{56x+16y}\) ( mol )
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,45 0,45 ( mol )
Ta có:
\(\dfrac{34,8x}{56x+16y}=0,45\)
\(\Leftrightarrow34,8x=25,2x+7,2y\)
\(\Leftrightarrow x=0,75y\)
\(\Leftrightarrow4x=3y\)
\(\Leftrightarrow x=3;y=4\)
\(\Rightarrow CTHH:Fe_3O_4\)
Đúng 1
Bình luận (0)