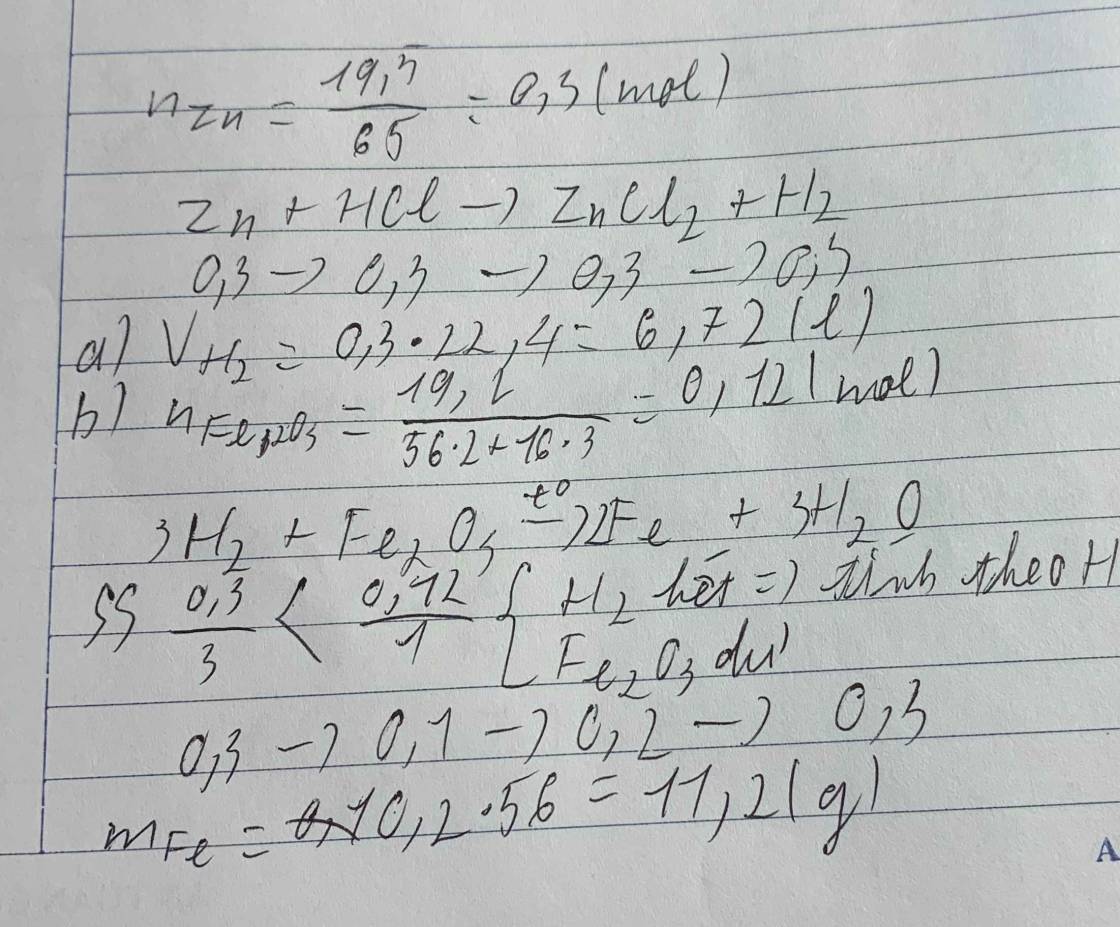khử hết 2g đồng (II) oxit bằng khí H2 ở nhiệt độ cao. thể tích khí H2 ở (đktc) cần dùng là?

Những câu hỏi liên quan
Khử hết 4 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) cần dùng là
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)=n_{H_2}\) \(\Rightarrow V_{H_2}=0,05\cdot22,4=1,12\left(l\right)\)
Đúng 2
Bình luận (0)
khử hoàn toàn 48g đồng (II) oxit bằng khí hidro ở nhiệt độ cao thu dc kim loại đồng và nc
tính gam đồng kim loại thu dc
tính thể tích khí h2 (đctc) cần dùng
PTHH: CuO+H2→H2O+Cu nCuO=4880=0,6 mol.
Bảo toàn nguyên tố: Số mol đồng kim loại thu được là: nCu=0,6 mol. \
Số gam đồng thu được là: mCu=0,6×64=38,4g
Số mol khí Hidro cần dùng là: nH2=nCuO=0,6 mol
Thể tích khí Hidro cần dùng là: V=0,6×22,4=13,44l
Đúng 2
Bình luận (0)
\(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6 0,6
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\\
V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 0
Bình luận (0)
Dùng khí hiđro để khử toàn bộ hỗn hợp gồm 24,0 gam đồng(II)oxit và 16,0 gam sắt(III)oxit ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) dùng để khử hết hỗn hợp oxit trên là
`CuO+ H_2 -> Cu+ H_2O`
`0,03 ----0,03` mol
`Fe_2O_3+ 3H_2 ->2Fe + 3H_2O`
`0,1-------0,3` mol
`n_(CuO) = 2,4/80 =0,03` mol
`n_(Fe_2O_3)=16/160 =0,1` mol
`=> V_(H_2)=(0,3+0,03).22,4=7,392 l`
Đúng 0
Bình luận (1)
Khử hoàn toàn 8 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Hãy tính thể tích khí hiđro (đktc) cần dùng.(Cho Cu = 64; O = 16)
\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{8}{80}=0,1\left(mol\right)\)
PTHH: \(CuO+H_2\rightarrow Cu+H_2O\)
.............1.............1...............................
.............0,1...........0,1...........................
\(V_{H_2\left(ĐKTC\right)}=n_{H_2}\cdot22,4=0,1\cdot22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
nCuO=8/80=0,1(mol)
CuO+H2->Cu+H2O
1 : 1 : 1 : 1 (mol)
0,1: 0,1 : 0,1: 0,1 (mol)
VH2=0,1x22,4=2,24(lít)
Đúng 1
Bình luận (0)
1) Dùng 4,48 lít khí H2(đktc) khử hoàn toàn đồng (II) oxit ở nhiệt độ cao. Tính khối lượng đồng sinh ra trong phản ứng trên?
2) Trong phòng thí nghiệm người ta điều chế O2 bằng cách nung nóng kali clorat xúc tác manga dioxit
a) Tính thể tích oxi (đktc) thu được khi có 36,75g kali clorat bị phân hủy
b) Lượng oxi thu được đốt cháy được bao nhiêu gam sắt?
1)
H2+CuO->Cu+H2O
0,2-----------0,2 mol
nH2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m Cu=0,2.64=12,8g
2)
2KClO3-to>2KCl+3O2
0,3----------------------0,45 mol
n KClO3=\(\dfrac{36,75}{122,5}\)=0,3 mol
=>VO2=0,45.22,4=10,08l
3Fe+2O2-to>Fe3O4
0,675--0,45 mol
=>m Fe=0,675.56=37,8g
Đúng 3
Bình luận (2)
Cho 19,5 g kẽm tác dụng hết với dung dịch axit clohiđric. a. Tính thể tích khí H2 sinh ra (ở đktc). b. Nếu dùng thể tích H2 trên để khử 19,2 g sắt (III) oxit ở nhiệt độ cao thì thu được bao nhiêu gam sắt
Khử 48 gam đồng 2 oxit khí H2,hãy:
a) tính số gam đồng kim loại thu được
b)tính thể tích khí H2 (ở đktc) cần dùng
\(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6 0,6 0,6
\(m_{Cu}=0,6.64=38,4g\\
V_{H_2}=0,6.22,4=13,44L\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 12,8 gam đồng trong lọ chứa khí oxi
a) Viết PTHH xảy ra.
b) Tính khối lượng đồng(II)oxit thu được.
c) Tính thể tích khí Hidro (đktc) cần dùng để khử hoàn toàn lượng đồng (II)oxit trên ở nhiệt độ cao.
Cho kim loại nhôm phản ứng hoàn toàn với 9,8 gam H2 SO4
a )viết phương trình hóa học xảy ra
b )Tính khối lượng Al đã tham gia
c )Tính thể tích hình H2 (đktc) thu được
d) dùng hết dùng hết lượng khí trên để khử đồng (3) oxit ở nhiệt độ cao tính khối lượng Cu thu được