Cho 35.2g hỗn hợp X gồm fe và cuo tác dụng với h2so4 loãng thu được 4.48 lít dung dịch A
a) viết PTHH xảy ra
b) tính khối lượng hỗn hợp ban đầu
c) cho dd A tác dụng với Bacl2 thu được kết tủa đen .Tính khối lượng kết tủa
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư), thu được 2,464 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư), thu được 23,9g kết tủa màu đen.
a) Viết các phương trình hóa học của phản ứng đã xảy ra.
b) Hỗn hợp khí thu được gồm những khí nào? Thể tích mỗi khí là bao nhiêu (đktc)?
c) Tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu?
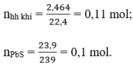
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.
Hòa tan hoàn toàn hỗn hợp gồm Mg và Fe2O3 trong dđ HCl thu được dd X và thoát ra 3,36 lít H2 (đkc). Cho dung dịch X tác dụng với dd KOH dư thu được kết tủa Y. Nung Y đến khối lượng không đổi được 22 gam chất rắn. a) Viết các PTHH xảy ra. b) Tính % khối lượng Mg và Fe2O3 ban đầu.
a)
Mg + 2HCl --> MgCl2 + H2
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
MgCl2 + 2KOH + 2KCl + Mg(OH)2
FeCl3 + 3KOH --> 3KCl + Fe(OH)3
Mg(OH)2 --to--> MgO + H2O
2Fe(OH)3 --to--> Fe2O3 + 3H2O
b) Gọi số mol Mg, Fe2O3 là a, b (mol)
Theo PTHH: \(a=n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: \(n_{MgO}=n_{Mg}=a=0,15\left(mol\right)\)
=> \(n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=\dfrac{22-0,15.40}{160}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Fe_2O_3\left(bđ\right)}=n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=0,1\left(mol\right)\)
=> b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{0,15.24+0,1.160}.100\%=18,37\%\\\%m_{Fe_2O_3}=\dfrac{0,1.160}{0,15.24+0,1.160}.100\%=81,63\%\end{matrix}\right.\)
cho 12g hỗn hợp fe và cu tác dụng với hcl vừa thu đc dd X và 2,24l khí h2 a) viết pthh xảy ra b) tính % khối lượng của mỗi kim loại trong hỗn hợp ban đầu c) cho 100ml dd naoh 1M vào dd X , tính khối lượng kết tủa sau pứ
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
a)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6\left(g\right)\)
b)\(\Rightarrow\%m_{Fe}=\dfrac{5,6}{12}\cdot100\%=46,67\%\) \(\Rightarrow\%m_{Cu}=100\%-46,67\%=53,33\%\)
c)\(n_{NaOH}=0,1\cdot1=0,1mol\)
\(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,1 0,1 0,1
\(m_{Fe\left(OH\right)_2}=0,1\cdot90=9\left(g\right)\)
cho 12g hỗn hợp gồm Fe và FeO tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng thu được 5,6 lít khí SO2 (đktc)
a, viết các PTHH xảy ra?
b, tính thành phần % theo khối lượng của mỗi chất trong hỗn hợp đầu?
c, dẫn toàn bộ khí SO2 thu được ở trên qua 300ml dung dịch NaOH 2M. Cô cạn dung dịch thu được bao nhiêu gam chất rắn khan?
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.2.....................................0.2\)
\(m_{Fe}=0.2\cdot56=11.2\left(g\right)\)
\(m_{Fe}=m_{hh}=11.2\left(g\right)\)
=> Đề sai
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(n_{H_2}=n_{Fe}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(m_{CuO}=35.2-0.2\cdot56=24\left(g\right)\)
\(n_{CuO}=\dfrac{24}{80}=0.3\left(mol\right)\)
\(\%Fe=\dfrac{11.2}{35.2}\cdot100\%=31.82\%\)
\(\%CuO=100-31.82=68.18\%\)
\(n_{H_2SO_4}=0.2+0.3=0.5\left(mol\right)\)
\(m_{H_2SO_4}=0.5\cdot98=49\left(g\right)\)
\(C\%H_2SO_4=\dfrac{49}{800}\cdot100\%=6.125\%\)
\(m_{FeSO_4}=0.2\cdot152=30.4\left(g\right)\)
\(m_{CuSO_4}=0.3\cdot160=48\left(g\right)\)
Cho hỗn hợp Y gồm metanol và phenol tác dụng với Na dư thu được 2.24 lít khí (đktc) . Nếu cho hỗn hợp trên tác dụng với dung dịch Br2 thì thu được 13.24 gam kết tủa ( 2,4,6-tribromphenol ) a) tính khối lượng hỗn hợp ban đầu. b) Nếu cho Y tác dụng với dd HNO3 thì khối lượng kết tủa thu được là bao nhiêu ?
cho 16,32g hỗn hợp (x) gồm al,mg,ba tác dụng vừa đủ với dung dịch h2so4 loãng thì thu được 10,08 lít khí h2 (đktc), dung dịch (y) và tạo ra 13,98g kết tủa. a)tính khối lượng mỗi kim loại trong hỗn hợp (x) b) cho từ từ dd koh 2mol/lít vào dd (y). tính thể tích dd koh cần dùng để tạo ra kết tủa duy nhất
Cho 7,8 gam hỗn hợp hai kim loại Mg và Al tác dụng với dung dịch H2SO4 loãng dư. Khi phản ứng kết thúc người ta thu được 8,96 lít khí (đktc).
a. Viết các phương trình hoá học xảy ra
b. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
c. Tính thể tích dung dịch H2SO4 2 M đã tham gia phản ứng
a)
2Al + 3H2SO4 → Al2(SO4)3 +3H2
Mg + H2SO4 → MgSO4 + H2
b. n H2 = 8,96/22,4 =0,4 mol
Gọi x và y là số mol của Al và Mg ta có hệ
27x+ 24y = 7,8 (1)
1,5x+ y = 0,4 (2)
Từ 1 và 2 => x = 0,2 ; y = 0,1
Khối lượng của Al và Mg là:
mAg = 0,2.27=5,4(gam)
mMg = 7,8 – 5,4 = 2,4(gam)
c. Theo phương trình số mol của H2SO4 là : 0,3 + 0,1 = 0,4(mol)
Thể tích dung dịch H2SO4 2M đã tham gia phản ứng là:
V = 0,4/2=0,2 lít
Gọi nMg = a (mol); nAl = b (mol)
=> 24a + 27b = 7,8 (1)
nH2 = 8,96/22,4 = 0,4 (mol)
PTHH:
Mg + H2SO4 -> MgSO4 + H2
a ---> a ---> a ---> a
2Al + 3H2SO4 -> 2Al2(SO4)3 + 3H2
b ---> 1,5b ---> b ---> 1,5b
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
mMg = 0,1 . 24 = 2,4 (g)
mAl = 0,2 . 27 = 5,4 (g)
nH2SO4 = 0,1 + 0,3 . 1,5 = 0,4 (mol)
VddH2SO4 = 0,3/2 = 0,2 (l)
a.b.\(n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Al}=y\end{matrix}\right.\)
\(Mg+H_2SO_4\left(l\right)\rightarrow MgSO_4+H_2\)
x x ( mol )
\(2Al+3H_2SO_4\left(l\right)\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
y 3/2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+27y=7,8\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,1.24=2,4g\)
\(\Rightarrow m_{Al}=0,2.27=5,4g\)
c.\(Mg+H_2SO_4\left(l\right)\rightarrow MgSO_4+H_2\)
0,1 0,1 ( mol )
\(2Al+3H_2SO_4\left(l\right)\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(V=\dfrac{n}{C_{M\left(H_2SO_4\right)}}=\dfrac{0,1+0,3}{2}=0,2l\)