Cho 2,3 gam Na tác dụng với rượu etylic, hãy viết pthh, tính khối lượng rượu etylic, tính thể tích khí sinh ra ở đktc

Những câu hỏi liên quan
Đốt cháy hoàn toàn 2,3 gam rượu etylic trong không khí.
a./ Viết PTHH.
b./ Tính khối lượng khí cacbonic sinh ra sau phản ứng.
c./ Tính thể tích không khí cần dùng cho phản ứng trên.
Đọc tiếp
Đốt cháy hoàn toàn 2,3 gam rượu etylic trong không khí.
a./ Viết PTHH.
b./ Tính khối lượng khí cacbonic sinh ra sau phản ứng.
c./ Tính thể tích không khí cần dùng cho phản ứng trên.
\(n_{C_2H_5OH}=\dfrac{2,3}{46}=0,05\left(mol\right)\)
PTHH: C2H5OH + 3O2 --to--> 2CO2 + 3H2O
0,05----------------->0,1
=> mCO2 = 0,1.44 = 4,4 (g)
Đúng 1
Bình luận (0)
a) PTHH \(C_2H_5OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
b) Khối lượng mol của rượu etylic là \(M_{etylic}=2M_C+5M_H+M_O+M_H=2.12+5.1+16+1=46\left(g/mol\right)\)
Số mol rượu etylic tham gia phản ứng là \(n_{etylic}=\dfrac{m_{etylic}}{M_{etylic}}=\dfrac{2,3}{46}=0,05\left(mol\right)\)
PTHH \(C_2H_5OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
TL mol 1 : 3 : 2 : 3
pứ mol 0,05 : ? : ? : ?
\(\Rightarrow n_{CO_2}=0,1\left(mol\right)\)
Khối lượng mol của CO2 là \(M_{CO_2}=M_C+2M_O=12+2.16=44\left(g/mol\right)\)
Khối lượng CO2 hình thành là \(m_{CO_2}=n_{CO_2}.M_{CO_2}=0,1.44=4,4\left(g\right)\)
c) Dễ dàng tính được \(n_{O_2}=1,5\left(mol\right)\)
Thể tích khí oxi cần dùng là \(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36\left(l\right)\)
Thể tích không khí cần dùng là \(V_{kk}=\dfrac{V_{O_2}.100\%}{21\%}=\dfrac{3,36.100}{21}=16\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 10ml rượu etylic 920 (khối lượng riêng của rượu etylic là 0,8 gam/ml) tác dụng hết với Na thì thể tích sinh ra là
A. 1,12 lít
B. 1,68 lít
C. 1,792 lít
D. 2,285 lít
Chọn đáp án D
(1) Câu này các em cần chú ý Na tác dụng cả với nước và ancol.Nhiều bạn không để ý là bị ăn hành ngay đấy.
(2) Cần nhớ độ rượu là thể tích ml rượu có trong 100 ml dung dịch rượu
Vậy ta có:
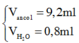
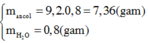
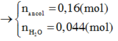

=>V=2,285(lit)
Đúng 0
Bình luận (0)
Cho 2,9g rượu etylic tác dụng hết với Na a. Tính thể tích khí H2 thu được ở đktc ? b. Tính thể tích rượu etylic đã dùng? Biết Dr= 0,8 g/ml
\(nC_2H_5OH=\dfrac{2,9}{46}=0,06\left(mol\right)\)
\(C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
0,06 0,06 0,06 0,03 (mol)
VH2 = 0,03.22,4= 0,672 (l)
V = m /D
=> V rượu etylic = 2,9 / 0,8 = 3,625 (ml)
Đúng 1
Bình luận (0)
a. Cho 300 gam dung dịch CH3COOH 5% tác dụng với một lượng dư Zn. Tính thể tích khí H2 sinh ra ở điều kiện tiêu chuẩn. b. Cho 300 gam dung dịch CH3COOH 5% nói trên tác dụng với 100 ml dung dịch rượu etylic 2M. Tính khối lượng etylic axetat thu được sau phản ứng (Cho C=12;H=1;O=16;Ca=40) Giúp mik vs ạ.
\(n_{CH_3COOH}=\dfrac{300\cdot5\%}{60}=0.25\left(mol\right)\)
\(2CH_3COOH+Zn\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
\(0.25........................................................0.125\)
\(V_{H_2}=0.125\cdot22.4=2.8\left(l\right)\)
\(n_{C_2H_5OH}=0.1\cdot2=0.2\left(mol\right)\)
\(CH_3COOH+C_2H_5OH⇌CH_3COOC_2H_5+H_2O\left(ĐK:H_2SO_{4\left(đ\right)},t^0\right)\)
\(0.2......................0.2.....................0.2\)
\(\Rightarrow CH_3COOHdư\)
\(m_{CH_3COOC_2H_5}=0.2\cdot88=17.6\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 4,6 g rượu etylic tác dụng với natri a, viết pt hóa học b, tính thể tích khí hiđro thoát ra ở đktc c, tính khối lượng sản phẩm Natrietylat tạo thành
\(n_{C_2H_5OH}=\dfrac{4,6}{46}=0,1mol\)
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
0,1 0,1 0,05
\(V_{H_2}=0,05\cdot22,4=1,12l\)
\(m_{C_2H_5ONa}=0,1\cdot68=6,8g\)
Đúng 3
Bình luận (0)
nC2H5OH=4,6/46=0,1mol
2C2H5OH+2Na→2C2H5ONa+H2
0,1 0,1 0,05
VH2=0,05⋅22,4=1,12l
mC2H5ONa=0,1⋅68=6,8g
Đúng 0
Bình luận (0)
a.Cho 300 gam dung dịch CH3COOH 5% tác dụng với một lượng dư Zn. Tính thể tích khí H2 sinh ra ở điều kiện tiêu chuẩn. b. Cho 300 gam dung dịch CH3COOH 5% nói trên tác dụng với 100 ml dung dịch rượu etylic 2M. Tính khối lượng etylic axetat thu được sau phản ứng (Cho C=12;H=1;O=16;Ca=40)
a) n CH3COOH = 300.5%/60 = 0,25(mol)
Zn + 2CH3COOH $\to$ (CH3COO)2Zn + H2
Theo PTHH :
n H2 = 1/2 n CH3COOH = 0,25/2 = 0,125(mol)
V H2 = 0,125.22,4 = 2,8(lít)
b) n C2H5OH = 0,1.2 = 0,2(mol)
\(CH_3COOH + C_2H_5OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O\)
Ta thấy :
n CH3COOH = 0,25 > n C2H5OH = 0,2 => CH3COOH dư
n CH3COOC2H5 = n C2H5OH = 0,2 mol
=> m CH3COOC2H5 = 0,2.88 = 17,6 gam
Đúng 1
Bình luận (0)
a, Hãy lập sơ đồ sản xuất rượu etylic từ tinh bột và viết các PTHH xảy ra b,Tính khối lượng rượu etylic và thể tích khí cacbonic thu được ( ở đktc) khi dùng 4 tấn nguyên liệu (chứa 80% tinh bột ) để sản xuất rượu. Biết hiệu suất của cả quá trình phản ứng đạt 65%
a. Cho 14 gam rượu etylic tác dụng với Natri (dư)
b. Tính khối lượng sản phẩm
c. Tính thể tích khí H2(đktc).
giải ra rõ ràng giúp mình ạ, mình cảm ơn
\(n_{C_2H_5OH}=\dfrac{14}{46}=\dfrac{7}{23}\left(mol\right)\)
\(C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(\dfrac{7}{23}...................\dfrac{7}{23}......\dfrac{7}{46}\)
\(m_{C_2H_5ONa}=\dfrac{7}{23}\cdot68=20.7\left(g\right)\)
\(V_{H_2}=\dfrac{7}{46}\cdot22.4=3.4\left(l\right)\)
Đúng 2
Bình luận (0)
\(a) 2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2\\ n_{C_2H_5ONa} = n_{C_2H_5OH} = \dfrac{14}{46} = \dfrac{7}{23}(mol)\\ m_{C_2H_5ONa} = \dfrac{7}{23}.68 = 20,7(gam)\\ n_{H_2} = \dfrac{1}{2}n_{C_2H_5OH} = \dfrac{7}{46}(mol)\\ m_{H_2} = \dfrac{7}{46}.2 = \dfrac{7}{23}(gam)\\ b) V_{H_2} = \dfrac{7}{46}.22,4 = 3,41(lít)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 34,5 gam rượu etylic a,Tính thể tích khí CO2 thoát ra ở đktc b,Cho toàn bộ lượng rượu trên tác dụng với dung dịch axit axetic (có axit axetic làm chất xúc tác) thì khối lượng este là bao nhiêu?biết hiệu xuất =90%
\(n_{C2H5OH}=\dfrac{34,5}{46}=0,75\left(mol\right)\)
Pt : \(C_2H_5OH+3O_2\xrightarrow[]{t^o}2CO_2+3H_2O\)
0,75 1,5
\(CH_3COOH+C_2H_5OH⇌CH_3COOC_2H_5+H_2O\)
0,75 0,75 0,75
a) \(V_{CO2\left(dktc\right)}=1,5.22,4=33,6\left(l\right)\)
b) \(m_{CH3COOC2H5\left(lt\right)}=0,75.88=66\left(g\right)\)
⇒\(m_{CH3COOC2H5\left(tt\right)}=\) \(66.90\%=59,4\left(g\right)\)
Chúc bạn học tốt
Đúng 3
Bình luận (2)























