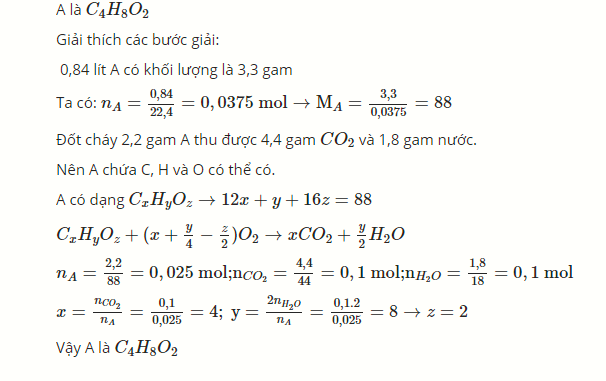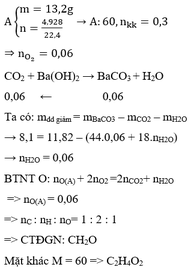Khi đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 8,1 g H2O. Ngoài ra không có chất nào khác. Biết rằng 0,84 lít hơi hợp chất A (DKTC) có khối lượng là 3,3g; TÌm cthh của hợp chất A

Những câu hỏi liên quan
đốt cháy hoàn toàn 2.2 gam hợp chất hữu cơ A thu được 4.4 gam CO₂ và 1.8 gam H₂O, ngoài ra không còn chất nào khác. Biết rằng 0.84 lít hơi hợp chất A(đktc) có khối lượng là 3.3 gam. Xác định CTPT của hợp chất A
Đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,2\left(mol\right)\)
Xét mC + mH = 0,1.12 + 0,2.1 = 1,4 (g) < 2,2 (g)
=> A chứa C, H, O
\(n_O=\dfrac{2,2-1,4}{16}=0,05\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,05 = 2 : 4 : 1
=> CTPT: (C2H4O)n
\(M_A=\dfrac{3,3}{\dfrac{0,84}{22,4}}=88\left(g/mol\right)\)
=> n = 2
=> CTPT: C4H8O2
Đúng 2
Bình luận (0)
\(n_A=\dfrac{0,84}{22,4}=0,0375 (mol) \Rightarrow M_A = {3,3}{0,0375}=88 ( mol) \)
\(A có dạng : C_xH_yO_z \rightarrow 12x+y+16z = 88 \)
\(C_xH_yO_z + ( x+\dfrac{y}{4}-\dfrac{z}{2}) O_2 \rightarrow xCO_2+\dfrac{x}{y}H_2O \)
\(n_A = \dfrac{2,2}{88}=0,025 (mol) \)
\(n_{CO_2} = \dfrac{4,4}{44}=0,1(mol) \)
\(n_{H_2O} = \dfrac{1,8}{18}=0,1(mol) \)
\(x=\dfrac{n_{CO_2}}{n_A} = \dfrac{0,1}{0,025}=4;y=\dfrac{2n_{H_2O}}{n_A} =\dfrac{0,1.2}{0,025}=8 \rightarrow z=2\)
Đúng 0
Bình luận (0)
Khi đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 4,4g Co2 và 1,8g H2O .Ngoài ra khôbg còn chất nào khác . Biết rằng 0,84 lít hợp chất A (đktc) có khối lượng là 3,3g ; tìm CTHH của hợp chất A
Ta có:
\(n_X=\frac{0,84}{22,4}=0,0375\left(mol\right)\)
\(\Rightarrow M_A=\frac{3,3}{0,0375}=88\)
Đốt cháy 2,2 gam A thu được 4,4 gam CO2CO2 và 1,8 gam nước.
Nên A chứa C, H và O có thể có.
A có dạng \(C_xH_yO_z\Rightarrow12x+y+16z=88\)
\(C_xH_yO_z+\left(x+\frac{y}{4}+\frac{x}{2}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
\(n_A=\frac{2,2}{88}=0,025\left(mol\right)\)
\(n_{CO2}=\frac{4,4}{44}=0,1\left(mol\right)\)
\(n_{H2O}=\frac{1,8}{18}=0,1\left(mol\right)\)
\(x=\frac{n_{CO2}}{n_A}=\frac{0,1}{0,025}=4;y=\frac{2n_{H2O}}{n_A}=\frac{0,1.2}{0,025}=8\Rightarrow z=2\)
Vậy A là C4H8O2
Đúng 1
Bình luận (0)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!Bài 1:Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.Bài 2:Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/...
Đọc tiếp
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 6,6g CO2 và 3,6g H2O. Biết A có tỉ khối so với khí H2 là 22. Xác định công thức phân tử của hợp chất hữu cơ.
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Bảo toán C: nC(A) = 0,15 (mol)
Bảo toàn H: nH(A) = 0,2.2 = 0,4 (mol)
=> \(n_O=\dfrac{2,2-0,15.12-0,4.1}{16}=0\left(mol\right)\)
Xét nC : nH = 0,15 : 0,4 = 3:8
=> CTPT: (C3H8)n
Mà MA = 22.2 = 44(g/mol)
=> n = 1
=> CTPT: C3H8
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 4,5 gam 1 hợp chất hữu cơ A thu được 6,6 gam CO2 và 2,7 gam H2O. Biết khối lượng mol của phân tử hợp chất hữu cơ là 60g/mol. Xác định CTHH của hợp chất hữu cơ
\(TrongA:n_C=n_{CO_2}=0,15\left(mol\right)\\ n_H=2n_{H_2O}=0,3\left(mol\right)\\ \Rightarrow n_O=\dfrac{4,5-12.0,15-0,3.1}{16}=0,15\left(mol\right)\\ \Rightarrow CTPT:C_xH_yO_z\\ Tacó:x:y:z=0,15:0,3:0,15=1:2:1\\ \Rightarrow CTĐGN:\left(CH_2O\right)_n\\ Tacó:\left(12+2+16\right).n=60\\ \Rightarrow n=2\\ Vậy:CTHHcủaA:C_2H_4O_2\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 6,72 lít không khí (đktc), dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thì thu được 11,82 gam kết tủa và khối lượng dung dịch Ba(OH)2 sau phản ứng giảm 8,1 gam (biết trong không khí oxi chiếm 20% thể tích). Tìm công thức phân tử của hợp chất hữu cơ A, biết rằng 13,2 gam hơi chất A đo ở đktc chiếm thể tích 4,928 lít hơi.
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 6,72 lít không khí (đktc), dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thì thu được 11,82 gam kết tủa và khối lượng dung dịch Ba(OH)2 sau phản ứng giảm 8,1 gam (biết trong không khí oxi chiếm 20% thể tích). Tìm công thức phân tử của hợp chất hữu cơ A, biết rằng 13,2 gam hơi chất A đo ở đktc chiếm thể tích 4,928 lít hơi.
hợp chất hữu cơ Y có tỉ khối hơi so với khí O2 là 1,5375. Đốt cháy hoàn toàn 1,15 g chất Y thu được 2,2g khí CO2 và 1,35g H2O. Xđ công thức phân từ của Y. Viết phương trình phản ứng đốt cháy Y và tính khối lượng sản phẩm tạo thành
Sửa đề : 1.4375
nCO2 = 2.2/44 = 0.05 (mol)
nH2O = 1.35/18 = 0.075 (mol)
mO = mY - mC - mH = 1.15 - 0.05*12 - 0.075*2 = 0.4(g)
nO = 0.4/16 = 0.025 (mol)
CT : CxHyOz
x : y : z = 0.05 : 0.15 : 0.025 = 2 : 6 : 1
CT nguyên : (C2H6O)n
MY = 1.4375*32 = 46 (g/mol)
=> 46n = 45
=> n = 1
Ct : C2H6O
Không biết đề có nhầm lẫn gì không nhưng sản phẩm có ở trên hết rồi ấy bạn ơiii
Đúng 2
Bình luận (1)
Sửa đề: \(1,5375\to 1,4375\)
\(m_{sản\ phẩm}= m_{CO_2} + m_{H_2O} = 2,2 + 1,35 = 3,55(gam)\\ n_{CO_2} = \dfrac{2,2}{44} = 0,05(mol)\\ n_{H_2O} = \dfrac{1,35}{18} = 0,075(mol)\\ n_{O_2} = \dfrac{2,2+1,35-1,15}{32} = 0,075(mol)\\ \)
Suy ra:
\(n_C = n_{CO_2} = 0,05(mol)\\ n_H = 2n_{H_2O} = 2.0,075 = 0,15(mol)\\ n_O = 2n_{CO_2} + n_{H_2O} -2n_{O_2} = 0,025\\ n_Y = \dfrac{1,15}{1,4375.32} = 0,025\)
Vậy :
Số nguyên tử C = \(\dfrac{n_C}{n_Y} = 2\)
Số nguyên tử H = \(\dfrac{n_H}{n_Y} = 6\)
Số nguyên tử O = \(\dfrac{n_O}{n_Y} = 1\)
Vậy CTPT của Y : C2H6O
\(C_2H_6O + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O\)
Đúng 1
Bình luận (1)
Đề bài: đốt cháy hoàn toàn hợp chất khí CxHy sau phản ứng thu được 6,72 lít CO2(đktc) và 7,2 g H2O. Tìm CTHH của hợp chất , biết hợp chất có tỉ khối với không khid là 1,517
ban oi online math la de giai toan chu khong phai hoa hoc nha
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b 3a và 7m 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là: A. C3H8 B. C2H6 C. C3H4O2 D. C3H6O2
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b = 3a và 7m = 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là:
A. C3H8
B. C2H6
C. C3H4O2
D. C3H6O2
Đáp án C
Vì đốt cháy A thu được CO2 và H2O nên A chứa C, H, có thể có O.
Khi đó gọi công thức phân tử của A là CxHyOz
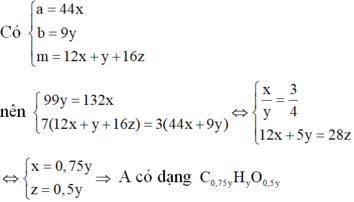
![]()
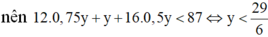
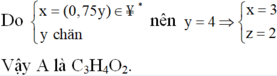
Nhận xét: Khi làm đến bước x : y = 3 :4 và kết hợp với quan sát 4 đáp án, ta có thể kết luận ngay A là C3H4O2.
Đúng 0
Bình luận (0)