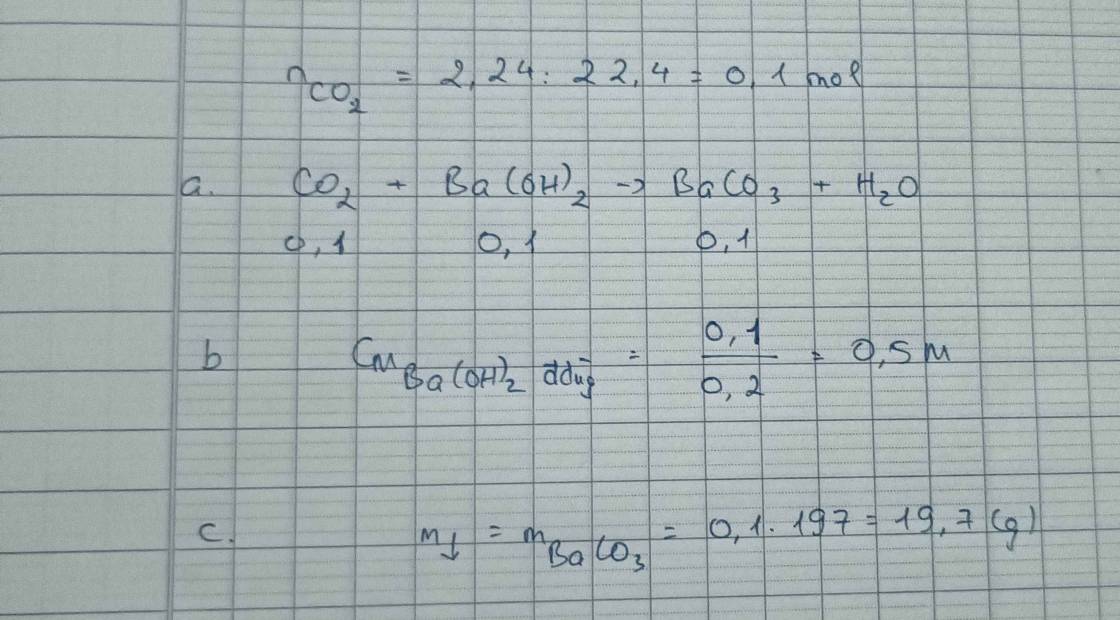Cho 4,48 lít(đktc)khí SO2 tác dụng hết với 250ml dung dịch Ba(OH)2 thu được muối sunfit và nước a)Viết phương trình hóa học b)Tính nồng độ dung dịch Ba(OH)2 đã phản ứng c)Tính khối lượng muối thu được sau phản ứng

Những câu hỏi liên quan
Dẫn 224 ml khí SO2 ( đktc ) đi qua 1,4 lít dung dịch Ca(OH)2 có nồng độ 0,02M thu được sản phẩm là muối canxi sunfit và nước
a) Viết phương trình hóa học
b) Tính khối lượng các chất sau phản ứng.
a)
PTHH : \(SO_2+Ca\left(OH\right)_2\rightarrow CáO_4+H_2O\)
b)
Ta có :
\(n_{SO_2}=\frac{0,224}{22,4}=0,01\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,01\times1,4=0,014\)
Theo ptpư : \(n_{SO_2}=n_{Ca\left(OH\right)_2}=n_{CaSO_3}=n_{H_2O}\)
Vậy nCa(OH)2 ( dư ) = \(n_{Ca\left(OH\right)_2\left(bđ\right)}-n_{Ca\left(OH\right)_2\left(pư\right)}\)
\(=0,014-0,001=0,004\left(mol\right)\)
Đúng 0
Bình luận (0)
Cho 3,36 lít khí CO2 (đktc) tác dụng 300 ml với dung dịch Ba(OH)2 sau phản ứng chỉ tạo muối BaCO3 và nước.
a) Viết phương trình hóa học.
b) Tính khối lượng kết tủa và nồng độ mol dung dịch Ba(OH)2 phản ứng.
giúp e với!
Số mol của khí cacbonic ở dktc
nCO2 = \(\dfrac{V_{CO2}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) CO2 + Ba(OH)2 → BaCO3 + H2O\(|\)
1 1 1 1
0,15 0,15 0,15
b) Số mol của bari cacbonat
nBaCO3 = \(\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
Khối lượng của bari cacbonat
mBaCO3 = nBaCO3 . MBaCO3
= 0,15 . 197
= 29,55 (g)
Số mol của dung dịch bari hidroxit
nBa(OH)2 = \(\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
300ml = 0,3l
Nồng độ mol của dung dịch bari hidroxit
CMBa(OH)2 = \(\dfrac{n}{V}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Biết 3,36 lít khí CO2 (đktc) tác dụng vừa hết với 200ml dung dịch Ca(OH)2 sản phẩm là CaCO3 và H2O. a. Viết phương trình hóa học b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng c. Tính khối lượng chất kết tủa thu được
a/ Ca(OH)2 + CO2--> CaCO3 + H2O
nCO2=3.36/22.4=0.15(mol)
nCO2=nCa(OH)2=0.15(mol)
200ml=0.2l
b/CMCa(OH)2= 0.15/0.2=0.75(M)
c/nCaCO3=nCO2=0.15(mol)
mCaCO3= 0.15 x 106=15.9(g)
Đúng 1
Bình luận (0)
Cho 1,12 lít khí CO2(đktc) tác dụng vừa hết với 100ml dung dịch Ba(OH)2, sản
phẩm là BaCO3 và H2O.
a. Viết phương trình hóa học xảy ra.
b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng.
c.Tính khối lượng chất kết tủa thu được
: Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2a/ Viết phương trình hóa học.b/ Tính nồng độ mol/lít của dung dịch Ba(OH)2 đã dùng.c/ Tính khối lượng chất kết tủa thu được
Đọc tiếp
: Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2
a/ Viết phương trình hóa học.
b/ Tính nồng độ mol/lít của dung dịch Ba(OH)2 đã dùng.
c/ Tính khối lượng chất kết tủa thu được
5. Biết 3,7185 Lít khí Sodium dioxide SO2 (đk chuẩn) tác dụng hết với
300ml dung dịch Barium hydroxide Ba(OH)2, Sản phẩm là Barium
sulfite BaSO2 và Nước
a. Viết phương trình hóa học
b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng
c. Tính khối lượng muối BaSO3 thu được
$n_{SO_2} = \dfrac{3,7185}{22,4} = 0,166(mol)$
\(SO_2+Ba\left(OH\right)_2\text{→}BaSO_3+H_2O\)
0,166 0,166 0,166 (mol)
$C_{M_{Ba(OH)_2}} = \dfrac{0,166}{0,3} = 0,553M$
$m_{BaSO_3} = 0,166.217 = 36,022(gam)$
Đúng 4
Bình luận (1)
. Cho 5,6 lít khí CO2(đktc) tác dụng vừa đủ với 100ml dung dịch Ca(OH)2.( phản ứng chỉ thu được muối trung hòa và nước)
a/ Tính nồng độ mol của dung dịch Ca(OH)2 đã dùng?
b/ Tính khối lượng chất kết tủa thu được?
\(a.n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ a.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\\ 0,25.......0,25............0,25..........0,25\left(mol\right)\\ C_{MddCa\left(OH\right)_2}=\dfrac{0,25}{0,1}=2,5\left(M\right)\\ b.m_{\downarrow}=m_{CaCO_3}=100.0,25=25\left(g\right)\)
Đúng 1
Bình luận (0)
1. Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2, sản phẩm là BaCO3 và H2O.a. Viết phương trình hóa học.b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng.c. Tính khối lượng kết tủa thu được.2. 200ml dung dịch HCl có nồng độ 3,5M hòa tan vừa hết 20 gam hỗn hợp hai oxit CuO và Fe2O3.a. Viết các phương trình hóa học.b. Tính khối lượng mỗi oxit có trong hỗn hợp đầu.a. Tính khối lượng các chất sau phản ứng.
Đọc tiếp
1. Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2, sản phẩm là BaCO3 và H2O.
a. Viết phương trình hóa học.
b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng.
c. Tính khối lượng kết tủa thu được.
2. 200ml dung dịch HCl có nồng độ 3,5M hòa tan vừa hết 20 gam hỗn hợp hai oxit CuO và Fe2O3.
a. Viết các phương trình hóa học.
b. Tính khối lượng mỗi oxit có trong hỗn hợp đầu.
a. Tính khối lượng các chất sau phản ứng.
2.
a, \(n_{HCl}=0,2.3,5=0,7\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: x 2x
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: y 6y
Ta có: \(\left\{{}\begin{matrix}80x+160y=20\\2x+6y=0,7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
b, \(m_{CuO}=0,05.80=4\left(g\right);m_{Fe_2O_3}=20-4=16\left(g\right)\)
c,
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,05 0,05
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,1 0,2
\(m_{CuCl_2}=0,05.135=6,75\left(g\right)\)
\(m_{FeCl_3}=0,1.162,5=16,25\left(g\right)\)
Đúng 2
Bình luận (0)
1.
a, \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: CO2 + Ba(OH)2 → BaCO3 + H2O
Mol: 0,1 0,1 0,1
b, \(C_{M_{ddBa\left(OH\right)_2}}=\dfrac{0,1}{0,2}=0,5M\)
c, \(m_{BaCO_3}=0,1.197=19,7\left(g\right)\)
Đúng 1
Bình luận (0)
Dẫn 22,4 ml khí SO2 (đktc) đi qua 700 ml dung dịch Ca(OH)2 có nồng độ 0,01 M, sản phẩm là muối canxi sunfit. a) Viết phương trình hóa học b) Tính khối lượng các chất sau phản ứng.