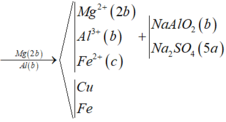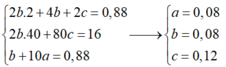tính thể tích khí h2 tối thiểu cần dùng để phản ứng hết với 30,3 gam hỗn hợp M gồm oxit và kẽm oxit và đồng 2 oxit .tỉ lệ mol tương ứng là 2:@Nguyễn Thơ nn :3

Những câu hỏi liên quan
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Đọc tiếp
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
Đọc tiếp
Hỗn hợp X gồm CuO, FeO và oxit của kim loại M (có hóa trị II không đổi) với tỉ lệ mol tương ứng là 3 : 5 : 1. Dẫn một luồng khí H2 dư đi qua 23,04 gam X nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Y. Để hòa tan hết Y cần 360 ml dung dịch HNO3 nồng độ 3M, thu được V lít (đktc) khí NO duy nhất và dung dịch Z chỉ chứa muối nitrat của kim loại. Viết các phản ứng xảy ra, xác định kim loại M và tính giá trị V.
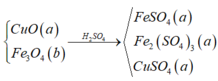
Hòa tan hết hỗn hợp gồm Fe3O4 và CuO (tỉ lệ mol 1 : 1) cần dùng dung dịch H2SO4 loãng, thu được dung dịch muối X. Cho hỗn hợp gồm Mg và Al có tỉ lệ mol tương ứng 2 : 1 vào dung dịch X, kết thúc phản ứng thu được dung dịch Y và m gam rắn Z. Cho dung dịch NaOH dư vào dung dịch Y, thấy lượng NaOH phản ứng là 35,2 gam, lấy kết tủa thu được đem nung ngoài không khí đến khối lượng không đổi thu được 16,0 gam hỗn hợp gồm hai oxit. Giá trị của m là A. 14,08 gam B. 11,84 gam C. 13,52 gam D. 15,20 gam
Đọc tiếp
Hòa tan hết hỗn hợp gồm Fe3O4 và CuO (tỉ lệ mol 1 : 1) cần dùng dung dịch H2SO4 loãng, thu được dung dịch muối X. Cho hỗn hợp gồm Mg và Al có tỉ lệ mol tương ứng 2 : 1 vào dung dịch X, kết thúc phản ứng thu được dung dịch Y và m gam rắn Z. Cho dung dịch NaOH dư vào dung dịch Y, thấy lượng NaOH phản ứng là 35,2 gam, lấy kết tủa thu được đem nung ngoài không khí đến khối lượng không đổi thu được 16,0 gam hỗn hợp gồm hai oxit. Giá trị của m là
A. 14,08 gam
B. 11,84 gam
C. 13,52 gam
D. 15,20 gam
Hòa tan hết hỗn hợp gồm Fe3O4 và CuO (tỉ lệ mol 1 : 1) cần dùng dung dịch H2SO4 loãng, thu được dung dịch muối X. Cho hỗn hợp gồm Mg và Al có tỉ lệ mol tương ứng 2 : 1 vào dung dịch X, kết thúc phản ứng thu được dung dịch Y và m gam rắn Z. Cho dung dịch NaOH dư vào dung dịch Y, thấy lượng NaOH phản ứng là 35,2 gam, lấy kết tủa thu được đem nung ngoài không khí đến khối lượng không đổi thu được 16,0 gam hỗn hợp gồm hai oxit. Giá trị của m là A. 14,08 gam B. 11,84 gam C. 13,52 gam D. 15,20 gam
Đọc tiếp
Hòa tan hết hỗn hợp gồm Fe3O4 và CuO (tỉ lệ mol 1 : 1) cần dùng dung dịch H2SO4 loãng, thu được dung dịch muối X. Cho hỗn hợp gồm Mg và Al có tỉ lệ mol tương ứng 2 : 1 vào dung dịch X, kết thúc phản ứng thu được dung dịch Y và m gam rắn Z. Cho dung dịch NaOH dư vào dung dịch Y, thấy lượng NaOH phản ứng là 35,2 gam, lấy kết tủa thu được đem nung ngoài không khí đến khối lượng không đổi thu được 16,0 gam hỗn hợp gồm hai oxit. Giá trị của m là
A. 14,08 gam
B. 11,84 gam
C. 13,52 gam
D. 15,20 gam
Đề: Đốt cháy hoàn toàn 6,3 gam hỗn hợp X gồm kim loại Mg và Al (tỉ lệ tương ứng 3 : 2) cần dùng vừa đủ V lít khí O2 (đktc), thu được hỗn hợp Y gồm hai oxit bazo.
a. Tính khối lượng mỗi oxit trong Y.
b. Tính giá trị V.
PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\) (1)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (2)
a) Gọi số mol của Mg là a (mol) \(\Rightarrow n_{Al}=\dfrac{2}{3}a\left(mol\right)\)
\(\Rightarrow24a+27\cdot\dfrac{2}{3}a=6,3\) \(\Rightarrow a=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgO}=0,15\left(mol\right)\\n_{Al_2O_3}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgO}=0,15\cdot40=6\left(g\right)\\m_{Al_2O_3}=0,05\cdot102=5,1\left(g\right)\end{matrix}\right.\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{O_2\left(1\right)}=0,075\left(mol\right)\\n_{O_2\left(2\right)}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{O_2}=0,15\left(mol\right)\) \(\Rightarrow V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)
Đúng 1
Bình luận (0)
Dùng khí hidro dư để khử 30g hỗn hợp gồm 60% sắt (III) oxit và đồng (II)oxit
a)Tính khối lượng mỗi kim loại thu được sau phản ứng.
b)Tính thể tích khí hidro đã phản ứng (đkc).
c)Tính khối lượng HCl cần tác dụng với kẽm có được lượng hidro dùng cho phản ứng trên.
PT: Fe2O3+3H2to→2Fe+3H2O
CuO+H2to→Cu+H2O
a, Ta có: mFe2O3=20.60%=12(g)
⇒nFe2O3=\(\dfrac{12}{160}\)=0,075(mol
mCuO=20−12=8(g
⇒nCuO=\(\dfrac{8}{80}\)=0,1(mol)
Theo pT:
nFe=2nFe2O3=0,15(mol)
nCu=nCuO=0,1(mol)
⇒mFe=0,15.56=8,4(g)
mCu=0,1.64=6,4(g)
b, Theo PT: nH2=3nFe2O3+nCuO=0,325(mol)
⇒VH2=0,325.22,4=7,28(l)
c. Zn+2HCl->ZnCl2+H2
0,65----------0,325
=>m HCl=0,65.36,5=23,725g
Đúng 4
Bình luận (0)
Ủa bạn cái câu a . 20x60% ( 20 ở đâu vậy bạn
Đúng 0
Bình luận (0)
Tính thể tích khí \(H_2\) (đktc) tốt thiểu cần dùng để phản ứng hết với 30,3 gam hỗn hợp M gồm \(Al_2O_3,Zno\) và \(CuO \) (tỉ lệ mol tương ứng là 2 : 2 : 3)
gọi x là số mol \(Al_2O_3\)=> \(n_{ZnO}\)=x và\(n_{CuO}=1,5x\) mol.
=> 102x + 81x + 80.1,5x = 30,3=> x=0,1 mol
\(Al_2O_3+H_2\underrightarrow{to}\) không sảy ra
\(ZnO+H_2\underrightarrow{to}Zn+H_2O\)
0,1->0,1
\(CuO+H_2\underrightarrow{to}Cu+H_2O\)
0,15->0,15
=>\(n_{H2}\) phản ứng =0,1+0,15=0,25 mol
=)\(V_{H2}=0,25.22,4=5,6\) (lít)
#hoctot
Đúng 0
Bình luận (0)
Gọi a là số mol của Al2O3
nAl2O3 = nZnO = 1,5a (mol)
=> 102a+81a+81.1,5a=30,3
giải phương trình trên a=0,1
PTHH: Al2O3 + H2 ---> ko xảy ra pứ
ZnO + H2 --> Zn + H2O
0,1......0,1.....0,1.....0,1
CuO + H2 --> Cu + H2O
0,15....0,15....0,15...0,15
nH2 pứ= 0,1+ 0,15 = 0,25 mol
=> VH2 = 0,25.22,4=5,6 lít
Đúng 0
Bình luận (0)
Bài 1. Hỗn hợp A gồm đồng (II) oxit và sắt (III) oxit, trong đó sắt (III) oxit chiếm 80% khối lượng Tính khối lượng khí H2 cần thiết để khử hoàn toàn 50 gam A.Bài 2. Cho 13 gam kẽm tác dụng hoàn toàn với dung dịch có 0,3 mol axit HCl, thu được m gam ZnCl2 và V lít khí hiđro (đktc). Tính m, V.Bài 3: Cho 6 gam magie tác dụng với dung dịch H2SO4 (loãng). a. Tính thể tích khí hiđro (đktc) thu được, biết hiệu suất phản ứng là 90%.b. Nếu dùng lượng H2 ở trên để khử hoàn toàn 11,2 gam sắt (III) ox...
Đọc tiếp
Bài 1. Hỗn hợp A gồm đồng (II) oxit và sắt (III) oxit, trong đó sắt (III) oxit chiếm 80% khối lượng Tính khối lượng khí H2 cần thiết để khử hoàn toàn 50 gam A.
Bài 2. Cho 13 gam kẽm tác dụng hoàn toàn với dung dịch có 0,3 mol axit HCl, thu được m gam ZnCl2 và V lít khí hiđro (đktc). Tính m, V.
Bài 3: Cho 6 gam magie tác dụng với dung dịch H2SO4 (loãng).
a. Tính thể tích khí hiđro (đktc) thu được, biết hiệu suất phản ứng là 90%.
b. Nếu dùng lượng H2 ở trên để khử hoàn toàn 11,2 gam sắt (III) oxit, thu được tối đa bao nhiêu gam sắt?
Bài 4: Cần dùng m gam khí H2 để khử hết 22,3 gam PbO (hiệu suất phản ứng là 80%). Tính m.
Bài 5: Dùng khí H2 khử 11,2 gam sắt (III) oxit thành Fe. Tính khối lượng Fe thu được, biết hiệu suất phản ứng là 90%.
Bài 6: Cho m gam khí H2 đi từ từ qua 64 gam CuO đun nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 57,6 gam chất rắn A. Tính % khối lượng các chất trong A.
Bài 7. Cho 7,5 gam hỗn hợp X gồm Al và Mg tác dụng hoàn toàn với dung dịch HCl dư.
a. Tính khối lượng muối AlCl3; MgCl2 thu được sau phản ứng. Biết nhôm chiếm 36% khối lượng hỗn hợp X.
Cho 52 gam hỗn hợp X gồm Ni, Cr, Sn (trong đó số mol Cr gấp 2 lần số mol Ni) tác dụng hết với lượng dư dung dịch HC1 loãng, nóng thu được dung dịch Y và 13,44 khí H2 (đktc). Nếu cho 52 gam hỗn hợp X tác dụng hoàn toàn với O2 (dư) để tạo hỗn hợp 3 oxit thì thể tích khí O2 (đktc) phản ứng là A. 11,2 lít. B. 6,72 lít. C. 10,08 lít. D. 7,84 lít.
Đọc tiếp
Cho 52 gam hỗn hợp X gồm Ni, Cr, Sn (trong đó số mol Cr gấp 2 lần số mol Ni) tác dụng hết với lượng dư dung dịch HC1 loãng, nóng thu được dung dịch Y và 13,44 khí H2 (đktc). Nếu cho 52 gam hỗn hợp X tác dụng hoàn toàn với O2 (dư) để tạo hỗn hợp 3 oxit thì thể tích khí O2 (đktc) phản ứng là
A. 11,2 lít.
B. 6,72 lít.
C. 10,08 lít.
D. 7,84 lít.
Đáp án A
Gọi a, b, c lần lượt là số mol của Ni, Cr và Sn
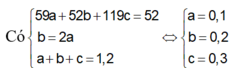
Khi cho hỗn hợp tác dụng với oxi dư thì hỗn hợp sản phẩm thu được gồm NiO, Cr2O3 và SnO2
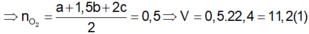
Đúng 0
Bình luận (0)