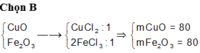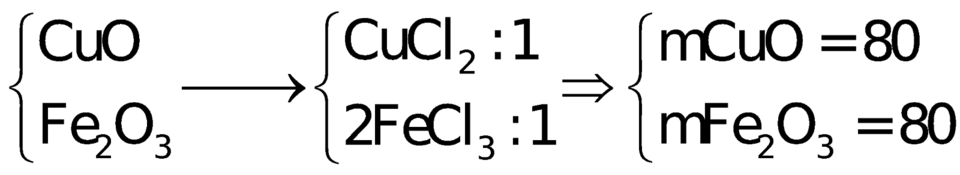tỉ lệ khối lượng của Fe2O3

Những câu hỏi liên quan
hỗn hợp X gồm Fe2O3 và MgO trong đó nguyên tố oxi chiếm 32% theo khối lượng. tỉ lệ số mol của Fe2O3 và MgO tương ứng là
Gọi số mol Fe2O3, MgO là a, b (mol)
nO = 3a + b (mol)
\(\%m_O=\dfrac{48a+16b}{160a+40b}.100\%=32\%\)
=> a = b
=> a : b = 1 : 1
Đúng 0
Bình luận (0)
hỗn hợp X gồm Fe2O3 và MgO trong đó nguyên tố oxi chiếm 32% theo khối lượng. tỉ lệ số mol của Fe2O3 và MgO tương ứng là
Gọi số mol Fe2O3, MgO là a, b (mol)
nO = 3a + b (mol)
%mO = ( 48a + 16b : 160a + 40b) . 100% = 32%
=> a = b
=> a : b = 1 : 1
Vậy tỉ lệ số mol của Fe2O3 và MgO tương ứng là 1 : 1.
Đúng 2
Bình luận (0)
Gọi số mol Fe2O3, MgO là a, b (mol)
nO = 3a + b (mol)
Đúng 0
Bình luận (0)
Gọi số mol Fe2O3, MgO là a, b (mol)
nO = 3a + b (mol)
Đúng 0
Bình luận (0)
28. Hòa tan hoàn toàn 24 gam hh X gồm Fe2O3 và CuO (tỉ lệ mol Fe2O3 và CuO là 1:1) trong dd H2SO4 dư thu
được dd Y có H2SO4 (dư 25% so với lượng đã tham gia phản ứng) và m gam muối.
a) Tính tỉ lệ % khối lượng của các chất trong X và tính m.
b) Tính số gam H2SO4 có trong dung dịch axit ban đầu.
c) Cho dd Y tác dụng với dung dịch BaCl2 dư thu được a gam kết tủa. Tính a
a) \(\left\{{}\begin{matrix}160n_{Fe_2O_3}+80n_{CuO}=24\\n_{Fe_2O_3}=n_{CuO}\end{matrix}\right.\Rightarrow n_{Fe_2O_3}=n_{CuO}=0,1\)
\(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{160.0,1}{24}.100\%=66,67\%\\\%m_{CuO}=\dfrac{80.0,1}{24}.100\%=33,33\%\end{matrix}\right.\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0,1------>0,3-------->0,1
CuO + H2SO4 --> CuSO4 + H2O
0,1-->0,1---------->0,1
nCuSO4 = 0,1 (mol)
nFe2(SO4)3 = 0,1 (mol)
=> m = 0,1.160 + 0,1.400 = 56(g)
b) \(m_{H_2SO_4\left(pthh\right)}=\left(0,3+0,1\right).98=39,2\left(g\right)\)
=> mH2SO4(thực tế) = \(\dfrac{39,2.125}{100}=49\left(g\right)\)
c) \(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
=> nBaSO4 = 0,5 (mol)
=> mBaSO4 = 0,5.233 = 116,5(g)
Đúng 1
Bình luận (0)
A là một loại quặng chứa 40% Fe2O3, B là một loại quặng chứa 50% Fe3O4. Trộn A vs B theo tỉ lệ khối lượng mA : mB = 1 : 2, ta đc quặng C. Tính khối lượng của sắt trong quặng C.
Cho một lượng hỗn hợp gồm CuO, Fe2O3 tan hết trong dung dịch HCl thu được 2 muối có tỉ lệ mol 1: 1. Phần trăm khối lượng CuO và Fe2O3 trong hỗn hợp lần lượt là:
A. 45,38% và 54,62%
B. 50% và 50%
C. 54,62% và 45,28%
D. 33,33% và 66,67%
Đáp án B
CuO + 2HCl → CuCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Giả sử số mol 2 muối CuCl2 và FeCl3 đều là 1 mol
=> nCuO = nCuCl2 = 1 mol ; nFe2O3 = 0,5nFeCl3 = 0,5 mol
=> mhh đầu = 80.1 + 160.0,5 = 160g
=> %mCuO = %mFe2O3 = 50%
Đúng 0
Bình luận (0)
Một loại oxit MxOy có tỉ lệ khối lượng của M và O bằng 1:1. CTHH của chất đó là (giải thích):
A. Fe2O3 B. CuO C. SO2 D. CO2
Xem thêm câu trả lời
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
dùng hidro khử hoàn toàn 40g hỗn hợp gồm Fe2O3 và CuO,trong hỗn hợp tỉ lệ khối lượng Fe2O3 và CuO là 3:2. Tính khối lượng Fe và Cu thu được sau pứ
\(Tacó:m_{Fe_2O_3}:m_{CuO}=3:2\\ m_{Fe_2O_3}+m_{CuO}=40\\ \Rightarrow m_{Fe_2O_3}=24\left(g\right)\Rightarrow n_{Fe_2O_3}=0,15\left(mol\right)\\ \Rightarrow m_{CuO}=16\left(g\right)\Rightarrow n_{CuO}=0,2\left(mol\right)\\ Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\left(1\right)\\ CuO+H_2O-^{t^o}\rightarrow Cu+H_2O\left(2\right)\\TheoPT\left(1\right): n_{Fe}=2n_{Fe_2O_3}=0,3\left(mol\right)\\ \Rightarrow m_{Fe}=16,8\left(g\right)\\TheoPT\left(2\right): n_{Cu}=n_{CuO}=0,2\left(mol\right)\\ \Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
Đúng 3
Bình luận (0)
Cho một lượng hỗn hợp gồm CuO, Fe2O3 tan hết trong dung dịch HCl thu được 2 muối có tỉ lệ mol là 1 : 1. Phần trăm khối lượng CuO và Fe2O3 trong hỗn hợp lần lượt là A. 45,38% và 54,62%. B. 50% và 50%. C. 54,63% và 45,38%. D. 33,33% và 66,67%
Đọc tiếp
Cho một lượng hỗn hợp gồm CuO, Fe2O3 tan hết trong dung dịch HCl thu được 2 muối có tỉ lệ mol là 1 : 1. Phần trăm khối lượng CuO và Fe2O3 trong hỗn hợp lần lượt là
A. 45,38% và 54,62%.
B. 50% và 50%.
C. 54,63% và 45,38%.
D. 33,33% và 66,67%
Cho một lượng hỗn hợp gồm CuO, Fe2O3 tan hết trong dung dịch HCl thu được 2 muối có tỉ lệ mol là 1 : 1. Phần trăm khối lượng CuO và Fe2O3 trong hỗn hợp lần lượt là A. 45,38% và 54,62%. B. 50% và 50%. C. 54,63% và 45,38%. D. 33,33% và 66,67%.
Đọc tiếp
Cho một lượng hỗn hợp gồm CuO, Fe2O3 tan hết trong dung dịch HCl thu được 2 muối có tỉ lệ mol là 1 : 1. Phần trăm khối lượng CuO và Fe2O3 trong hỗn hợp lần lượt là
A. 45,38% và 54,62%.
B. 50% và 50%.
C. 54,63% và 45,38%.
D. 33,33% và 66,67%.
5. Hỗn hợp A chứa Fe ,FeO , Fe3O4, Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4). Số mol của FeO và Fe2O3 có trong 30,72g A lần lượt là?
9. Cho hỗn hợp X có chứa FeO , Fe3O4 và Fe2O3 với tỉ lệ mol tương ứng là 3:1:2. Thành phần % về khối lượng của Fe3O4 có trong 38,44g X là?
20. Cho 33,6 lít hỗn hợp khí B (đktc) gồm SO2 và O2 có tỉ lệ mol tương ứng là 2:3. Tỉ khối hơi của B số vs khí hiđro là?
Đọc tiếp
5. Hỗn hợp A chứa Fe ,FeO , Fe3O4, Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4). Số mol của FeO và Fe2O3 có trong 30,72g A lần lượt là?
9. Cho hỗn hợp X có chứa FeO , Fe3O4 và Fe2O3 với tỉ lệ mol tương ứng là 3:1:2. Thành phần % về khối lượng của Fe3O4 có trong 38,44g X là?
20. Cho 33,6 lít hỗn hợp khí B (đktc) gồm SO2 và O2 có tỉ lệ mol tương ứng là 2:3. Tỉ khối hơi của B số vs khí hiđro là?
5. Hỗn hợp A chứa Fe ,FeO , Fe3O4, Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4). Số mol của FeO và Fe2O3 có trong 30,72g A lần lượt là?
---
Gọi x,2x,3x,4x lần lượt là số mol của Fe,FeO, Fe3O4, Fe2O3 trong 30,72(g) A. (mol) (x>0)
mA= 30,72(g)
<=>mFe+ mFeO+mFe3O4+mFe2O3=30,72
<=> 56x+72.2x+232.3x+160.4x=30,72
<=>1536x=30,72
<=>x=0,02
=>nFeO=2x=0,04(mol)
nFe2O3=4x=0,08(mol)
9. Cho hỗn hợp X có chứa FeO , Fe3O4 và Fe2O3 với tỉ lệ mol tương ứng là 3:1:2. Thành phần % về khối lượng của Fe3O4 có trong 38,44g X là?
Gọi 3x,x,2x lần lượt là số mol FeO, Fe3O4 và Fe2O3 trong 38,44g hhX (x>0)
Ta có: mX= 38,44
<=>mFeO+mFe3O4+mFe2O3=38,44
<=>3x.72+x.232+2x.160=38,44
<=> 768x=38,44
<=> x=961/19200
=> \(\%mFe3O4=\frac{\frac{961}{19200}.232}{38,44}.100\approx30,208\%\)
20. Cho 33,6 lít hỗn hợp khí B (đktc) gồm SO2 và O2 có tỉ lệ mol tương ứng là 2:3. Tỉ khối hơi của B số vs khí hiđro là?
---
nB= 1,5(mol)
nSO2= 2/5 . 1,5=0,6(mol)
nO2= 1,5 - 0,6=0,9(mol)
-> \(\overline{M}_B=\frac{m_B}{n_B}=\frac{m_{SO2}+m_{O2}}{n_B}=\frac{0,6.64+0,9.32}{1,5}=44,8\left(\frac{g}{mol}\right)\\ \rightarrow d_{\frac{B}{H_2}}=\frac{\overline{M}_B}{M_{H_2}}=\frac{44,8}{2}=22,4\)
Đúng 0
Bình luận (0)