Ngâm một Lá Cu trong 300ml Agno3 sau 1 thời gian phản ứng nhấc lá đồng ra khỏi đ cân lại thây tăng lên 2,28g. a, Tính khối lương ag bám vào lá cu
b, xác định nồng độ mol của đ muối đồng nitrat tạo thành sau phản ứng
Bài 1: ngâm một lá đồng 500ml dd AgNO3 đến khi phản ứng hoàn toàn. lấy lá đồng ra làm khô, cân thì thấy khối lượng lá đồng tăng thêm 15,2g. Hãy xác định nồng độ mol của dd bạc nitrat...
Bài 2: cho 78g một kim loại A tác dụng với khí clo dư tạo thành 149g muối . Hãy xác định kim loại A có hóa trị 1.
Bài 3: viết các pthh
a, điều chế Zn từ ZnSO4
b, điều chế MgSO4 từ mỗi chất sau : Mg, MgCl2, MgO, MgCO3
các chất cần thiết coi như đủ
Bài 1:
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\\ \Rightarrow n_{Ag}=2n_{Cu}\\ m_{tăng}=m_{Ag}-m_{Cu}=15,2\left(g\right)\\ \Rightarrow108n_{Ag}-64n_{Cu}=15,2\\ \Rightarrow216n_{Cu}-64n_{Cu}=15,2\\ \Rightarrow n_{Cu}=0,1\left(mol\right)\\ \Rightarrow n_{AgNO_3}=0,2\left(mol\right)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
Bài 2:
\(n_A=\dfrac{78}{M_A}\left(mol\right);n_{ACl}=\dfrac{149}{M_A+35,5}\left(mol\right)\\ PTHH:2A+Cl_2\rightarrow2ACl\\ \Rightarrow n_A=n_{ACl}\Rightarrow\dfrac{78}{M_A}=\dfrac{149}{M_A+35,5}\\ \Rightarrow78M_A+2769=149M_A\\ \Rightarrow71M_A=2769\\ \Rightarrow M_A=39\\ \Rightarrow A\text{ là kali }\left(K\right)\)
Bài 3:
\(a,2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\\ b,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\)
Ngâm 1 lá đồng trong 20 ml dd AgNO3. Phản ứng xong lấy lá đồng ra, rửa nhẹ, làm khô, khối lượng lá đồng tăng thêm 1,52g.
a) Viết PTHH phản ứng xảy ra.
b) Xác định nồng độ mol của dd AgNO3 đã dùng
c) Tính nồng độ phần trăm của dd thu được sau phản ứng, biết khối lượng riêng của dd này là 1,1g/ml và thể tích của dd sau phản ứng thay đổi không đáng kể
\(a,PTHH:Cu+2AgNO_3\to Cu(NO_3)_2+2Ag\\ b,\text{Đặt } n_{AgNO_3}=x(mol)\\ \Rightarrow n_{Ag}=x;n_{Cu}=\dfrac{1}{2}x\\ \Rightarrow 108x-32x=1,52\\ \Rightarrow x=0,02(mol)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,02}{ 0,02}=1M\)
\(c,V_{Cu(NO_3)_2}=20(ml)\\ \Rightarrow m_{dd_{Cu(NO_3)_2}}=20.1,1=22(g)\\ n_{Cu(NO_3)_2}=0,01(mol)\\ \Rightarrow m_{Cu(NO_3)_2}=0,01.188=1,88(g)\\ \Rightarrow C\%_{Cu(NO_3)_2}=\dfrac{1,88}{22}.100\%=8,55\%\)
Ngâm một lá đồng trong 20ml dung dịch bạc nitrat cho đến khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì khối lượng lá đồng tăng thêm 1,52g. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ bạc giải phóng ra bám hết vào lá đồng).
A. 0,75 M
B. 0,5 M
C. 1 M
D. 0,25 M
Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
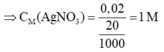
⇒ Chọn C.
bài 1: Ngâm một lá kẽm vào dung dịch CuSO4 . Sau một thời gian lấy lá kẽm ra thấy Khối Lượng Dung Dịch tăng 0,2g.Tính khối luuwojng kẽm đã tham gia phản ứng
bài 2: Ngâm một bản sắt trong dung dịch CuSO4 . Sau một thời gian lấy ra thấy khối luuwojng abrn sắt tăng thêm 1g.
a) Tính khối lượng muối sắt tạo thành
b) Tính khối lượng Cu bám lên bản sắt
bài 3: Ngâm một lá đồng trong 30ml dd AgNO3 ,Khối lượng lá đồng tăng thêm 2,28g.Xác định khối lượng mol của AgNO3
hơi nhiều một tí,các bạn cố gắng giúp mình nha !!! Thank you very much!!!!
bài 3
Cu +2 AgNO3 -> Cu(NO3)2 + 2Ag
x...............2x.................................2x (mol)
theo bài ta có : 216x-64x=152x=2,28
==> x=0,015 (mol)=> n AgNO3=2x=0,03
==> CMAgNO3 =\(\dfrac{0,03}{\dfrac{30}{1000}}=1\left(M\right)\)
vậy............
bài 1
Zn + CuSO4 -> ZnSO4 + Cu
x x x (mol)
theo bài có 161x-160x=0,2==> x=0,2 = nZn
==> mZn tham gia = 0,2.65=13 (g)
vậy.........
bài 2
a,Fe + CuSO4-> FeSO4 + Cu
x ...............x...........x............x (mol)
theo bài có : 64x-56x=1==> x=0,125 = nFeSO4
==> mFeSO4= 0,125.152=19 (g)
b, nCu=x=0,125 (mol)
==> m Cu = 0,125.64=8 (g)
vậy
Ngâm một lá sắt trong 100ml dung dịch đồng nitrat cho đến khi sắt không thể tan thêm được nữa. Lấy lá sắt ra, rửa nhẹ, làm khô và cân thì khối lượng lá sắt tăng thêm 1,6g. Hãy xác định nồng độ mol của dung dịch đồng nitrat đã dùng (giả thiết toàn bộ đồng giải phóng ra bám hết vào lá sắt).
A. 1 M
B. 0,5 M
C. 1,5 M
D. 2 M
1.cho lá sắt có khối lượng 50g vào dung dịch CuSO4. Sau một thời gian nhấc lá sắt ra thì thấy khối lượng lá sắt là 51(g) . Tính số mol muối sắt tạo thành sau phản ứng. Biết Cu đều bám vào mặt lá sắt
Ngâm một lá đồng vào 340 gam dung dịch AgNO3 10%. Sau khi tất cả bạc bị đẩy ra khỏi dung dịch AgNO3 và bám hết vào lá đồng, thì khối lượng lá đồng tăng lên 38%. Xác định khối lượng lá đồng ban đầu.
Ngâm một lá đồng vào 340 gam dung dịch AgNO3 10%. Sau khi tất cả bạc bị đẩy ra khỏi dung dịch AgNO3 và bám hết vào lá đồng, thì khối lượng lá đồng tăng lên 38%. Xác định khối lượng lá đồng ban đầu.
Nhúng 1 lá nhôm vào dd 200ml CuSO4 . Sau một thời gian lấy lá nhôm ra khỏi dd làm khô rồi cân thì thấy khối lượng lá nhôm tăng 1,38g
a) Tính khối lượng đồng tạo thành
b) Tính nồng độ mol CuSO4 đã phản ứng
\(a,\) Đặt \(n_{CuSO_4}=x(mol)\)
\(PTHH:2Al+3CuSO_4\to Al_2(SO_4)_3+3Cu\\ \dfrac{2}{3}x.....x......\dfrac{1}{3}x.....x(mol)\\ \Rightarrow \Delta m_{Al\uparrow}=m_{Cu}-m_{Al}=64x-\dfrac{2}{3}.27x=1,38\\ \Rightarrow x=0,03\\ \Rightarrow m_{Cu}=0,03.64=1,92(g)\\ b,n_{CuSO_4}=0,03(mol)\\ \Rightarrow C_{M_{CuSO_4}}=\dfrac{0,03}{0,2}=0,15M\)
Gọi khối lượng Al ban đầu là a gam
khối lượng Al pư là x gam
PTHH: 2Al+3CuSO4→Al2(SO4)3+3Cu
a, vì khối lượng của nhôm sau pư tăng 1,38g, nên ta có PT:
(a-x) + 192x/54 = a + 1,38
⇒ x= 0,54
⇒ a= 0,54 + 1,38 = 1,92g
b, nAl=0,54/27 = 0,02 mol
theo PTHH có nCuSO4=2/3 .nAl = 0,03 mol
⇒CMCuSO4=0,03/0,2=0,15M
Chúc bạn học tốt nha!