Bài 3: Khi phân tích một mẫu quặng bôxit (chứa Al,O,), người ta thấy có 5,4 g nhôm. Tính xem trong mẫu quặng đó có bao nhiêu gam nhôm oxit Al,O, ứng với lượng nhôm trên

Những câu hỏi liên quan
bài 1: người ta dung quặng nhôm bôxit để sản xuất nhôm theo sơ đồ sau: 2Al2O3 4Al + 3O2 hàm lượng Al2O3 trong quặng bôxit là 40%. để có 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng. biết hiệu suất phản ứng của cả quá trình là 90%. bài 2: có thể bao nhiêu kg nhôm từ 1 tấn quặng bôxit chứa 95% nhôm, biết hiệu suấ phản ứng là 98%
Đọc tiếp
bài 1: người ta dung quặng nhôm bôxit để sản xuất nhôm theo sơ đồ sau:
2Al2O3 = 4Al + 3O2
hàm lượng Al2O3 trong quặng bôxit là 40%. để có 4 tấn nhôm nguyên chất cần bao nhiêu tấn quặng. biết hiệu suất phản ứng của cả quá trình là 90%.
bài 2: có thể bao nhiêu kg nhôm từ 1 tấn quặng bôxit chứa 95% nhôm, biết hiệu suấ phản ứng là 98%
2Al2O3--->4Al+3O2
ta có
cứ 204 tấn Al2O3_____108 tấn Al
--> 4 tấn AL cần 7,56 tấn Al2O3
vì hàm lượng quặng chỉ chứa 40% nên lượng quặng ban đầu là 18,9 tấn
H=90%
-->khối lượng quặng cần là 21 tấn
Đúng 0
Bình luận (3)
Nhôm oxit ( Al2 O3) là thành phần chính của quặng bôxit. Điện phân nóng chảy 21,2 g quặng bôxit thu được 10,8 g kim loại nhôm và 96 g khí oxi. Tính phần trăm khối lượng của nhôm oxit ( Al2 O3) chứ trong quặng bôxit ?
Theo ĐLBTKL: mAl2O3 = mAl + mO2
=> mAl2O3 = 10,8 + 9,6 = 20,4 (g)
=> \(\%Al_2O_3=\dfrac{20,4}{21,2}.100\%=96,226\%\)
Đúng 1
Bình luận (0)
Trong một loại quặng boxit có 50% nhôm oxit. Nhôm luyện từ oxit đó còn chứa 1,5% tạp chất. Tính lượng nhôm thu được khi luyện 0,5 tấn quặng boxit trên. Hiệu suất phản ứng 100%.
Lượng nhôm oxit có trong 0,5 tấn quặng là : 0,5x50/100 = 0,25 tấn = 250kg
Phương trình hoá học điều chế Al :
2 Al 2 O 3 → 4Al + 3 O 2
Khối lượng Al nguyên chất thu được từ 250 kg quặng :
x = 250x4x27/(2x102) = 132,4(kg)
Khối lượng Al lẫn tạp chất: 132,4 x 101,5% = 134,386 (kg).
Đúng 0
Bình luận (0)
Hơi lệch một chút, cái này liên quan đến hóa ạ :( mình sắp ktra 1 tiết rồi mong mn thông cảmQuặng boxit là có thành phần chủ yếu Al2O3. Để điều chế nhôm người ta liền phân 150g quặng boxit thu được 54g Nhôm Al và 48gam khí Oxi (O2) phản ứng xảy ra theo sơ đồ sau: Al2O3 - Al +O2a) Viết công thức về khối lượng của phản ứng và dựa vào sơ đồ trên viết PTHHb)Tính khối lượng Al2O3 đã phản ứng c) Tính tỉ lệ% của khối lượng Al2O3 chứa trong quặng boxit đó ??
Đọc tiếp
Hơi lệch một chút, cái này liên quan đến hóa ạ :( mình sắp ktra 1 tiết rồi mong mn thông cảm
Quặng boxit là có thành phần chủ yếu Al2O3. Để điều chế nhôm người ta liền phân 150g quặng boxit thu được 54g Nhôm Al và 48gam khí Oxi (O2) phản ứng xảy ra theo sơ đồ sau: Al2O3 -> Al +O2
a) Viết công thức về khối lượng của phản ứng và dựa vào sơ đồ trên viết PTHH
b)Tính khối lượng Al2O3 đã phản ứng
c) Tính tỉ lệ% của khối lượng Al2O3 chứa trong quặng boxit đó ??
Người ta điều chế Al từ một loại quặng có chứa 80% Al2 O3 . Biết hiệu suất của phản ứng đạt 75%. Khối lượng quặng để điều chế ra 5,4 tấn nhôm là
\(PTHH:2Al_2O_3\rightarrow4Al+3O_2\)
Cứ \(204\)tấn\(Al_2O_3\)tham gia pứ thì thu được \(108\) tấn \(Al\)
\(\Rightarrow\)Để thu được \(5,4\) tấn \(Al\) cần \(10,2\)tấn \(Al_2O_3\)
Vì: \(H=75\%\Rightarrow m_{Al_2O_3}=\frac{10,2.100}{75}=13,6\)(Tấn)
Mà quặng chỉ chứa\(80\%Al_2O_3\)
\(\Rightarrow\) Khối lượng quặng để điều chế\(5,4\)tấn \(Al\) là:
\(m_{quặng}=\frac{13,6.100}{80}=17\)(Tấn)
Vậy ......
Bài 2. Nhôm oxit (Al2O3) là thành phần chính của quặng boxit, còn lại là tạp chất . điện phân nóng chảy 127,5 gam quặng boxit theo phản ứng :Al2O3 Al + O2.Thu được 54 gam Al (nhôm) và 48 gam O2 (khí oxi) a.Tính khối lượng Al2O3 (Nhôm oxit) đã phản ứng? b.Tính tỉ lệ phần trăm về khối lượng của Nhôm oxit có trong quặng boxit?
Đọc tiếp
Bài 2. Nhôm oxit (Al2O3) là thành phần chính của quặng boxit, còn lại là tạp chất . điện phân nóng chảy 127,5 gam quặng boxit theo phản ứng :
Al2O3 Al + O2.
Thu được 54 gam Al (nhôm) và 48 gam O2 (khí oxi)
a.Tính khối lượng Al2O3 (Nhôm oxit) đã phản ứng?
b.Tính tỉ lệ phần trăm về khối lượng của Nhôm oxit có trong quặng boxit?
a/ nAl= 54/27= 2(mol)
nO2=48/32=1,5(mol)
PTHH: 2 Al2O3 -to-> 4 Al +3 O2
Ta có: 2/4 = 1,5/3
=> P.ứ hết
=> nAl2O3= 1/2. nAl=1/2. 2=1(mol)
=> mAl2O3=1.102=102(g)
b) %mAl2O3= (102/127,5).100= 80%
Đúng 2
Bình luận (0)
Ngta dùng quặng Bỗít để sản xuất nhôm .Hàm lượng Al2O3 trong quặng là 40%.Để có đc 5,4 tấn Al nguyên chất thì cần bao nhiêu?
\(m_{bôxit}=\dfrac{5,4.100}{40}=13,5\left(tấn\right)\)
Đúng 0
Bình luận (0)
Hơi lệch một chút, cái này liên quan đến hóa ạ :( mình sắp ktra 1 tiết rồi mong mn thông cảmQuặng boxit là có thành phần chủ yếu Al2O3. Để điều chế nhôm người ta liền phân 150g quặng boxit thu được 54g Nhôm Al và 48gam khí Oxi (O2) phản ứng xảy ra theo sơ đồ sau: Al2O3 - Al +O2a) Viết công thức về khối lượng của phản ứng và dựa vào sơ đồ trên viết PTHHb)Tính khối lượng Al2O3 đã phản ứngc) Tính tỉ lệ% của khối lượng Al2O3 chứa trong quặng boxit đó ??
Đọc tiếp
Hơi lệch một chút, cái này liên quan đến hóa ạ :( mình sắp ktra 1 tiết rồi mong mn thông cảm
Quặng boxit là có thành phần chủ yếu Al2O3. Để điều chế nhôm người ta liền phân 150g quặng boxit thu được 54g Nhôm Al và 48gam khí Oxi (O2) phản ứng xảy ra theo sơ đồ sau: Al2O3 -> Al +O2
a) Viết công thức về khối lượng của phản ứng và dựa vào sơ đồ trên viết PTHH
b)Tính khối lượng Al2O3 đã phản ứng
c) Tính tỉ lệ% của khối lượng Al2O3 chứa trong quặng boxit đó ??
chị vào chỗ này là sẽ có đáp án đấy:Câu hỏi của Đào Minh Anh - Hóa học lớp 8
Đúng 0
Bình luận (0)
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một lạo quặng sắt (thành phần chính là
F
e
2
O
3
). Khi phân tích mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit
F
e
2
O
3
ứng với hàm lượng sắt nói trên là: A. 6g. B. 8(g). C.4g. D.3g. Hãy chọn đáp số đúng...
Đọc tiếp
Khu mỏ sắt ở Trại Cau (Thái Nguyên) có một lạo quặng sắt (thành phần chính là F e 2 O 3 ). Khi phân tích mẫu quặng này, người ta nhận thấy có 2,8g sắt. Trong mẫu quặng trên, khối lượng sắt (III) oxit F e 2 O 3 ứng với hàm lượng sắt nói trên là:
A. 6g. B. 8(g). C.4g. D.3g.
Hãy chọn đáp số đúng.
Phương trình hóa học:
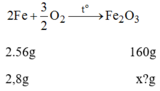
Khối lượng F e 2 O 3 ứng với lượng sắt trên là:
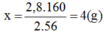
→ Chọn C.
Đúng 0
Bình luận (0)


















