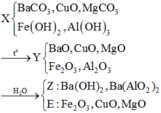Nung 6,02g hỗn hợp X gồm Zn(oh)2 và fe(oh)3 đến khối lượng không đổi, thấy khối lượng hỗn hợp giảm 1,17g và thu được chất rắn Y a. Xác định thành phần % khối lượng mỗi Hidroxit có trong hỗn hợp. b. Cần mấy ml dd HCl 14,6% ( D=1,15g/ml) vừa đủ để hoà tan hết lượng Y trên

Những câu hỏi liên quan
Nung 6,02g hỗn hợp X gồm Zn(oh)2 và fe(oh)3 đến khối lượng không đổi, thấy khối lượng hỗn hợp giảm 1,17g và thu được chất rắn Y a. Xác định thành phần % khối lượng mỗi Hidroxit có trong hỗn hợp. b. Cần mấy ml dd HCl 14,6% ( D=1,15g/ml) vừa đủ để hoà tan hết lượng Y trên
Nung 204g hỗn hợp gồm Mg(OH)2 và Fe(OH)3 đến khối lượng không đổi thấy khối lượng chất rắn giảm đi 54g.Tính
a) khối lượng mỗi oxit thu được. Biết tỉ lệ mol của chúng trong hỗn hợp sản phẩm chất rắn là 1 : 1
b) Thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp.
Hai hidroxit đều k tan nên khi phân hủy cho ra oxit và nước
Mg(OH)2 -------> MgO+ H2O
-----------------------x---------x
2Fe(OH)3 -------> Fe2O3 + 3H2O
------------------------y------------3y
Gọi x, y lần lượt là số mol của MgO và Fe2O3
Theo đề bài ta có hệ phương trình: x=y (x-y=0) và 18x + 54y=54<=> x=0,75, y=0,75
=>mMgO=0,75.40=30g, mFe2O3=0,75.170=127,5
%mMg(OH)2=0,75.58.100/204=21,32% => %mFe(OH)3=100-21,32=78,68%
Đúng 1
Bình luận (0)
nung 16,9gam hỗn hợp Mg(OH)2 và Fe (OH)3 đến khối lượng ko đổi thu đc 12,4 gam chất rắn. tính thành phần % theo khối lượng mỗi chất trong hỗn hợp ban đầu
\(n_{Mg\left(OH\right)_2}=a\left(mol\right)\)
\(n_{Fe\left(OH\right)_3}=b\left(mol\right)\)
\(m_{hh}=58a+107b=16.9\left(g\right)\left(1\right)\)
\(Mg\left(OH\right)_2\underrightarrow{^{^{t^0}}}MgO+H_2O\)
\(a.............a\)
\(2Fe\left(OH\right)_3\underrightarrow{^{^{t^0}}}Fe_2O_3+3H_2O\)
\(b.............\dfrac{b}{2}\)
\(m_{Cr}=40a+160\cdot\dfrac{b}{2}=12.4\left(g\right)\left(1\right)\)
\(\left(1\right),\left(2\right):a=0.07,b=0.12\)
\(\%m_{Mg\left(OH\right)_2}=\dfrac{0.07\cdot40}{16.9}\cdot100\%=16.57\%\)
\(\%m_{Fe\left(OH\right)_3}=83.43\%\)
Đúng 3
Bình luận (0)
Hỗn hợp chất rắn X gồm: BaCO3, Fe(OH)2, Al(OH)3, CuO và MgCO3. Nung X trong không khí đến khối lượng không đổi, thu được hỗn hợp rắn Y. Cho Y vào nước dư, thu được dung dịch Z chứa 2 chất tan và phần không tan E. Các chất trong E gồm A. Fe2O3, Cu, MgO B. Fe2O3, CuO, MgO C. FeO, CuO, MgO D. Fe2O3, CuO, MgO, Al2O3
Đọc tiếp
Hỗn hợp chất rắn X gồm: BaCO3, Fe(OH)2, Al(OH)3, CuO và MgCO3. Nung X trong không khí đến khối lượng không đổi, thu được hỗn hợp rắn Y. Cho Y vào nước dư, thu được dung dịch Z chứa 2 chất tan và phần không tan E. Các chất trong E gồm
A. Fe2O3, Cu, MgO
B. Fe2O3, CuO, MgO
C. FeO, CuO, MgO
D. Fe2O3, CuO, MgO, Al2O3
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là
A. Mg và FeO.
B. MgO và Fe2O3.
C. MgO và FeO.
D. Mg và Fe.
Đáp án B
2Fe(OH)2 + ½ O2 → t 0 Fe2O3 + 2H2O
Vậy chất rắn gồm: MgO, Fe2O3
Đúng 0
Bình luận (0)
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là A. Mg và FeO. B. MgO và FeO. C. MgO và Fe2O3. D. Mg và Fe.
Đọc tiếp
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là
A. Mg và FeO.
B. MgO và FeO.
C. MgO và Fe2O3.
D. Mg và Fe.
Đáp án C
Mg(OH)2 → t 0 MgO + H2O
2Fe(OH)2 + ½ O2 → t 0 Fe2O3 + 2H2O
Vậy chất rắn gồm: MgO, Fe2O3
Đúng 0
Bình luận (0)
Nung nóng 1,32a gam hỗn hợp Mg(OH)2, Fe(OH)2 trong không khí đến khối lượng khôn đổi thu được chất rắn Y có khối lượng bằng a gam. Viết PTHH, tính % khối lượng mỗi chất trong hỗn hợp đầu?
PTHH:
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
x....................x
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
y...................................0,5y
Gọi số mol Mg(OH)2, Fe(OH)2 lần lượt là x, y (mol)
Theo đề ra, ta có:
\(\begin{cases}58x+90y=1,32a\\40x+80y=a\end{cases}\)
\(\Rightarrow\begin{cases}x=0,015a\\y=0,005a\end{cases}\)
=> mMgO = 0,015a x 40 = 0,6a (gam)
=> %mMgO = \(\frac{0,6a}{a}.100\%=60\%\)
=> %mFe2O3 = 100% - 60% = 40%
Đúng 0
Bình luận (0)
PTHH: Mg(OH)2 → MgO + H2O
Fe(OH)2 → FeO + H2O
Gọi số mol của Mg(OH)2 là x , số mol của Fe(OH)2 là y => Số mol của MgO là a , số mol của FeO là b
Ta có hệ phương trình sau:
58x + 90y = 1,32a (1)40x + 72y = a (2)Nhân phương trình (2) với 1,32 ta có :
52,8x + 95,04y = 1,32a (3)
Vì phương trình (3) và phương trình (1) đều bằng 1,32a
=> 58x + 90y = 52,8x + 95,04y
=> x = 0,97y
%MgO trong hỗn hợp oxit là:
40x/40x+72y.100%=40.0,97y/40.0,97y+72y.100%=35,02%.40x/40x+72y.100%=40.0,97y/40.0,97y+72y.100%=35,02%
%FeO trong hỗn hợp oxit là:
100% - 35,02% = 64,98%
Đúng 0
Bình luận (0)
1 hỗn hợp gồm BaSO4 và Fe(OH)3 nặng 100g. nhiệt phân đến khối lượng không đổi thấy hỗn hợp giảm 3,6g . tính thành phần phần trăm khối lượng các chất rắn ban đầu
Để 26,88 gam phôi Fe ngoài không khí một thời gian, thu được hỗn hợp rắn X gồm Fe và các oxit. Hòa tan hết X trong 288 gam dung dịch HNO3 31,5%, thu được dung dịch Y chứa các muối và hỗn hợp khí Z gồm 2 khí, trong đó oxi chiếm 61,11% về khối lượng. Cô cạn Y, rồi nung đến khối lượng không đổi thấy khối lượng chất rắn giảm 67,84 gam. Xác định nồng độ % Fe(NO3)3 trong Y? A. 28,14% B. 26,36% C. 24,47% D. 25,19%
Đọc tiếp
Để 26,88 gam phôi Fe ngoài không khí một thời gian, thu được hỗn hợp rắn X gồm Fe và các oxit. Hòa tan hết X trong 288 gam dung dịch HNO3 31,5%, thu được dung dịch Y chứa các muối và hỗn hợp khí Z gồm 2 khí, trong đó oxi chiếm 61,11% về khối lượng. Cô cạn Y, rồi nung đến khối lượng không đổi thấy khối lượng chất rắn giảm 67,84 gam. Xác định nồng độ % Fe(NO3)3 trong Y?
A. 28,14%
B. 26,36%
C. 24,47%
D. 25,19%