Chứng minh bán kính của nguyên tử Al lớn hơn bán kính của ion \(O^{2-}\)

Những câu hỏi liên quan
Khác với nguyên tử O, ion oxit O 2 - có
A. bán kính ion nhỏ hơn và ít electron hơn.
B. bán kính ion nhỏ hơn và nhiều electron hơn.
C. bán kính ion lớn hơn và ít electron hơn.
D. bán kính ion lớn hơn và nhiéu electron hơn.
Trong các nguyên tử và ion : Ne, Na, Mg, Al, Al3+, Mg2+, Na+ , O2–, F–, hạt có bán kính lớn nhất và hạt có bán kính nhỏ nhất là A. Al3+, O2– B. Na, Al3+ C. Na, Ne D. O2–, Na+
Đọc tiếp
Trong các nguyên tử và ion : Ne, Na, Mg, Al, Al3+, Mg2+, Na+ , O2–, F–, hạt có bán kính lớn nhất và hạt có bán kính nhỏ nhất là
A. Al3+, O2–
B. Na, Al3+
C. Na, Ne
D. O2–, Na+
Đáp án : B
Các nguyên tử ion có số lớp e nhiều hơn thì bán kính lớn hơn
Các nguyên tử ion có cùng số lớp e
cùng số e thì nguyên tử ion nào có điện tích âm sẽ có bán kính lớn hơn và ngược lại
Đúng 0
Bình luận (0)
a) Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b) Vì sao cả Na2O và MgO đều là chất rắn ở nhiệt độ thường?
c) Vì sao nhiệt độ nóng chảy của MgO (2 852oC) cao hơn rất nhiều so với Na2O (1 132oC)?
a)
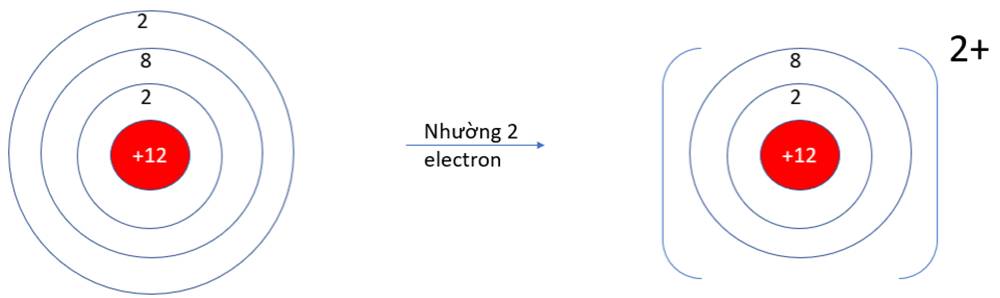
- Ở dạng nguyên tử, Na và Mg đều có 3 lớp electron. Ở dạng ion Na+, Mg2+ chỉ có 2 lớp electron
=> Bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b, Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion nên ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion nên ở điều kiện thường MgO tồn tại ở thể rắn.
c, Tá có:
+ Bán kính ion Na+ < bán kính ion Mg2+.
+ Điện tích ion Mg2+ < điện tích ion Na+.
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.
Đúng 0
Bình luận (0)
Trong các nguyên tố sau, nguyên tử của nguyên tố có bán kính lớn nhất là
A. O B. F
C. N D. Al.
Cho các phát biểu sau:(a) Trong không khí ẩm, bề mặt của gang bị ăn mòn điện hóa.(b) Ở điều kiện thường, tất cả các kim loại đều tồn tại ở trạng thái rắn.(c) Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử.(d) Bán kính của nguyên tử kim loại luôn lớn hơn bán kính của nguyên tử phi kim.Số phát biểu đúng là A. 4. B. 2. C. 3. D. 1.
Đọc tiếp
Cho các phát biểu sau:
(a) Trong không khí ẩm, bề mặt của gang bị ăn mòn điện hóa.
(b) Ở điều kiện thường, tất cả các kim loại đều tồn tại ở trạng thái rắn.
(c) Nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử.
(d) Bán kính của nguyên tử kim loại luôn lớn hơn bán kính của nguyên tử phi kim.
Số phát biểu đúng là
A. 4.
B. 2.
C. 3.
D. 1.
Đáp án B
(a) Đúng vì hình thành cặp điện cực Fe - C nên bề mặt gang bị ăn mòn điện hóa.
(b) Sai, Hg là kim loại duy nhất tồn tại ở trạng thái lỏng ở điều kiện thường.
(c) Đúng.
(d) Sai, còn phụ thuộc vào điện tích hạt nhân, số lớp e...
→ Có 2 phát biểu đúng.
Đúng 0
Bình luận (0)
Trong các nguyên tố sau, nguyên tử của nguyên tố có bán kính lớn nhất là
A. Al. B. P C. S . D. K.
Electron trong nguyên tử hidro chuyển động xung quanh hạt nhân bên trong một khối cầu có bán kính lớn hơn bán kính hạt nhân là 10000 lần. Nếu ta phóng đại hạt nhân lên thành một quả bóng có đường kính 6cm thì bán kính khối cầu tức là bán kính nguyên tử sẽ là bao nhiêu mét?
Đáp án
Bán kính của hạt nhân bằng 6/2 = 3 (cm). Bán kính của nguyên tử là : 3 x 10000 = 30000 (cm) = 300 (m).
Đúng 0
Bình luận (0)
Câu 92. Hai nguyên tố X và Y đứng kê tiếp nhau ở cùng một chu kỳ trong bảng tần hoàn (bán kính nguyên tỉ X lớn hơn bán kính nguyên tử Y), có tông số hạt mang điện là 58. a/ Viết cáấu hình electron của nguyên tử X, Y. b/ Xác định vị trí của X, Y trong bảng tuân hoàn và gọi tên nguyên tổ X, Y.
a) Trong cùng 1 chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử của nguyên tố giảm dần \(\Rightarrow Z_X< X_Y\).
-Vì 2 nguyên tố X,Y đứng kế nhau trong bảng tuần hoàn nên \(Z_X+1=Z_Y\left(1\right)\)
-Vì 2 nguyên tố X,Y có tổng số hạt mang điện là 58 nên \(2\left(Z_X+Z_Y\right)=58\left(2\right)\)
Từ (1), (2) ta có: \(\left\{{}\begin{matrix}Z_X=14\\Z_Y=15\end{matrix}\right.\)
Cấu hình electron của nguyên tử X,Y:
\(X:1s^22s^22p^63s^23p^2\) ; \(Y:1s^22s^22p^63s^23p^3\)
b) Vị trí của X,Y trong bảng tuần hoàn:
X: ô 14, nhóm IVA, chu kì 3. X là Si.
Y: ô 15, nhóm VA, chu kì 3. Y là P.
Đúng 1
Bình luận (0)
2. Hai hình tròn có cùng tâm O như hình bên. Hình tròn bé có bán kính 5m. Chu vi của hình tròn lớn là 40,82m. Hỏi bán kính hình tròn lớn dài hơn bán kính hình tròn bé bao nhiêu mét ?
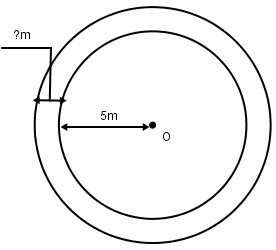
Hình tròn lớn có bán kính là:
40,82 : 2 : 3,14 = 6,5(m)
Bán kính hình tròn lớn hơn bán kính hình tròn bé số mét là:
6,5 - 5 = 1,5(m)
Đáp số : 1,5m
Đúng 2
Bình luận (0)
Theo mẫu nguyên tử Bo, bán kính quỹ đạo dừng K của electron trong nguyên tử hiđro là
r
0
Khi electron chuyển động trên quỹ đạo O thì bán kính là: A.
4
r
0
B.
5
r
0
C.
16
r
0
D.
25
r
0
Đọc tiếp
Theo mẫu nguyên tử Bo, bán kính quỹ đạo dừng K của electron trong nguyên tử hiđro là r 0 Khi electron chuyển động trên quỹ đạo O thì bán kính là:
A. 4 r 0
B. 5 r 0
C. 16 r 0
D. 25 r 0
Chọn D.
Khi electron chuyển động trên quỹ đạo O thì bán kính r = n 2 r = 0 25 r 0 .
Đúng 0
Bình luận (0)













