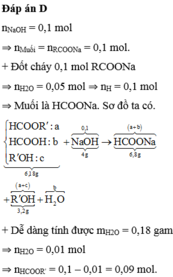
một dd X chứa 6,3g axit A, 9,8 gam axit B, 3,65 gam axit C. Trung hòa hoàn toàn dd X cần vừa đủ 400ml dd KOH 1M. Tính khối lượng khối lượng muối khan thu đc khi cô cạn dd sau phản ứng

Những câu hỏi liên quan
Hòa tan hoàn toàn hỗn hợp na2co3 và k2co3 bằng 400ml dd hcl 1,5M thu được 5,6l khí co2 (đktc) và một dd A. trung hòa axit còn dư tronh dd A bằng lượng dd naoh vừa đủ thu được dd B, rồi cô cạn dd B sau pứ được 39,9g hỗn hợp muối khan. tính thành phần % về khối lượng các muối cacbonat trong hỗn hợp đầu.
Hòa tan hoàn toàn hỗn hợp Na2CO3, K2CO3 bằng 400ml dd HCl 1,5M thu được 5,6l khí CO2 (đktc) và một dd A. trung hòa axit còn dư tronh dd A bằng lượng dd NaOH vừa đủ thu được dd B, rồi cô cạn dd B sau pứ được 39,9g hỗn hợp muối khan. Tính thành phần % về khối lượng các muối cacbonat trong hỗn hợp đầu
Giúp mình với, cảm ơn rất nhiều
Ta có: \(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{HCl}=0,4.1,5=0,6\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{Na_2CO_3}=x\left(mol\right)\\n_{K_2CO_3}=y\left(mol\right)\end{matrix}\right.\)
PT: \(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O+CO_2\)
\(K_2CO_3+2HCl\rightarrow2KCl+H_2O+CO_2\)
\(HCl_{dư}+NaOH\rightarrow NaCl+H_2O\)
Theo PT: \(n_{CO_2}=n_{Na_2CO_3}+n_{K_2CO_3}=x+y\left(mol\right)\) ⇒ x + y = 0,25 (1)
\(n_{HCl\left(pư\right)}=2x+2y\left(mol\right)\) \(\Rightarrow n_{HCl\left(dư\right)}=0,6-2x-2y\left(mol\right)\)
Có: \(\left\{{}\begin{matrix}n_{NaCl}=2n_{Na_2CO_3}+n_{HCl\left(dư\right)}=0,6-2y\left(mol\right)\\n_{KCl}=2n_{K_2CO_3}=2y\left(mol\right)\end{matrix}\right.\)
⇒ 58,5(0,6 - 2y) + 74,5.2y = 39,9 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{0,1.106}{0,1.106+0,15.138}.100\%\approx33,9\%\\\%m_{K_2CO_3}\approx66,1\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Hỗn hợp X gồm este, một axit cacboxylic và một ancol (đều no, đơn chức, mạch hở). Thủy phân hoàn toàn 6,18 gam X bằng lượng vừa đủ dd chứa 0,1 mol NaOH thu được 3,2 gam một ancol. Cô cạn dd sau thủy phân rồi đem lượng muối khan thu được đốt cháy hoàn toàn thu được 0,05 mol H2O. Phần trăm khối lượng của este có trong X là A. 23,34%. B. 56,34%. C. 7,44%. D. 87,38%.
Đọc tiếp
Hỗn hợp X gồm este, một axit cacboxylic và một ancol (đều no, đơn chức, mạch hở). Thủy phân hoàn toàn 6,18 gam X bằng lượng vừa đủ dd chứa 0,1 mol NaOH thu được 3,2 gam một ancol. Cô cạn dd sau thủy phân rồi đem lượng muối khan thu được đốt cháy hoàn toàn thu được 0,05 mol H2O. Phần trăm khối lượng của este có trong X là
A. 23,34%.
B. 56,34%.
C. 7,44%.
D. 87,38%.
Hỗn hợp X gồm este, một axit cacboxylic và một ancol (đều no, đơn chức, mạch hở). Thủy phân hoàn toàn 6,18 gam X bằng lượng vừa đủ dd chứa 0,1 mol NaOH thu được 3,2 gam một ancol. Cô cạn dd sau thủy phân rồi đem lượng muối khan thu được đốt cháy hoàn toàn thu được 0,05 mol H2O. Phần trăm khối lượng của este có trong X là A. 23,34%. B. 56,34%. C. 7,44%. D. 87,38%.
Đọc tiếp
Hỗn hợp X gồm este, một axit cacboxylic và một ancol (đều no, đơn chức, mạch hở). Thủy phân hoàn toàn 6,18 gam X bằng lượng vừa đủ dd chứa 0,1 mol NaOH thu được 3,2 gam một ancol. Cô cạn dd sau thủy phân rồi đem lượng muối khan thu được đốt cháy hoàn toàn thu được 0,05 mol H2O. Phần trăm khối lượng của este có trong X là
A. 23,34%.
B. 56,34%.
C. 7,44%.
D. 87,38%.
Đáp án D
nNaOH = 0,1 mol
⇒ nMuối = nRCOONa = 0,1 mol.
+ Đốt cháy 0,1 mol RCOONa
⇒ nH2O = 0,05 mol ⇒ nH = 0,1 mol
⇒ Muối là HCOONa.
Sơ đồ ta có.
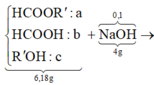
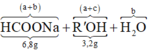
+ Dễ dàng tính được mH2O = 0,18 gam
⇒ nH2O = 0,01 mol
⇒ nHCOOR' = 0,1 – 0,01 = 0,09 mol.
+ Ta có
nAncol = a + c = (0,09 + c) > 0,09
⇒ MAncol < 3,2÷0,09 = 35,67
⇒ Ancol là CH3OH
⇒ Este là HCOOCH3 với số mol = 0,09
⇒ mHCOOCH3 = 5,4 gam
⇒%mHCOOCH3 = 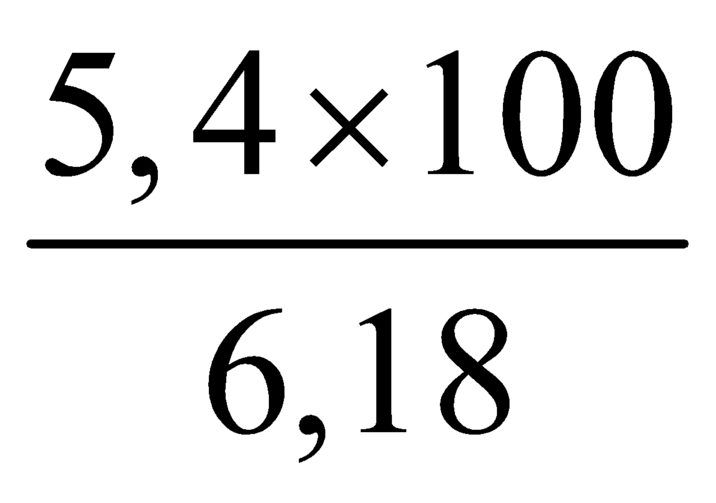 ×100% = 87,38%
×100% = 87,38%
Đúng 0
Bình luận (0)
Bài 3: Cho 4,8 gam Fe2O3 tác dụng với 1 lượng vừa đủ dd axit H2SO4 9,8% vừa đủ. Sau phản ứng thu được muối Fe2(SO4)3 và nước. Hãy tính khối lượng của dd axit đã phản ứng và khối muối thu được
PTHH: \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{4,8}{160}=0,03\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4}=0,09\left(mol\right)\\n_{Fe_2\left(SO_4\right)_3}=0,03\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{ddH_2SO_4}=\dfrac{0,09\cdot98}{9,8\%}=90\left(g\right)\\m_{Fe_2\left(SO_4\right)_3}=0,03\cdot400=12\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 3,25 g kim loại kẽm tác dụng với dd axit axetic 20%. Sau phản ứng thu được dd muối A và khí B
a,Tính thể tích khí B sinh ra (ở dktc ) và khối lượng dd Axit axetic cần dùng?
b,Sau phản úng đem cô cạn dd A thì thu được bao nhiêu gam muối khan ?
nZn = 3,25/65=0,05 mol
2Zn + 2CH3COOH --> 2CH3COOZn + H2
0,05 0,05 0,05 0,025 mol
=> VH2= 0,025*22,4=0,56 lít
mdd=(0,05*60*100)/20=15 g
b)mCH3COOZn = 0,05*124=6,2 g
Đúng 0
Bình luận (0)
Cho một lượng dư Na2CO3 vào 200 ml dd H2SO4 thấy thoát ra một chất khí không màu. Cho toàn bộ khí đó vào 88 gam dd KOH 40%. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dd thì thu được 57.6 gam hỗn hợp 3 muối khan. a) tính khối lượng mỗi muối trong hỗn hợp thu được. b) tính CM dd H2SO4 đã dùng
bài 1: hòa tan hoàn toàn 8 gam một oxit kim loại R cần vừa đủ dd chứa 10.95 gam HCl.tìm R biết R có hóa trị 3 TRONG HỢP CHẤT TRÊN.BÀI 2: hòa tan hoàn toàn 5.4 gam một kim loại X trong dd HCl dư thu được 6.72 lít khí (đktc). tìm X.bài 3: cho 31.2 gam hỗn hợp gồm kim loại Al và Al2O3 tác dụng vừa đủ với dd H2SO4 20% loãng thu được 13.44 lít khí ở đktc.a. tính tp % theo khối lượng của mỗi chất trong hỗn hợp ban đầu?b. tính khối lượng dd axit cần dùng.c. tính C% của mỗi chất có trong dd sau phản ứng...
Đọc tiếp
bài 1: hòa tan hoàn toàn 8 gam một oxit kim loại R cần vừa đủ dd chứa 10.95 gam HCl.tìm R biết R có hóa trị 3 TRONG HỢP CHẤT TRÊN.
BÀI 2: hòa tan hoàn toàn 5.4 gam một kim loại X trong dd HCl dư thu được 6.72 lít khí (đktc). tìm X.
bài 3: cho 31.2 gam hỗn hợp gồm kim loại Al và Al2O3 tác dụng vừa đủ với dd H2SO4 20% loãng thu được 13.44 lít khí ở đktc.
a. tính tp % theo khối lượng của mỗi chất trong hỗn hợp ban đầu?
b. tính khối lượng dd axit cần dùng.
c. tính C% của mỗi chất có trong dd sau phản ứng.
R2O3+6HCl->2RCl3+3H2O
nHCl=0.3(mol)
->nR=0.05(mol)->MR2O3=8:0.05=160(g/mol)
->MR=(160-16*3):2=56(g/mol)->M là Fe
Bài 2
nH2=0.3(mol)
2X+2nHCl->2XCln+nH2(n là hóa trị của kim loại)
nX=0.6:n
+) n=1->MX=9(g/mol)->loại
+)n=2->MX=18(g/mol)->loại
+)n=3->MX=27(g/mol)->X là Al
Bài cuối bạn viết phương trình,chỉ phương trình Al+H2SO4 mới tạo khí thôi,vậy bạn tính được khối lượng nhôm,từ đó tính ra khối lượng nhôm oxit nhé,vì đang vội nên mình không giải giúp bạn được
Đúng 0
Bình luận (0)
Bài 3
nH2 = \(\frac{13,44}{22,4}\) = 0,6 mol
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 \(\uparrow\) (1)
0,4 <---- 0,6 <-------- 0,2 <------ 0,6 (mol)
Al2O3 + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2O (2)
a) %mAl = \(\frac{0,4.27}{31,2}\) . 100% = 34,62%
%mAl2O3 = 65,38%
b) nAl2O3 = \(\frac{31,2-0,4.27}{102}\) = 0,2 (mol) = nAl2(SO4)3
Theo pt(2) nH2SO4 = 3nAl2O3 = 0,6 (mol)
m dd H2SO4 = \(\frac{\left(0,6+0,6\right)98}{20\%}\) = 588(g)
c) m dd spư = 31,2 + 588 - 0,6 . 2 = 618 (g)
C%(Al2(SO4)3) = \(\frac{\left(0,2+0,2\right)342}{618}\) . 100% = 22,14%
Đúng 0
Bình luận (0)
Bài 1: Gọi công thức oxit kim loại R là : R2O3
nHCl= 10,95 : 36,5 = 0,3 mol
Có pt : R2O3 +6 HCl →2 RCl3 + 3H2O
0,05mol <-- 0,3 mol
→MR2O3=mR2O3 : n = 8:0,05=160 (g/mol)
hay 2R+16.3=160↔mR=56 g/mol→R là sắt (Fe)
Bài 2:nH2=6,72 : 22,4=0,3 mol
2 X + 2n HCl→2XCln+n H2
0,6/n <--------------------- 0,3 (mol)
MX= m:n=5,4:0,6/n=9n
xét bảng :
| n | 1 | 2 | 3 |
| MX | 9(loại) | 18(loại) | 27(chọn) |
→ X là Al (nhôm)
Đúng 0
Bình luận (0)
Trung hoà 5,48 gam hỗn hợp gồm axit axetic, phenol và axit benzoic, cần dùng 600 ml dd NaOH 0,1M. Cô cạn dd sau phản ứng, thu được hỗn hợp chất rắn khan có khối lượng là: A. 6,80 gam B. 8,64 gam C. 4,90 gam D. 6,84 gam
Đọc tiếp
Trung hoà 5,48 gam hỗn hợp gồm axit axetic, phenol và axit benzoic, cần dùng 600 ml dd NaOH 0,1M. Cô cạn dd sau phản ứng, thu được hỗn hợp chất rắn khan có khối lượng là:
A. 6,80 gam
B. 8,64 gam
C. 4,90 gam
D. 6,84 gam
n NaOH = 0,06 mol . Theo đề phản ứng trung hòa vừa đủ => tổng n các axit = 0,06 mol ( tỉ lệ 1:1)
1 mol axit thành 1 mol muối natri khối lượng tăng 22g
=> 0,06 mol axit thành 0,06 mol Na khối lượng tăng 1,32g
=> m muối = m rắn = 5,48 + 1,32 = 6,8g .
=> Đáp án A
Đúng 0
Bình luận (0)