Cho 14.4 gam một kim loại chưa rõ hóa trị phản ứng hoàn toàn với 43.8 gam hcl xđ tên kim loại
Cho 7,2g một kim loại chưa rõ hóa trị , phản ứng hoàn toàn với 100 ml dung dịch HCl 6 M. Xác định tên kim loại đã dùng.
Gọi hóa trị của kim loại M là n
M + nHCl → MCln + n/2H2
nHCl = 0,6/n=> MM =
\(n_{HCl}=0,1.6=0,6\left(mol\right)\)
PTHH: 2X + 2nHCl → 2XCln + nH2
Mol: \(\dfrac{0,6}{n}\) 0,6
\(\Rightarrow M_X=\dfrac{7,2}{\dfrac{0,6}{n}}=12n\)
Do X là kim loại nên có hóa trị l, ll, lll
| n | l | ll | lll |
| MX | 12 | 24 | 36 |
| Kết luận | loại | thỏa mãn | loại |
⇒ X là magie (Mg)
Cho 7,2g kim loại M chưa rõ hóa trị, phản ứng hoàn toàn cới 21,9g HCl. Xác định tên kim loại đã dùng.
giúp mình với:33
Gọi hóa trị của kim loại M là n
M + nHCl → MCln + n/2H2
nHCl = \(\dfrac{21,9}{36,5}\)= 0,6 mol
nM = \(\dfrac{0,6}{n}\)=> MM = \(\dfrac{7,2n}{0,6}\) = 12n
=> Với n = 2 và MM = 24 g/mol là giá trị thỏa mãn
Kim loại M là Magie (Mg)
Hòa tan 8 gam oxit của một kim loại ( chưa rõ hóa trị của kim loại ) vào dung dịch chưa a gam HCl ( vừa đủ), phản ứng xong thu được 13,5g muối và nước. Xác định tên kim loại đem dùng. Tính giá trị a.
M2On+2nHCl->2MCln+nH2O
nMCl2=13.5/(MM+35.5*2)
nM2On=8/(2MM+16n)=nMCl2/2
->MM=(1136-216n)/11
vs n=2->MM=64(Cu)
hòa tan hoàn toàn 9,6 gam kim loại a chưa rõ trị bằng dd hcl vừa đủ. khi phản ứng kết thúc thu được 8,96 lít khí hidro đktc. xác định tên kim loại a
Cho 12 gam một Oxít kim loại hoá trị II phản ứng hoàn toàn với 21,9 g HCl . Xác định tên kim loại đã dùng.
nHCl = 21,9/36,5 = 0,6 (mol)
PTHH: RO + 2HCl -> RCl2 + H2O
Mol: 0,3 <--- 0,6
M(RO) = 12/0,3 = 40 (g/mol)
=> R + O = 40
=> R = 24
=> Là Mg
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\)
Gọi kim loại đó là R
\(RO+2HCl\rightarrow RCl_2+H_2O\)
0,3 0,6 ( mol )
\(M_{RO}=\dfrac{12}{0,3}=40\) ( g/mol )
Ta có: O = 16 ( g/mol )
=> R = 40-16 =24 (g/mol )
=> R là Magie(Mg)
Cho 12 gam một Oxít kim loại hoá trị II phản ứng hoàn toàn với 21,9 g HCl . Xác định tên kim loại đã dùng.
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PTHH: RO + 2HCl → RCl2 + H2O
Mol: 0,3 0,6
\(M_{RO}=\dfrac{12}{0,3}=40\left(g/mol\right)\)
\(\Rightarrow M_R=40-16=24\left(g/mol\right)\)
⇒ R là magie (Mg)
Đặt oxit KL là RO
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\\ RO+2HCl\rightarrow RCl_2+H_2O\\ n_{RO}=\dfrac{n_{HCl}}{2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ \Rightarrow M_{RO}=\dfrac{12}{0,3}=40\left(\dfrac{g}{mol}\right)\\ Mà:M_{RO}=M_R+16\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_R+16=40\\ \Leftrightarrow M_R=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow R\left(II\right):Magie\left(Mg=24\right)\)
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
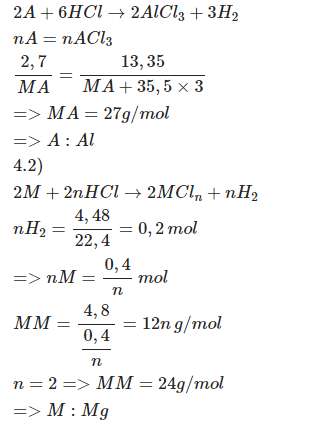
\(\Rightarrow\) \(M:mg\)
Ví dụ 1: Cho 7,2 g một kim loại chưa rõ hóa trị phản ứng hoàn toàn với 21,9 g HCl. Xác định tên kim loại.
giúp tui bài cuối cùng này nha. Xíu tui phải chụp cho cô rồi. Làm ơn ><
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PTHH: 2X + 2nHCl --> 2XCln + nH2
____\(\dfrac{0,6}{n}\)<---0,6
=> \(M_X=\dfrac{7,2}{\dfrac{0,6}{n}}=12n\left(g/mol\right)\)
Xét n = 1 => L
Xét n = 2 => MX = 24 (Mg)
Hoà tan hoàn toàn 2,8 gam một kim loại R chưa rõ hoá trị bằng dung dịch HCl loãng dư, sau phản ứng thu được 1,12 lít H2 (đktc). Kim loại R là:
A. Fe.
B. Cu.
C. Zn.
D. Al.