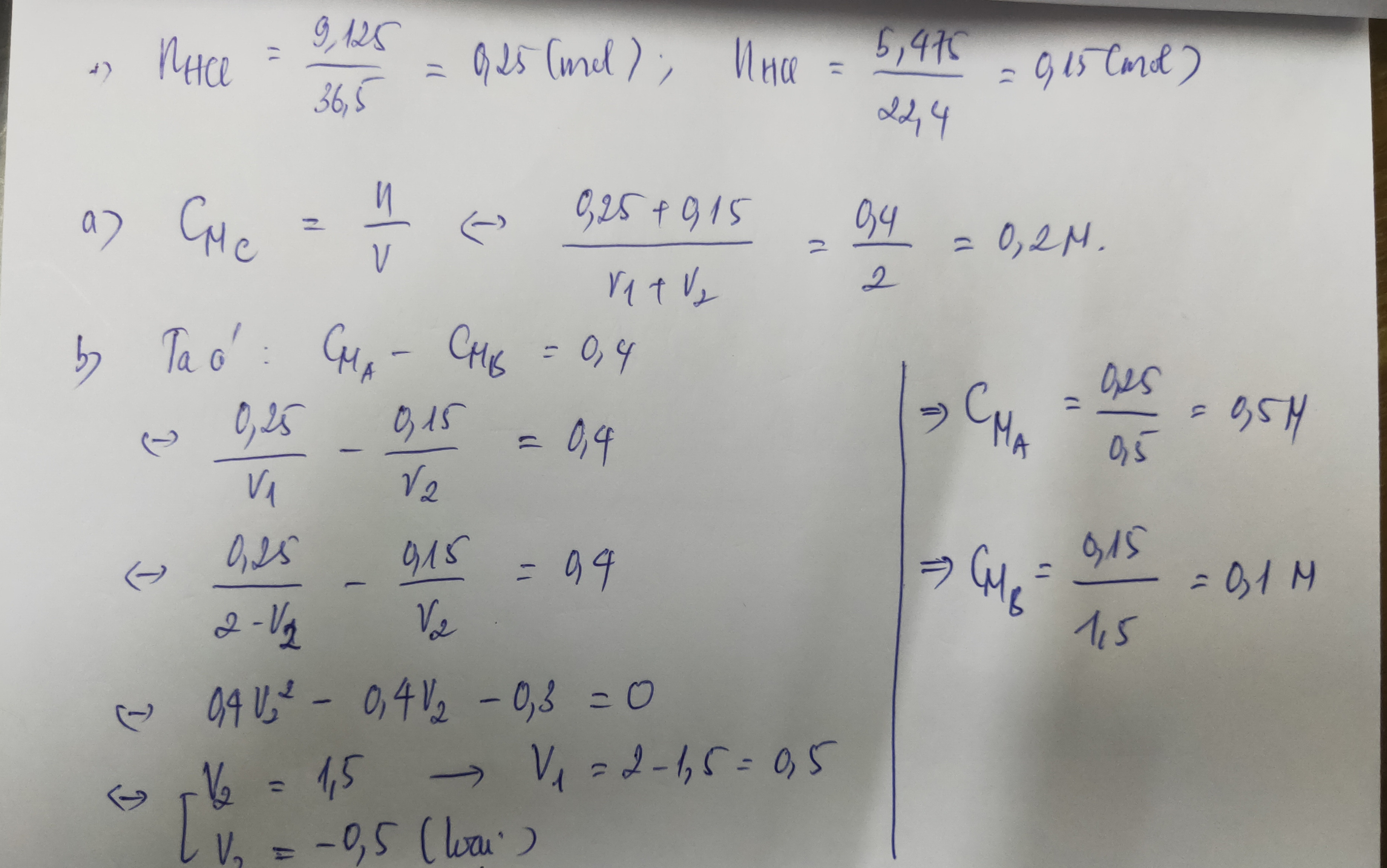Trộn V1 lít dd H2SO4 1,5M vs V2 lít dd NaOH 2M thu được 800ml dd A . Tính V1 , V2 biết 800ml dd A có thể hòa tan 15,3 g Al2O3 ( giả sử pha trộn không làm thay đổi thể tích dung dịch)

Những câu hỏi liên quan
trộn v1 l dd h2so4 0,3M với v2 l dd naoh0,4M thu đc 0,6l dung dịch A.tính v1,v2 biết 0,3 l dd A hòa tan vừa đủ 0,51 g al2o3
Coi sự pha trộn không thay đổi thể tích và xảy ra hoàn toàn
Trộn V1 lít dung dịch HCl 0,6M với V2 lít dung dịch NaOH 0,4M thu được 0,6 lít dung dịch A. Biết 0,6 lít dung dịch A có thể hòa tan hết 1,02 gam Al2O3 (xem như sự pha trộn không làm thay đổi thể tích). Tính V1 và V2.
nHCl=0,6V1 mol; n NaOH=0,4V2 mol
Do dd A có thể hòa tan Al2O3=> HCl hoặc NaOH dư
*TH1: HCl dư
Al2O3+6HCl-> 2AlCl3+3H2O nAl2O3=0,01 mol=> nHCl dư =0,06 mol
nHCl phản ứng= n NaOH=0,4V2 mol=>n HCl dư = 0,6V1-0,4V2=0,06 mol
V1+V2=0,6l
giải hpt ra V1=V2=0,3l
*TH2: NaOH dư
2NaOH+Al2O3-> 2NaAlO2+H20 (3)
n NaOH dư=2nAl2O3=0,02 mol
=>nNaOH dư= 0,4V2-0,6V1=0,02 mol
V1+V2=0,6l
giải hpt ra V1=0,22l, V2=0,38l
Đúng 0
Bình luận (1)
Trộn V1 , 1 lít dd HCl 0,6 M , với V2 , 1 dd NaOH 0,4 M thu được 0,6 l dd A . Tính V1 ,V2 . Biết 0,6 l dd A có thể hòa tan hết 1,02 gam Al2O3 (coi sự pha trộn ko làm thay đổi thể tích).
nAl2O3 = 0.1
nHCl = 0.6V1
nNaOH = 0.4V2
TH1: HCl dư
NaOH + HCl = NaCL + H2O
0.4V2----0.4V2
Al2O3 + 6HCl = 2AlCl3 + 3H2O
0.1----------0.6
có 0.6 = 0.6V1 - 0.4V2
V1 + V2 = 0.6
=> loại
TH2 : NaOH dư
NaOH + HCl = NaCL + H2O
0.6V1----0.6V1
2NaOH + Al2O3 = 2NaALO2 + H2O
0.2------------0.1
0.2 = 0.4V2 - 0.6V1
V1 + V2 = 0.6
=> V1 = 0.04,V2 = 0.56
Đúng 0
Bình luận (0)
trộn V1 lít dd NaOH 0,4M vs V2 lít dd HCl 0,6M đc 0,5 lít dd A. Tính V1, V2 biết 0,5 lít dd A hòa tan đc tối đa 4 gam CuO
n CuO = 4/80 = 0,05(mol)
CuO + 2HCl $\to$ CuCl2 + H2O
n HCl dư = 2n CuO = 0,1(mol)
$NaOH + HCl \to NaCl + H_2O$
Theo PTHH :
n HCl pư = n NaOH = 0,4.V1 = 0,4V1(mol)
Suy ra:
0,4V1 + 0,1 = 0,6V2
mà V1 + V2 = 0,5
Suy ra V1 = 0,2 (lít) ; V2 = 0,3(lít)
Đúng 2
Bình luận (0)
Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 7. Tính tỉ lệ V1 : V2
\(pH=7\Rightarrow n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(0,05+0,06.2\right)\text{}V_2=\left(0,08+0,02.2\right)V_1\)
\(\Rightarrow V_1:V_2=17:12\)
Đúng 1
Bình luận (0)
Bài 3. Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 13. Tính tỉ lệ V1 : V2
\(n_{OH^-}=0,12V_1\)
\(n_{H^+}=0,17V_2\)
\(n_{OH^-dư}=\left(V_1+V_2\right).10^{-1}\)
Ta có:
\(n_{OH^-dư}+n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(V_1+V_2\right).10^{-1}=0,12V_1\)
\(\Leftrightarrow0,1V_1=0,02V_2\)
\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{5}\)
Đúng 1
Bình luận (0)
Trộn V1 dd HCl 0,1M với V2 dd HCl 0,5M thu đc 400ml dd HCl 0,35M . Tính V1, V2 giả sử thể tích hao hụt ko đáng kể
\(n_{HCl\left(3\right)}=0,35.0,4=0,14\left(mol\right)\)
Ta có: \(\left\{{}\begin{matrix}0,1.V_1+0,5.V_2=0,14\\V_1+V_2=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}V_1=0,15\\V_2=0,25\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Trộn lẫn V1 ml dd NaOH 3% có D=1,05g/ml và V2 ml dd NaOH 10%, D= 1,12g/ml để pha chế được 2 lít dd NaOH 8% có khối lượng riêng là 1,1g/ml. Tính V1 và V2
1.
Nồng độ mol/lit của đ NaOH(1)=\(\dfrac{3.10.1,05}{40}\)=0.7875
......................................... khi trộn là: =\(\dfrac{8.10.1,1}{40}\)=2.2
Áp dụng quy tắc đường chéo ta có
Vdd1/(2-Vdd1)=0.42477
---> Vdd1=0.6l
Vdd2=1.4l
Đúng 1
Bình luận (0)
Có V1 lít dd HCl chứa 9,125g HCl (dd A) và V2 lít dd HCl chứa 6,475 HCl (dd B). Trộn dd A với ddB để được 2l ddC. Khi pha trộn V dd không đổi
a/ Tính CM của dd C
b/ Tính CM của 2 dd A và B biết hiệu số CM của 2 dd là 0,4M.