Chọn 7 chất rắn khác nhau lần lượt tác dụng với HCl có 7 khi thoát ra.Viết các PTHH PƯ minh họa.
Mình mới tìm dc 5 khí(SO2;CO2;H2S;H2;Cl2)
Cho m1 gam Al vào 100 ml dung dịch gồm Cu(NO3)2 0,3M và AgNO3 0,3M. Sau khi các phản ứng xảy ra hoàn toàn thì thu đựơc m2 gam chất rắn X. Nếu cho m2 gam X tác dụng với lượng dư dung dịch HCl thì thu được 0,336 lít khí (đktc). Giá trị của m1 và m2 lần lượt là:
A. 8,10 và 5,43
B. 1,08 và 5,16
C. 0,54 và 5,16
D. 1,08 và 5,43
Đáp án D
Ta có:
![]()
Chất rắn X + dd HCl dư → H2
⇒ trong chất rắn X có Al dư
⇒ Cu(NO3)2 và AgNO3 hết
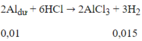
Al phản ứng hết với dd Cu(NO3)2 và AgNO3
Quá trình nhận e:

Tổng số mol e nhận = 0,06 + 0,03 = 0,09 mol
Quá trình nhường e:
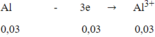
Vậy:
m2 = mAl dư + mCu + mAg = 0,01.27 + 0,03.64 + 0,03.108 = 5,43 gam
m1 = mAl ban đầu = (0,01 + 0,03).27 = 1,08g
Đốt nóng hỗn hợp gồm FeO và CuO với Cacbon có dư thì thu được chất rắn A và khí B. Cho B tác dụng với nước vôi trong có dư thu được 8 gam kết tủa. Cho chất rắn A tác dụng với dung dịch HCl có nồng độ 10% thì cần một lượng axit là 73 gam thì vừa đủ.
a. Viết các PTPU xảy ra.
b. Tính khối lượng FeO và CuO trong hỗn hợp ban đầu và thể tích khí B sinh ra. (các khí đo ở đktc)
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl
Bài 1 :
Cho 24,8 gam hỗn hợp gồm Na2CO3 và Na2SO4 tác dụng với dung dịch BaCl2 dư thấy tạo a gam kết tủa X .Cho a gam kết tủa trên tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí đktc và còn lại là b gam chất rắn Y . tìm giá trị a,b
Bài 2 : Có 5 chất bột trắng : NaCl ; Na2CO3 ; Na2SO4 ; BaCO3 ; BaSO4 .Chỉ dùng nước và khí CO2 hãy , có thể phân biệt được từng chất không ? Nếu được hãy trình bày cách nhận biết .Viết các PTHH .
Bài 1 :
PTHH :
\(Na_2CO_3+BaCl_2-->BaCO_3\downarrow+2NaCl\left(1\right)\)
\(Na_2SO_4+BaCl_2-->BaSO_4\downarrow+2NaCl\left(2\right)\)
Từ (1) và (2) => kết tủa thu được là \(BaCO_3;BaSO_4\)
Cho X tác dụng với dung dịch HCl dư ta có phương trình :
\(BaCO_3+2HCl-->BaCl_2+H_2O+CO_2\uparrow\)
\(\rightarrow\) Khí sinh ra là CO\(_2\) .Chất rắn Y không bị hoà tan là \(BaSO_4\)
\(\left(1\right)->n_{Na_2SO_3}=n_{BaCO_3}=n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(->m_{Na_2CO_3}=0,1.106=10,6\left(g\right)->n_{Na_2SO_4}=24,8-10,6=14,2\left(g\right)\)
\(\Rightarrow n_{Na_2SO_4}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
\(\left(2\right)->n_{BaSO_4}=n_{Na_2SO_4}=0,1\left(mol\right)\)
\(->m_{BaCO_3}=0,1.197=19,7\left(g\right)\)
\(->m_{BaSO_4}=0,1.233=23,3\left(g\right)->b=23,3\)
\(->a=19,7+b=19,7+23,3=43\)
Vậy ........................
Chỉ dùng CO2 và nước có thể phân biệt từng chất trong 5 chất trên :
| Thuốc thử | NaCl | \(Na_2CO_3\) | \(Na_2SO_4\) | \(BaCO_3\) | \(BaSO_4\) |
| \(H_2O\) | tan | tan | tan | không tan | không tan |
| \(CO_2\)dư ( lần 1) | \(\downarrow\)tan ( dung dịch 1 ) | \(\downarrow\) không tan | |||
| Dung dịch 1 | không có hiện tượng | \(\downarrow\) (trắng ) | \(\downarrow\) ( trắng ) | ||
| \(CO_2\)dư ( lần 2 ) | \(\downarrow\) tan | \(\downarrow\) không tan |
PTHH :
( lần 1 ) \(CO_2+H_2O+BaCO_3-->BaHCO_3\left(dd1\right)\)
\(Ba\left(HCO_3\right)_2+Na_2CO_3-->BaCO_3\downarrow+2NaHCO_3\)
\(Ba\left(HCO_3\right)_2+Na_2SO_4-->BaSO_4\downarrow+2NaHCO_3\)
( lần 2 ) \(CO_2+H_2O+BaCO_3-->Ba\left(HCO_3\right)_2\)
Trên màn hình có một số biểu tượng phần mềm. Em và bạn hãy lần lượt sử dụng chuột để thực hiện các thao tác sau:
a) Nháy chuột vào biểu tượng This PC để chọn nó.
b) Nháy chuột vào một vị trí khác để không chọn biểu tượng đó nữa.
c)Nháy chuột chọn một biểu tượng rồi kéo thỏ chuột để di chuyển nó.
d)Nháy chuột chọn một biểu tượng phần mềm ở cạnh biểu tượng This PC.
Quan sát và nhận xét bạn cầm chuột có đúng không?
Em lần lượt thực hiện các thao tác và quan sát xem bạn cầm chuột đúng cách hay chưa.
Câu 1: Hỗn hợp A nặng m gam gồm Fe2O3 và Al.Nung A đến hoàn toàn thu được rắn B, choB tác dụng H2SO4 loãng thu được 2240 ml khí đktc. Mặt khác nếu cho B tác dụng với dung dịch NaOH dư thì thấy còn lại 13,6 gam chất rắn không tan.
a) Xác định khối lượng các chất trong A và B.
b) Tính thể tích dung dịch HCl 0,5M để hòa tan hết 13,6 gam chất rắn trên.
Câu 2: Có 11,98 gam hỗn hợp X gồm Al và Fe3O4. Thực hiện phản ứng nhiệt nhôm sau một thời gian thu được rắn Y. Hòa tan Y vào dung dịch NaOH dư thu được dung dịch Z và thoát ra 2,016 lít khí (đktc). Sục khí CO2 đến dư vào dung dịch Z thu được 7,8gam kết tủa. Tính khối lượng mỗi chất trong X và Y. Tính hiệu suất phản ứng nhiệt nhôm.
giải chi tiết giúp mình với , mình cảm ơn nhiều :)))
Câu 1:
a)
Gọi \(\left\{{}\begin{matrix}n_{Fe_2O_3}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
TH1: Al dư
PTHH: Fe2O3 + 2Al --to--> Al2O3 + 2Fe
a--->2a-------->a------->2a
=> B gồm \(\left\{{}\begin{matrix}Al_2O_3:a\left(mol\right)\\Fe:2a\left(mol\right)\\Al:b-2a\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
2a------------------------>2a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
(b-2a)------------------------>1,5(b - 2a)
=> 2a + 1,5b - 3a = 0,1
=> 1,5b - a = 0,1
Rắn không tan là Fe
=> \(n_{Fe}=2a=\dfrac{13,6}{56}=\dfrac{17}{70}\left(mol\right)\)
=> \(a=\dfrac{17}{140}\left(mol\right)\) => \(b=\dfrac{31}{210}\left(mol\right)\)
Xét \(n_{Al\left(dư\right)}=b-2a=\dfrac{-2}{21}\) (vô lí)
TH2: Fe2O3 dư
PTHH: Fe2O3 + 2Al --to--> Al2O3 + 2Fe
0,5b<---b--------->0,5b---->b
=> B gồm \(\left\{{}\begin{matrix}Al_2O_3:0,5b\left(mol\right)\\Fe:b\left(mol\right)\\Fe_2O_3:a-0,5b\left(mol\right)\end{matrix}\right.\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
b------------------------>b
=> b = 0,1
Rắn không tan gồm Fe và Fe2O3
=> \(56b+160\left(a-0,5b\right)=13,6\)
=> a = 0,1
A gồm \(\left\{{}\begin{matrix}Fe_2O_3:m_{Fe_2O_3}=0,1.160=16\left(g\right)\\Al:m_{Al}=0,1.27=2,7\left(g\right)\end{matrix}\right.\)
B gồm \(\left\{{}\begin{matrix}Al_2O_3:m_{Al_2O_3}=0,05.102=5,1\left(g\right)\\Fe:m_{Fe}=0,1.56=5,6\left(g\right)\\Fe_2O_3:m_{Fe_2O_3}=0,05.160=8\left(g\right)\end{matrix}\right.\)
b)
Rắn không tan gồm \(\left\{{}\begin{matrix}Fe:0,1\left(mol\right)\\Fe_2O_3:0,05\left(mol\right)\end{matrix}\right.\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1-->0,2
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
0,05---->0,3
=> nHCl = 0,2 + 0,3 = 0,5 (mol)
=> \(V_{ddHCl}=\dfrac{0,5}{0,5}=1\left(l\right)\)
Câu 2:
\(n_{H_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)\)
Gọi số mol Al2O3 là x (mol)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,06<---------------------0,06<--------0,09
Al2O3 + 2NaOH --> 2NaAlO2 + H2O
x------------------>2x
2NaAlO2 + CO2 + 3H2O --> Na2CO3 + 2Al(OH)3
0,1<-------------------------------------0,1
=> 0,06 + 2x = 0,1
=> x = 0,02 (mol)
PTHH: 8Al + 3Fe3O4 --to--> 4Al2O3 + 9Fe
Có \(\dfrac{n_{Al_2O_3}}{n_{Fe}}=\dfrac{4}{9}\)
=> nFe = 0,045 (mol)
mY = mX = 11,98 (g)
=> \(m_{Al_2O_3}+m_{Al\left(Y\right)}+m_{Fe}+m_{Fe_3O_4\left(Y\right)}=11,98\)
=> \(m_{Fe_3O_4\left(Y\right)}=5,8\left(g\right)\)
=> \(n_{Fe_3O_4\left(Y\right)}=\dfrac{5,8}{232}=0,025\left(mol\right)\)
Bảo toàn Fe: \(n_{Fe_3O_4\left(bđ\right)}=0,04\left(mol\right)\)
Bảo toàn Al: nAl(bđ) = 0,1 (mol)
PTHH: 8Al + 3Fe3O4 --to--> 4Al2O3 + 9Fe
Xét tỉ lệ: \(\dfrac{0,1}{8}< \dfrac{0,04}{3}\) => Hiệu suất tính theo Al
PTHH: 8Al + 3Fe3O4 --to--> 4Al2O3 + 9Fe
0,04<------------------0,02
=> \(H\%=\dfrac{0,04}{0,1}.100\%=40\%\)
Chất tác dụng với dung dịch N a 2 C O 3 tạo khí thoát ra là
A. HCl.
B. N a 2 S O 4 .
C. F e S O 4 .
D. B a C l 2 .
em hãy so sánh sự khác nhau và giống nhau về sự nở ra vì nhiệt của chất rắn và chất khí.
giúp mình với ![]()
Giống nhau:
- Chất khí và chất rắn đều có nở khi nhiệt độ tăng và co lại khi nhiệt độ giảm.
Khác nhau:
- Các chất rắn khác nhau nở vì nhiệt khác nhau còn các chất khí khác nhau nở vì nhiệt giống nhau.
- Chất khí nở vì nhiệt nhiều hơn chất rắn
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3, thu được 0,448 lít NO (đktc) là sản phẩm khử duy nhất và m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây
A. 413
B. 415
C. 411
D. 414