a, Hỗn hợp X gồm K và Al có khối lượng 10,5 gam hòa tan X vào nước x tan hết tạo thành dung dịch A Cho từ từ HCl vào dung dịch A lúc đầu cho kết tủa thì khi thể tích HCl 1M vào là 100 ml thìa bắt đầu kết tủa Tính phần trăm khối lượng mỗi kim loại trong x. b, Một hỗn hợp y gồm K Al trộn 10,5 gam X với 9,3 gam y được hỗn hợp Z cho Z tan hết trong nước được dung dịch B. Thêm 1 giọt dd HCl vào B thì đã xuất hiện kết tủa Tính khối lượng KL trong y.

Những câu hỏi liên quan
Một hỗn hợp X gồm K và Al có khối lượng là 10,5 gam. Hòa tan X trong nước thì hỗn hợp X tan hết cho ra dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A. Khi bắt đầu không có kết tủa. Kể từ thể tích dung dịch HCl 1M thêm vào là 100ml thì dung dịch A bắt đầu cho kết tủa. Số mol mỗi kim loại trong hỗn hợp X là (các phản ứng xảy ra hoàn toàn): A.
n
K
0...
Đọc tiếp
Một hỗn hợp X gồm K và Al có khối lượng là 10,5 gam. Hòa tan X trong nước thì hỗn hợp X tan hết cho ra dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A. Khi bắt đầu không có kết tủa. Kể từ thể tích dung dịch HCl 1M thêm vào là 100ml thì dung dịch A bắt đầu cho kết tủa. Số mol mỗi kim loại trong hỗn hợp X là (các phản ứng xảy ra hoàn toàn):
A. n K = 0 , 1 mol ; n Al = 0 , 2 mol
B. n K = 0 , 2 mol ; n Al = 0 , 1 mol
C. n K = 0 , 2 mol ; n Al = 0 , 15 mol
D. n K = 0 , 15 mol ; n Al = 0 , 1 mol
Hỗn hợp X gồm hai kim loại K và Al có khối lượng 10,5 gam. Hòa tan hoàn toàn hỗn hợp X trong nước được dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A: lúc đầu không có kết tủa, khi thêm được 100 ml dung dịch HCl 1M thì bắt đầu có kết tủa. Tính thành phần % số mol của các kim loại trong X.
Ta có phương trình:
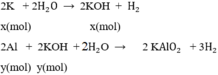
Thêm từ từ HCl vào dd A lúc đầu không có kết tủa do HCl trung hòa KOH dư:
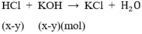
Khi HCl trung hòa hết KOH dư thì xuất hiện kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 + KCl
Gọi x, y lần lượt là mol K và Al ban đầu
Để trung hòa hết KOH cần: 0,1. 1 = 0,1 mol HCl
Theo pt ⇒ x - y = 0,1
Theo bài ra ta có hệ pt:
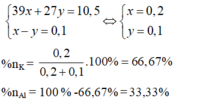
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm hai kim loại K và Al có khối lượng 10,5 gam. Hòa tan hoàn toàn hỗn hợp X trong nước được dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A, lúc đầu không có kết tủa, khi thêm được 100 ml dung dịch HCl 1M thì bắt đầu có kết tủa. Tính thành phần % số mol của các kim loại trong X.
Gọi số mol K và Al trong hỗn hợp x, y
2K + 2H2O → KOH + H2 (1)
x x (mol)
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2)
y y (mol)
Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì:
HCl + KOH → KCl + H2O (3)
X – y x – y (mol)
Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4)
Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M.
Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I)
Mặt khác: 39x + 27 y = 10,5 (II)
Từ (1) và (II) ⇒ x = 0,2; y = 0,1.
% nK =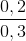 .100% = 66,67%;
.100% = 66,67%;
%nAl = 100% – 66,67% = 33,33%.
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm hai kim loại K và Al có khối lượng 10,5 gam. Hòa tan hoàn toàn hỗn hợp X trong nước được dung dịch A. Thêm từ từ dung dịch HCl 1M vào dung dịch A: lúc đầu không có kết tủa, khi thêm được 100 ml dung dịch HCl 1M thì bắt đầu có kết tủa. Tính thành phần % số mol của các kim loại trong X.
Gọi số mol K và Al trong hỗn hợp x, y
2K + 2H2O → KOH + H2 (1)
x x (mol)
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2)
y y (mol)
Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì:
HCl + KOH → KCl + H2O (3)
X – y x – y (mol)
Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4)
Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M.
Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I)
Mặt khác: 39x + 27 y = 10,5 (II)
Từ (1) và (II) => x = 0,2; y = 0,1.
% nK = 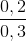 .100% = 66,67%;
.100% = 66,67%;
%nAl = 100% - 66,67% = 33,33%.
Đúng 0
Bình luận (1)
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và Al vào nước dư, thu được dung dịch Y. Chia Y làm ba phần bằng nhau: - Cho từ từ dung dịch HCl 1M vào phần một đến khi bắt đầu xuất hiện kết tủa thì dùng hết 100 ml. - Cho từ từ 450 ml dung dịch HCl 1M vào phần hai, thu được 3a gam kết tủa. - Cho từ từ 750 ml dung dịch HCl 1M vào phần ba, thu được a gam kết tủa. Giá trị của m là A. 36,90. B. 28,50. C. 40,65. D. 44,40.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và Al vào nước dư, thu được dung dịch Y. Chia Y làm ba phần bằng nhau:
- Cho từ từ dung dịch HCl 1M vào phần một đến khi bắt đầu xuất hiện kết tủa thì dùng hết 100 ml.
- Cho từ từ 450 ml dung dịch HCl 1M vào phần hai, thu được 3a gam kết tủa.
- Cho từ từ 750 ml dung dịch HCl 1M vào phần ba, thu được a gam kết tủa.
Giá trị của m là
A. 36,90.
B. 28,50.
C. 40,65.
D. 44,40.
Chọn D.
Dung dịch Y chứa NaOH và NaAlO2
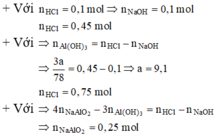
Vậy X gồm Na (1,05 mol) và Al (0,75 mol) Þ m = 44,4 (g)
Đúng 0
Bình luận (0)
Hỗn hợp x gồm 2 kim loại là Na và Al có khối lượng là 7,3 gam. Hòa tan hỗn hợp x chống nước được dung dịch A. Thêm từ từ dung dịch ax HCl 2M vào dung dịch A:lúc đầu không có kết tủa, khi thêm được 50 ml dung dịch HCl 2M thì bắt đầu có kết tủa. Tính tỷ lệ về số mol giữa Na và Al trong X.
Hòa tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt X. Thêm từ từ dung dịch HCl 1M vào dung dịch X nhận thấy khi bắt đầu xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100 ml. Còn khi cho 250 ml hoặc 650 ml dung dịch HCl 1M vào dung dịch X thì sẽ thu được lượng kết tủa như nhau. Giá trị m là A. 20,5 B. 23,6 C. 19,5 D. 39,0
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp Na2O, Al2O3 vào nước được dung dịch trong suốt X. Thêm từ từ dung dịch HCl 1M vào dung dịch X nhận thấy khi bắt đầu xuất hiện kết tủa thì thể tích dung dịch HCl 1M đã cho vào là 100 ml. Còn khi cho 250 ml hoặc 650 ml dung dịch HCl 1M vào dung dịch X thì sẽ thu được lượng kết tủa như nhau. Giá trị m là
A. 20,5
B. 23,6
C. 19,5
D. 39,0
Gọi số mol của Na2O là x, Al2O3 là y mol
Nhận thấy khi thêm 0,1 mol HCl mới bắt đầu tạo kết tủa → Trong dung dịch X chứa NaAlO2 và NaOH dư → nNaOH dư = 0,1 mol
Khi thêm 0,25 mol hoặc 0,65 mol HCl thì lượng kết tủa như nhau → khi thêm 0,25 mol HCl thì lượng HCl hết lượng NaAlO2 còn dư
→ nHCl = nNaOH dư + nAl(OH)3 → 0,25 = 0,1 + nAl(OH)3 → nAl(OH)3 = 0,15 mol
Khi thêm 0,65 mol thì HCl và NaAlO2 đều hết
→ 4nNaAlO2 = (nHCl -nNaOH dư)+ 3nAl(OH)3 → 8y = (0,65-0,1) + 3.0,15 → y = 0,125 mol
Bảo toàn nguyên tố Na → nNa2O = (nNaOH dư + nNaAlO2) :2 = (0,1 + 0,25 ):2 = 0,175mol
→ m= 0,125.102 +0,175.62 = 23,6 gam.
Đáp án B
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2O và Al2O3 vào nước, thu được dung dịch X. Thêm từ từ dung dịch HCl 1M vào X, khi hết 100 ml thì bắt đầu xuất hiện kết tủa; khi hết 300 ml hoặc 700 ml thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là A. 23,4 và 35,9 B. 15,6 và 27,7 C. 23,4 và 56,3 D. 15,6 và 55,4
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2O và Al2O3 vào nước, thu được dung dịch X. Thêm từ từ dung dịch HCl 1M vào X, khi hết 100 ml thì bắt đầu xuất hiện kết tủa; khi hết 300 ml hoặc 700 ml thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là
A. 23,4 và 35,9
B. 15,6 và 27,7
C. 23,4 và 56,3
D. 15,6 và 55,4
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2O và Al2O3 vào nước, thu được dung dịch X. Thêm từ từ dung dịch HCl 1M vào X, khi hết 100 ml thì bắt đầu xuất hiện kết tủa; khi hết 300 ml hoặc 700 ml thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là A. 23,4 và 35,9 B. 15,6 và 27,7. C. 23,4 và 56,3. D. 15,6 và 55,4
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2O và Al2O3 vào nước, thu được dung dịch X. Thêm từ từ dung dịch HCl 1M vào X, khi hết 100 ml thì bắt đầu xuất hiện kết tủa; khi hết 300 ml hoặc 700 ml thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là
A. 23,4 và 35,9
B. 15,6 và 27,7.
C. 23,4 và 56,3.
D. 15,6 và 55,4
Đáp án B
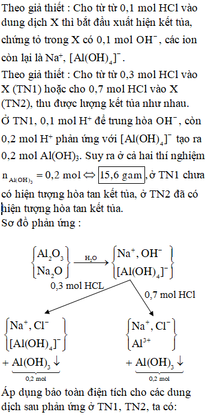
Cho từ từ 0,1 mol HCl vào dung dịch X thì bắt đầu xuất hiện kết tủa, chứng tỏ trong X có 0,1 mol OH - , các ion còn lại là Na+, Al OH 4 - .
Cho từ từ 0,3 mol HCl vào X (TN1) hoặc cho 0,7 mol HCl vào X (TN2), thu được lượng kết tủa như nhau. Ở TN1, 0,1 mol H+ để trung hòa OH - , còn 0,2 mol H+ phản ứng với Al OH 4 - tạo ra 0,2 mol Al(OH)3. Suy ra ở cả hai thí nghiệm
![]()
ở TN1 chưa có hiện tượng hòa tan kết tủa, ở TN2 đã có hiện tượng hòa tan kết tủa.
Sơ đồ phản ứng :
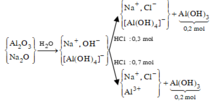
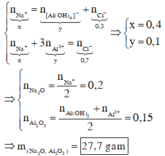
Áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng ở TN1, TN2, ta có :
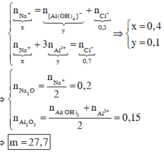
Đúng 0
Bình luận (0)