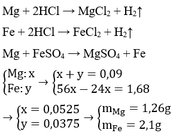Cho hỗn hợp kim loại Mg và Fe vào H2SO4 loãng dư . Sau phản ứng , thu được 2,016 lít khí ( đktc ) . Nếu cho hỗn hợp này tác dụng với FeSO4 dư thì khối lượng kim loại tăng 1,68 g . Tính khối lượng mỗi kim loại trong hỗn hợp .

Những câu hỏi liên quan
Cho H2SO4 loãng dư tác dụng với hợp kim Mg, Fe thu được 2,016 lít khí ở đktc. Nếu hợp kim này tác dụng với dung dịch FeSO4 dư thì khối lượng hợp kim tăng lên 1,68 gam. Tính khối lượng mỗi kim loại trong hợp kim
Cho 12,4 g hỗn hợp x gồm 2 kim loại cu và mg vào dung dịch H2SO4 loãng dư,thu được 5,6 lít khí(đktc) A)Tính khối lượng mỗi kim loại trong hỗn hợp x B)Cho hỗn hợp trên tác dụng với dung dịch AgNO3 dư tính khối lượng kim loại tạo thành Giải giúp ghi rõ a)b)c) để mình biết
cho 3,79 (G) hỗn hợp Zn và Al tác dụng với dung dịch H2SO4 loãng dư .Sau phản ứng thu được 1,792 lít khí (đktc)
a)tính khối lượng mỗi kim loại
b) tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu
PTHH:
Zn + H2SO4 ---> ZnSO4 + H2 (1)
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
Ta có: \(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
Gọi x, y lần lượt là số mol của Zn và Al
a. Theo PT(1): \(n_{H_2}=n_{Zn}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}y\left(mol\right)\)
=> \(x+\dfrac{3}{2}y=0,8\) (*)
Theo đề, ta có: 65x + 27y = 3,79 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+\dfrac{3}{2}y=0,8\\65x+27y=3,79\end{matrix}\right.\)
(Ra số âm, bn xem lại đề nhé.)
Đúng 0
Bình luận (0)
Bài 6: Cho 11,6 gam hỗn hợp 2 kim loại Cu và Fe vào dd H2SO4 loãng dư, thu được 3,36 lít khí (đktc).
Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu.
Tính khối lượng muối thu được sau phản ứng.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
_____0,15<--------------0,15<---0,15
=> mFe = 0,15.56 = 8,4 (g)
=> mCu = 11,6 - 8,4 = 3,2 (g)
\(\left\{{}\begin{matrix}\%Fe=\dfrac{8,4}{11,6}.100\%=72,414\%\\\%Cu=\dfrac{3,2}{11,6}.100\%=27,586\%\end{matrix}\right.\)
mFeSO4 = 0,15.152 = 22,8 (g)
Đúng 1
Bình luận (0)
Cho 7,8 gam hỗn hợp hai kim loại là Mg và Al tác dụng với dung dịch H 2 SO 4 loãng, dư. Khi phản ứng kết thúc, người ta thu được 8,96 lít khí (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Khối lượng kim loại trong hỗn hợp:
- Số mol H 2 ở (1) và (2) n H 2 = 8,96/22,4 = 0,4 mol
- Đặt x và y là số mol Mg và Al có trong hỗn hợp. Từ (1) và (2) ta có hệ phương trình đại số :
x + 3/2y = 0,4
24x + 27y = 7,8
Giải hệ phương trình, ta được x = 0,1 và y = 0,2.
Khối lượng các kim loại :
m Mg = 0,1 x 24 = 2,4g
m Al = 0,2 x 27 = 5,4g
Đúng 1
Bình luận (0)
Cho hỗn hợp hai kim loại Mg và Fe và H2SO4 loãng , dư . Sau phản ứng , thu được 2,016 lít khí ( đktc ) . Nếu cho hỗn hợp này tác dụng với FeSO4 dư thì khối lượng kim loại tăng 1,68 gma , Tính khối lượng mỗi kim loại trog hỗn hợp .
Ta có phương trình phản ứng :
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2\(\) ( 1 )
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2\(\) ( 2 )
Mg + FeSO4 \(\rightarrow\) MgSO4 + Fe ( 3 )
\(n_{H_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)\(\)
Đặt số mol của Mg và Fe lần lượt là a và b . ( a , b > 0 ) \(n_{Fe\left(3\right)}=n_{Mg}=a\) Ta có : \(\left\{{}\begin{matrix}a+b=0,09\\m_{Fe\left(3\right)}-m_{Mg}=1,68\Rightarrow56a-24a=1,68\Rightarrow32a=1,68\Rightarrow a=0,0525\end{matrix}\right.\) \(\Rightarrow b=0,09-0,0525=0,0375\) \(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=24.0,0525=1,26\\m_{Fe\left(3\right)}=56.0,0375=2,1\end{matrix}\right.\)
Đúng 0
Bình luận (2)
PT1: Mg + H2SO4 -> MgSO4 +H2\(\uparrow\)
PT2: Fe + H2SO4 -> FeSO4 +H2\(\uparrow\)
theo 2 pt trên khí đó là H2
=> nH2=V/22,4=2,016/22,4=0,09(mol)
Cho hỗn hợp 2 kim loại tác dụng với FeSO4 thì chỉ có Mg phản ứng ,
Gọi a là số mol Mg
Pt3: Mg +FeSO4 -> MgSO4 + Fe\(\downarrow\)
vì sau phản ứng 3 thì khối lượng kim loại kim loại tăng 1,68 gam nên
mFe(3) - mMg(3)=1,68
<=> 56a-24a=1,68
=> a= 0,0525 (mol)
=> nMg=0,0525(mol)
Theo pt 1: nMg=nH2=0,0525(mol)
=> nH2(còn lại ở PT2)=0,09-0,0525=0,0375(mol)
mà nH2(pt2)=nFe
=> nH2(pt2)=nFe =0,0375(mol)
Vậy mMg=nMg.MMg=0,0525.24=1,26(g)
mFe=nFe.MFe=0,0375.56=2,1 (g)
Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp Al, Fe tác dụng với dung dịch H 2 S O 4 loãng, dư thấy thu được 8,96 lít khí ở đktc. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít khí H 2 ở đktc. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Bài 3 : cho 13,2g hỗn hợp A gồm Mg và Cu tác dụng với dung dịch h2so4 dư sau phản ứng thu được 3,36 lít khí h2 ( đktc )
a. Tính phần trăm khối lượng của từng kim loại trong hỗn hợp ban đầu
b. Nếu cho hỗn kim loại trên vào dung dịch h2so4 đặc nóng thu được khí so2 ( đktc ) tính khối lượng muối tạo thành
Bài 4 : hoà tan hoàn toàn 18,4g hỗn hợp X gồm Fe và Mg bằng dung dịch HCl 0,8M (vừa đủ) sau phản ứng thu được 11,2 lít khí (đktc)
a. Tính thành phần phần trăm khối lượng mỗi kim loại có trong hỗn...
Đọc tiếp
Bài 3 : cho 13,2g hỗn hợp A gồm Mg và Cu tác dụng với dung dịch h2so4 dư sau phản ứng thu được 3,36 lít khí h2 ( đktc ) a. Tính phần trăm khối lượng của từng kim loại trong hỗn hợp ban đầu b. Nếu cho hỗn kim loại trên vào dung dịch h2so4 đặc nóng thu được khí so2 ( đktc ) tính khối lượng muối tạo thành Bài 4 : hoà tan hoàn toàn 18,4g hỗn hợp X gồm Fe và Mg bằng dung dịch HCl 0,8M (vừa đủ) sau phản ứng thu được 11,2 lít khí (đktc) a. Tính thành phần phần trăm khối lượng mỗi kim loại có trong hỗn hợp b. Tính thể tích dung dịch HCl đã dùng Giúp e vs ạ 🤗
Bài 3 :
a) $Mg + H_2SO_4 \to MgSO_4 + H_2$
$n_{Mg} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$\%m_{Mg} = \dfrac{0,15.24}{13,2}.100\% = 27,27\%$
$\%m_{Cu} = 100\% -27,27\% = 72,73\%$
b) $n_{Cu} = \dfrac{13,2 - 0,15.24}{64}= 0,15(mol)$
$\Rightarrow m_{muối} = 0,15.120 + 0,15.160= 42(gam)$
Đúng 2
Bình luận (0)
Bài 4 :
Gọi $n_{Fe} = a(mol) ; n_{Mg} = b(mol)$
$56a + 24b = 18,4(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
Theo PTHH : $n_{H_2} = a + b = \dfrac{11,2}{22,4} = 0,5(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,3
$\%m_{Fe} = \dfrac{0,2.56}{18,4}.100\% = 60,87\%$
$\%m_{Mg} = 100\% -60,87\% = 39,13\%$
b) $n_{HCl} = 2n_{H_2} = 1(mol)$
$V_{dd\ HCl} = \dfrac{1}{0,8}= 1,25(lít)$
Đúng 2
Bình luận (0)
3a) \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(n_{H_2}=n_{Mg}=0,15\left(mol\right)\)
=> \(\%m_{Mg}=\dfrac{0,15.24}{13,2}.100=27,28\%\)
\(\%m_{Cu}=100-27,28=72,73\%\)
b) \(n_{Cu}=\dfrac{13,2-3,6}{64}=0,15\left(mol\right)\)
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
0,15------------------->0,15
Mg + 2H2SO4 → MgSO4 + SO2 + 2H2O
0,15------------------->0,15
\(m_{muối}=0,15.160+0,15.120=42\left(g\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
1.cho 17,6g hỗn hợp A gồm Fe và Cu tác dụng với dung dịch h2so4 dư sau phản ứng thu được 4,48 lít khí h2 ( đktc)a. Tính khối lượng của từng kim loại trong hỗn hợp ban đầu b. Tính phần trăm khối lượng của từng kim loại trong hỗn hợp ban đầuc. Nếu cho hỗn kim loại trên vào dung dịch h2so4 đặc dư nóng thu được khí so2( đktc) tính khối lượng muối tạo thành 2. hòa tan hoàn toàn 27,6g hỗn hợp gồm Fe Fe2o3 Fe3o4 vào lượng dư dung dịch h2so4 98% ( đun nóng) sau phản ứng thu được dung dịch X và 5,04 lít...
Đọc tiếp
1.cho 17,6g hỗn hợp A gồm Fe và Cu tác dụng với dung dịch h2so4 dư sau phản ứng thu được 4,48 lít khí h2 ( đktc)
a. Tính khối lượng của từng kim loại trong hỗn hợp ban đầu
b. Tính phần trăm khối lượng của từng kim loại trong hỗn hợp ban đầu
c. Nếu cho hỗn kim loại trên vào dung dịch h2so4 đặc dư nóng thu được khí so2( đktc) tính khối lượng muối tạo thành
2. hòa tan hoàn toàn 27,6g hỗn hợp gồm Fe Fe2o3 Fe3o4 vào lượng dư dung dịch h2so4 98% ( đun nóng) sau phản ứng thu được dung dịch X và 5,04 lít khí so2 ( sản phẩm khử duy nhất, đo ở đktc ) tính khối lượng muối tan có trong dung dịch X
mong mọi người giúp vs ạ
Bài 1:
a+b) PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{Fe}\)
\(\Rightarrow m_{Fe}=0,2\cdot56=11,2\left(g\right)\) \(\Rightarrow m_{Cu}=6,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{11,2}{17,6}\cdot100\%\approx63,64\%\\\%m_{Cu}=36,36\%\end{matrix}\right.\)
c) Ta có: \(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
Bảo toàn nguyên tố: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)=n_{CuSO_4}\)
\(\Rightarrow m_{muối}=0,1\cdot400+0,1\cdot160=56\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 2:
Quy đổi hh gồm Fe (a mol) và O (b mol)
\(\Rightarrow56a+16b=27,6\) (1)
Ta có: \(n_{SO_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
Bảo toàn electron: \(3n_{Fe}=2n_O+2n_{SO_2}\) \(\Rightarrow3a-2b=0,45\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,39\\b=0,36\end{matrix}\right.\)
Bảo toàn nguyên tố: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,195\left(mol\right)\) \(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,195\cdot400=78\left(g\right)\)
Đúng 1
Bình luận (0)