Cho m gam hh gồm Al và Fe tác dụng hoàn toàn với dd H2SO4 loãng thu được 3,92 lít khí (đkc). Nếu cho m gam hh trên tác dụng với dd H2SO4 đặc nóng thì thu được 5,04 lít khí (đkc). Tìm giá trị của m ?

Những câu hỏi liên quan
Hoà tan hoàn toàn m (gam) hỗn hợp Al và Cu vào dd HNO3 loãng đủ thu được 3,9664 lít khí không màu hoá nâu trong không khí thoát ra và dd X. Nếu cũng cho m (gam) hh trên tác dụng với dd H2SO4 loãng thu được 2,9748 lít khí thoát ra (các khí đều đo ở đkc). Tính m gam hỗn hợp.
Td với H2SO4:
\(n_{H_2}=\dfrac{2,9748}{24,79}=0,12mol\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{Al}=\dfrac{0,12.2}{3}=0,08mol\)
Td với HNO3:
\(n_{Al}=a=0,08mol\\ n_{Cu}=b\)
Khí hoá nâu trong không khí → NO
\(n_{NO}=\dfrac{3,664}{24,79}=0,16mol\\ 3Cu+8HNO_3\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\\ Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\)
\(\Rightarrow a+\dfrac{2}{3}b=0,16\\ \Leftrightarrow0,08+\dfrac{2}{3}b=0,16\\ \Leftrightarrow b=0,12mol\\ \Rightarrow m=0,08.27+0,12.64=9,84g\)
Đúng 3
Bình luận (0)
Hh X gồm Fe,Cu,Ag.Chia 110,4g X thành 3 phần bằng nhau.Cho phần 1 tác dụng với Cl2 dư,thu đc m gam chất rắn.Phần 2 cho tác dụng với dd H2SO4 loãng dư thu được 2,24 lít khí H2 đktc.Hòa tan phần 3 trong 120g dd H2SO4 98% đun nóng thu được dd Y và 8,96 lít khí SO2 đktc a)Tính m b)Tính C% các chất trong dd Y
Hh X gồm Fe,Cu,Ag.Chia 110,4g X thành 3 phần bằng nhau.Cho phần 1 tác dụng với Cl2 dư,thu đc m gam chất rắn.Phần 2 cho tác dụng với dd H2SO4 loãng dư thu được 2,24 lít khí H2 đktc.Hòa tan phần 3 trong 120g dd H2SO4 98% đun nóng thu được dd Y và 8,96 lít khí SO2 đktc a)Tính m b)Tính C% các chất trong dd Y
41. Hoà tan 24,8g hh X gồm Fe, Mg, Cu trong dd H2SO4 đặc, nóng dư thu được dd A. Cô cạn dd A thu được 132 g muối khan. Nếu cho 24,8 g X tác dụng với dd HCl dư thu được 11,2 lít khí (đkc).
a. Viết phương trình phản ứng b. Tính % khối lượng mỗi kim loại trong hh X.
Gọi x, y, z là số mol Fe, Mg, Cu
=> \(56x+24y+64z=24,8\) (1)
X+ H2SO4 đặc nóng
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Mg + 2H2SO4→ MgSO4 + SO2↑ + 2H2O.
Cu + 2H2SO4→ CuSO4 + SO2↑ + 2H2O.
Các muối là \(Fe_2\left(SO_4\right)_3,MgSO_4,CuSO_4\)
=> \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{n_{Fe}}{2}=\dfrac{x.}{2};n_{MgCl_2}=n_{Mg}=y;n_{CuCl_2}=n_{Cu}=z\)
=> \(\dfrac{400x}{2}+120y+160z=132\) (2)
X + HCl dư thu được khí là H2
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
=> x+y=0,5 (mol) (3)
Từ (1), (2), (3) => x, y ,z
Xem lại đề vì hệ vô nghiệm
Đúng 2
Bình luận (1)
Hòa tan m gam Fe trong dung dịch H2SO4 loãng thì sinh ra 3,36 lít khí (đktc). Nếu cho m gam Fe tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít khí SO2 (đktc). Giá trị của V là A. 10,08. B. 5,04. C. 3,36. C. 3,36.
Đọc tiếp
Hòa tan m gam Fe trong dung dịch H2SO4 loãng thì sinh ra 3,36 lít khí (đktc). Nếu cho m gam Fe tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít khí SO2 (đktc). Giá trị của V là
A. 10,08.
B. 5,04.
C. 3,36.
C. 3,36.
Đáp án B
Xét giai đoạn m gam Fe tác dụng với dung dịch H2SO4 loãng:
Sơ đồ phản ứng :
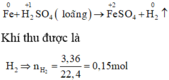
Các quá trình nhường, nhận electron :
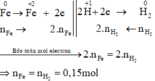
Xét giai đoạn m gam Fe tác dụng với H2SO4 đặc, nóng , dư:
Sơ đồ phản ứng:
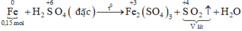
Các quá trình nhường, nhận electron:
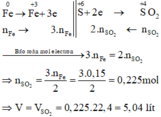
Đúng 0
Bình luận (0)
hoà tan m gam hỗn hợp Cu và Zn vào dd H2SO4 loãng dư thu được dd X, một kim loại khong tan, và 2,479 lít khí (đkc). Lấy toàn bộ lượng kim loại không tan thu được cho hoà tan vào x gam dd H2SO4 đặc nóng 98% thấy thu được 2,9748 lít khí SO2 (đkc) (sản phẩm khử duy nhất) a)PTHH b)tính m,x
a, \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
\(n_{Zn}=n_{H_2}=0,1\left(mol\right)\)
\(n_{SO_2}=\dfrac{2,9748}{24,79}=0,12\left(mol\right)\)
\(n_{Cu}=n_{SO_2}=0,12\left(mol\right)\)
\(\Rightarrow m=m_{Zn}+m_{Cu}=0,1.65+0,12.64=14,18\left(g\right)\)
Có: \(n_{H_2SO_{4\left(đ\right)}}=2n_{SO_2}=0,24\left(mol\right)\Rightarrow x=m_{ddH_2SO_4\left(đ\right)}=\dfrac{0,24.98}{98\%}=24\left(g\right)\)
Đúng 3
Bình luận (0)
32. Cho 10,38 g hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:
- Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lít khi (đkc).
- Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lít khí SO2 (đkc).
Tính khối lượng từng kim loại trong hỗn hợp ban đầu.
mFe=3,36 g; mAl=2,7 g; mAg=4,32 g
Giải thích các bước giải:
Gọi số mol Fe, Al, Ag trong mỗi phần là x, y, z.
P1: có Fe, Al phản ứng
nH2=0,105 mol; nSO2=0,13 mol
PTHH:
Fe+H2SO4→FeSO4+H2
2Al+3H2SO4→Al2(SO4)3+3H2
⇒3x/2+3y/2+z/2=0,13 (2)
mà 56x+27y+108z=10,38:2 (3)
Từ (1),(2),(3) ⇒x=0,03; y=0,05; z=0,02 mol
Khi đó: mFe=2.56.0,03=3,36 g; mAl=2.27.0,05=2,7 g
mAg=2.108.0,02=4,32 g
Đúng 0
Bình luận (0)
Vì phần 1 tác dụng với H2SO4 loãng => sinh ra khí H2
=> n H2 = 0,105 ( mol )
Có: n SO2 = 0,13 ( mol )
Gọi n Fe, n AL, n Ag ở mỗi phần lần lượt là a, b, c
Vì m Fe + m Al + m Ag = 10,38
=> 56a + 27b + 108c = 10,38 : 2 = 5,19 ( 1 )
PTHH của phần 1
Fe + H2SO4 ====> FeSO4 + H2
2Al + 3H2SO4 =====> Al2(SO4)3 + 3H2
theo pthh: a+ 1,5b = 0,105 ( mol ) ( 2 )
PTHH của phần 2
2Fe + 6H2SO4 =====> Fe2(SO4)3 + 3SO2 + 6H2O
2AL + 6H2SO4 ===> Al2(SO4)3 + 3SO2 + 6H2O
2Ag + 2H2SO4 =====> Ag2SO4 + SO2 + 2H2O
theo PTHH: 1,5a + 1,5b + 0,5c = 0,13 ( 3 )
từ ( 1 ) , (2) và (3) suy ra
a = 0,03 ( mol ) => m Fe = 3,36 ( g )
b = 0,05 ( mol ) => m Al = 2,7 ( g )
c = 0,02 ( mol ) => m Ag = 4,32 ( g )
Đúng 0
Bình luận (0)
42. Cho 8,3 g hỗn hợp A gồm 3 kim loại Đồng, Nhôm và Magiê tác dụng vừa đủ với dd H2SO4 20% (loãng). Sau phản ứng còn chất không tan B và thu được 5,6 lít khí (đkc). Hoà tan hoàn toàn B trong H2SO4 đđ, nóng, dư; thu được 1,12 lít khí SO2 (đkc).a. Tính % số mol mỗi kim loại trong hỗn hợp A.b. Tính C% các chất có trong dung dịch B, biết lượng H2SO4 phản ứng là vừa đủ.c. Dẫn toàn bộ khí SO2 ở trên vào dd Ca(OH)2 sau một thời gian thu được 3 g kết tủa và dd D. Lọc bỏ kết tủa cho Ca(OH...
Đọc tiếp
42. Cho 8,3 g hỗn hợp A gồm 3 kim loại Đồng, Nhôm và Magiê tác dụng vừa đủ với dd H2SO4 20% (loãng). Sau phản ứng còn chất không tan B và thu được 5,6 lít khí (đkc). Hoà tan hoàn toàn B trong H2SO4 đđ, nóng, dư; thu được 1,12 lít khí SO2 (đkc).
a. Tính % số mol mỗi kim loại trong hỗn hợp A.
b. Tính C% các chất có trong dung dịch B, biết lượng H2SO4 phản ứng là vừa đủ.
c. Dẫn toàn bộ khí SO2 ở trên vào dd Ca(OH)2 sau một thời gian thu được 3 g kết tủa và dd D. Lọc bỏ kết tủa cho Ca(OH)2 đến dư vào dd D, tìm khối lượng kết tủa thu được.
cho 11,8 g hh X gồm cu và fe vào dd h2so4 loãng dư đến khi pu xảy ra hoàn toàn thì thu được 0,56(l) khí ở kdtc).Cũng lượng X trên cho vào dd h2so4 đặc nóng thì thu được V lít khí so2(dktc),dẫn lượng khí thu được vào 250ml dd naoh 1M,thu được 21,9g muối
a)tính thành phần % khối lượng mỗi kl trong hh ban đầu
b)Tính V
\(n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
\(n_{NaOH}=0,25.1=0,25\left(mol\right)\)
Cho X vào dung dịch `H_2SO_4` loãng:
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,025<-----------------------0,025
a. \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{56.0,025.100\%}{11,8}=11,86\%\\\%m_{Cu}=\dfrac{\left(11,8-0,025.56\right).100\%}{11,8}=88,14\%\end{matrix}\right.\)
b. \(n_{Cu}=\dfrac{11,8-0,025.56}{64}=0,1625\left(mol\right)\)
Cũng lượng X trên cho vào dung dịch `H_2SO_4` đặc nóng:
Giả sử Fe tác dụng hết với dung dịch \(H_2SO_{4.đn}\)
\(2Fe+6H_2SO_{4.đn}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,025----------------------------------->0,0375
\(Cu+2H_2SO_{4.đn}\rightarrow CuSO_4+SO_2+2H_2O\)
0,1625--------------------------->0,1625
\(\Sigma n_{SO_2}=0,0375+0,1625=0,2\left(mol\right)\)
Có: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,25}{0,2}=1,25\)
=> Phản ứng giữa `NaOH` và `SO_2` tạo muối axit trước (tỉ lệ 1:1)
\(SO_2+NaOH\rightarrow NaHSO_3\)
0,2---->0,2------->0,2
Xét \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\Rightarrow\) NaOH dư.
\(n_{NaOH.dư}=0,25-0,2=0,05\left(mol\right)\)
\(NaOH+NaHSO_3\rightarrow Na_2SO_3+H_2O\)
0,05----->0,05---------->0,05
Xét \(\dfrac{0,05}{1}< \dfrac{0,2}{1}\Rightarrow NaHSO_3.dư\)
Sau phản ứng thu được: \(\left\{{}\begin{matrix}n_{NaHSO_3}=0,2-0,05=0,15\left(mol\right)\\n_{Na_2SO_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(m_{muối}=0,15.104+0,05.126=21,9=m_{muối.thu.được.theo.đề}\)
=> Giả sử đúng.
\(\Rightarrow V=V_{SO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)



















