tính số g nc thu đc khi cho 8,4l khí H tác dụng với 2,8 l khi Ở (các thể tích khí đo ở đktc)

Những câu hỏi liên quan
tính số gam nước thu được khi cho 8,4 lít khí hidro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
\(n_{H_2}=\dfrac{8.4}{22,4}=0,375\left(mol\right)\)
\(n_{O_2}=\dfrac{2.8}{22,4}=0,125\left(mol\right)\)
PTHH : 2H2 + O2 -> 2H2O
0,125 0,25
Ta thấy : 0,375 > 0,125 => H2 dư , O2 đủ
\(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 4
Bình luận (0)
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{8,4}{22,4}=0,375mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{2,8}{22,4}=0,125mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,375 >0,125 ( mol )
0,125 0,25 ( mol )
\(m_{H_2O}=n_{H_2O}.M_{H_2O}=0,25.18=4,5g\)
Đúng 2
Bình luận (1)
Bài tập 1: Tính số gam nước thu được khi cho 2,24lít khí Hiđrô tác dụng với 2,8 lít khí ôxi. ( Các thể tích khí đo ở đktc)
PTHH: \(4H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{4}< \dfrac{0,125}{1}\) \(\Rightarrow\) Oxi còn dư, Hidro p/ứ hết
\(\Rightarrow n_{H_2O}=0,05\left(mol\right)\) \(\Rightarrow m_{H_2O}=0,05\cdot18=0,9\left(g\right)\)
Đúng 3
Bình luận (0)
Tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi (các thể tích đo ở đktc).
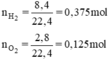
Phương trình hóa học của phản ứng tạo nước:
2H2 + O2 → 2H2O.
So sánh tỉ lệ 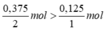 . Như vậy lượng H2 dư nên tính khối lượng nước sinh ra theo oxi.
. Như vậy lượng H2 dư nên tính khối lượng nước sinh ra theo oxi.
Theo phương trình trên ta có:
nH2O = 2. 0,125 = 0,25 mol.
mH2O = 0,25 .18 = 4,5g.
Đúng 0
Bình luận (0)
Bài 6 :tính số gam nước thu được khi cho 8,4 lít hidro tác dụng với 2,8 lít khí õi (các thể tích khí đo ở đktc )
GIúp mk với ạ :)))
\(n_{H_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,375}{2}>\dfrac{0,125}{2}\), ta được H2 dư.
Theo PT: \(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\Rightarrow m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 2
Bình luận (0)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 3
Bình luận (0)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 3
Bình luận (0)
Tính số gam nước thu được khi cho 8,4 lít khí H2 tác dụng với 2,8 lít khí O2 (các thể tích đo ở đktc).
PTHH: 2H2 + O2 -to-> 2H2O
Ta có: \(\dfrac{8,4}{2}>\dfrac{2,8}{1}\)
=> H2 dư, O2 hết nên tính theo \(V_{O_2}\)
Theo PTHH và đề bài, ta có:
\(m_{H_2O}=2.\dfrac{2,8}{22,4}.18=4,5\left(g\right)\)
Đúng 0
Bình luận (1)
PTHH 2H2 + O2 -t0-> 2H2O
2mol 1mol 2mol
2V(lit) V(lit)
Ta thấy thể tích H2 lớn hơn 2 lần thể tích Oxi, do đó H2 dư nên ta tính số gam nước theo số mol oxi
Theo PTHH ta có nH2=nH2O
nH2O= 2,8 . 2 :22,4 = 0,25 (mol)
Vậy mH2O= 0,25 . 18 =4,5 (gam)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Tính số gam nước thu được khi cho 8,96 lít khí hiđro tác dụng với 5,6 lít oxi (các thể tích đo ở đktc).
nH2 = V/22,4 = 8,96/22,4 = 0,4 (mol)
nO2 = V/22,4 = 5,6/22,4 = 0,25 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Ta có: 0,4/2 < 0,25/1
=> O2 dư
Theo PTHH: nH2O = nH2 = 0,4 (mol)
=> mH2O = n.M = 0,4 . 18 = 7,2(g)
Đúng 2
Bình luận (0)
Tính tổng số gam nước thu được khi cho 8,4 lít khí h2 tác dụng với 2,8 lít khí oxygen ( các khí đo ở đkc)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\\ Vì:\dfrac{8,4}{2}>\dfrac{2,8}{1}\Rightarrow O_2hết,H_2dư\\ n_{H_2O}=2n_{O_2}=2.\dfrac{2,8}{24}=\dfrac{7}{30}\left(mol\right)\\ m_{H_2O}=\dfrac{7}{30}.18=4,2\left(g\right)\)
Đúng 1
Bình luận (0)
Khi cho 100 g hợp kim gồm có Fe, Cr và Al tác dụng với lượng dư dung dịch NaOH thu được 6,72 lít khí. Lấy bã rắn không tan cho tác dụng một lượng dư dung dịch HCl (khi không có không khí) thu 38,08 lít khí. Các thể tích đo ở đktc. Xác định thành phần % của hợp kim.
Với NaOH dư, Fe, Cr không phản ứng
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\\\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\\ \Rightarrow \%m_{Al}=\dfrac{0,2.27}{100}=5,4\%\)
Phần không tan cho tác dụng một lượng dư dung dịch HCl
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ Cr+2HCl\rightarrow CrCl_2+H_2\\ Đặt:\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cr}=y\left(mol\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}56x+52y=100-5,4=94,6\left(g\right)\\x+y=\dfrac{38,08}{22,4}=1,7\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=1,55\\y=0,15\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=86,8\\\%m_{Cr}=7,8\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)