1 hỗn hợp gồm 1 ankin và H2 có V =8,96 (l) và mx=4,6 g.cho hỗn hợp X qua Ni nóng phản ứng hoàn toàn cho ra 1 hỗn hợp khí Y có tỷ khối so vs hỗn hợp X =2.Số mol H2 phản ứng,khối lượng và CTPT của ankin là:

Những câu hỏi liên quan
Hỗn hợp X gồm ankin Y và H2 có tỉ lệ mol là 1:2. Dẫn 13,44 lít hỗn hợp X (đktc) qua Ni, nung nóng thu được hỗn hợp Z có tỉ khối so với H2 là 11. Dẫn hỗn hợp Z qua dung dịch Br2 dư, sau phản ứng hoàn toàn thấy có 32 gam Br2 đã phản ứng. Công thức của ankin Y là: A. C4H6 B. C5H8 C. C3H4 D. C2H2
Đọc tiếp
Hỗn hợp X gồm ankin Y và H2 có tỉ lệ mol là 1:2. Dẫn 13,44 lít hỗn hợp X (đktc) qua Ni, nung nóng thu được hỗn hợp Z có tỉ khối so với H2 là 11. Dẫn hỗn hợp Z qua dung dịch Br2 dư, sau phản ứng hoàn toàn thấy có 32 gam Br2 đã phản ứng. Công thức của ankin Y là:
A. C4H6
B. C5H8
C. C3H4
D. C2H2
Chọn C.
X có nY = 0,2mol và nH2 = 0,4 mol . Dẫn hỗn hợp Z qua dung dịch Br2 dư, sau phản ứng hoàn toàn thấy có 0,2 mol Br2 đã phản ứng = số mol Y ban đầu
→ Z có 0,2 mol anken và 0,2 mol H2(H2 chỉ hidro hóa ankin thành anken)
→ mZ = 0,4. M = 0,2.Manken + 0,2.MH2 → Manken= 42g → anken là C3H6
→ Y là C3H4
Đúng 0
Bình luận (0)
Hỗn hợp H chứa 4,48 lit (đktc) hỗn hợp khí gồm H2, anken X và ankin Y. Nung nóng H với Ni để phản ứng xẩy ra hoàn toàn thu được hỗn hợp khí T. Biết tỉ khối của hỗn hợp T so với hỗn hợp H là 4/3. Số mol H2 dư sau phản ứng là A. 0,175. B. 0,12. C. 0,05. D. 0,09.
Đọc tiếp
Hỗn hợp H chứa 4,48 lit (đktc) hỗn hợp khí gồm H2, anken X và ankin Y. Nung nóng H với Ni để phản ứng xẩy ra hoàn toàn thu được hỗn hợp khí T. Biết tỉ khối của hỗn hợp T so với hỗn hợp H là 4/3. Số mol H2 dư sau phản ứng là
A. 0,175.
B. 0,12.
C. 0,05.
D. 0,09.
B
Có mH = mT → 0,2. MH = nT. MT → nT = 0,2. 3/4= 0,15 mol
Có nH2 pư = nH - nT = 0,2 - 0,15 = 0,05 mol
Có nX + 2nY = 0,05 → nX + nY < 0,05 → 0,2 > nH2 ban đầu > 0,2 - 0,05 = 0,15 mol
0,2 - 0,05> nH2 dư > 0,15- 0,05 → 0,15> nH2 dư > 0,1
Vậy chỉ có B thỏa mãn. Đáp án B
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm 0,5 mol H2 và 0,3 mol ankin X. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 16,25. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 32 gam. Ankin X là A. Axetilen. B. Pent-2-in. C. But-1-in. D. Propin.
Đọc tiếp
Hỗn hợp khí A gồm 0,5 mol H2 và 0,3 mol ankin X. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 16,25. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 32 gam. Ankin X là
A. Axetilen.
B. Pent-2-in.
C. But-1-in.
D. Propin.
Đáp án D
Với nAnkin = 0,3 ⇒ Số mol H2 pứ tối đa = 2nAnkin = 0,6 mol.
Bảo toàn số mol liên kết π ta có: nH2 pứ + nBr2 = 0,6 mol.
⇒ nH2 pứ = 0,6 – 0,2 = 0,4 mol ⇒ nH2 dư = 0,1 mol.
⇒ Số mol của B sau phản ứng = nH2 dư + nAnkin = 0,4 mol.
⇒ mB = mA = nHỗn hợp B × MHỗn hợp B = 0,4×16,25×2 = 13 gam
Vậy mH2 ban đầu + mAnkin ban đầu = 13 gam. =>0,5×2 + 0,3×MAnkin = 13.
=> MAnkin = 40 ⇒ Ankin đó là Propin
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm 0,5 mol H2 và 0,3 mol ankin X. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 16,25. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 32 gam. Ankin X là A. Axetilen B. Pent-2-in C. But-1-in D. Propin
Đọc tiếp
Hỗn hợp khí A gồm 0,5 mol H2 và 0,3 mol ankin X. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 16,25. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 32 gam. Ankin X là
A. Axetilen
B. Pent-2-in
C. But-1-in
D. Propin
Đáp án D
Với nAnkin = 0,3
⇒ Số mol H2 pứ tối đa
= 2nAnkin = 0,6 mol.
Bảo toàn số mol liên kết π ta có:
nH2 pứ + nBr2 = 0,6 mol.
⇒ nH2 pứ = 0,6 – 0,2 = 0,4 mol
⇒ nH2 dư = 0,1 mol.
⇒ Số mol của B sau phản ứng
= nH2 dư + nAnkin = 0,4 mol.
⇒ mB = mA = nHỗn hợp B × MHỗn hợp B
= 0,4×16,25×2 = 13 gam
Vậy:
mH2 ban đầu + mAnkin ban đầu = 13 gam
Û 0,5×2 + 0,3×MAnkin = 13.
Û MAnkin = 40
⇒ Ankin đó là Propin
Đúng 0
Bình luận (0)
Hỗn hợp X gồm ankin Y và H2 có tỉ lệ mol là 1:2. Dẫn 13,44 lít hỗn hợp X (đktc) qua Ni, nung nóng thu được hỗn hợp Z có tỉ khối so với H2 là 11. Dẫn hỗn hợp Z qua dung dịch Br2 dư, sau phản ứng hoàn toàn thấy có 32g Br2 đã phản ứng. Tìm công thức ankin Y
0,6 mol X gồm : \(\left\{{}\begin{matrix}C_nH_{2n-2}:x\left(mol\right)\\H_2:2x\left(mol\right)\end{matrix}\right.\)
=> x + 2x = 0,6 => x = 0,2
Vậy: \(\left\{{}\begin{matrix}C_nH_{2n-2}:0,2\left(mol\right)\\H_2:0,4\left(mol\right)\end{matrix}\right.\)
Z có phản ứng với Br2 -> Z có anken
nBr2 = 0,2 (mol)
\(C_nH_{2n-2}+H_2\rightarrow C_nH_{2n}\)
0,2 ........... 0,2 ...... 0,2 (mol)
\(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
0,2 ......... 0,2 ...... 0,2 (mol)
Vậy Z gồm: \(\left\{{}\begin{matrix}H_2dư:0,4-0,2=0,2\left(mol\right)\\C_nH_{2n}:0,2\left(mol\right)\end{matrix}\right.\)
dZ/H2 = 11 => MZ = 22
Ta có:
\(\dfrac{0,2.2+0,2.14n}{0,2+0,2}=22\)
\(\Rightarrow n=3\)
\(Y:C_3H_4\)
Đúng 0
Bình luận (0)
Một hỗn hợp khí M gồm ankin X và H2 có tỉ khối hơi so với CH4 là 0,6. Nung nóng hỗn hợp M với bột Ni để phản ứng xảy ra hoàn toàn thu được hỗn hợp khí N có tỉ khối hơi so với CH4 là 1,0. Ankin X là A. axetilen. B. metylaxetilen. C. etylaxetilen. D. propylaxetilen.
Đọc tiếp
Một hỗn hợp khí M gồm ankin X và H2 có tỉ khối hơi so với CH4 là 0,6. Nung nóng hỗn hợp M với bột Ni để phản ứng xảy ra hoàn toàn thu được hỗn hợp khí N có tỉ khối hơi so với CH4 là 1,0. Ankin X là
A. axetilen.
B. metylaxetilen.
C. etylaxetilen.
D. propylaxetilen.
Đáp án B
hhM gồm CnH2n - 2 và H2 có dM/CH4 = 0,6.
Nung M với Ni → hhN có N/CH4 = 1.
• Ta có hhN có M = 16 → H2 dư.
Đặt nCnH2n - 2 x mol và H2 y mol.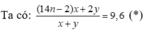
Vì phản ứng xảy ra hoàn toàn → hhN gồm CnH2n + 2 x mol và H2 dư (y - 2x) mol.![]()
Từ (*), (**) → y = 4x → n = 3 → CH≡C-CH3 → metylaxetilen
Đúng 0
Bình luận (0)
Hỗn hợp X gồm ankin và H2 có tỷ lệ mol 1: 1. Cho 8,96 lít hỗn hợp X qua Ni nung nóng thu được 6,72 lít hỗn hợp Y. Cho Y vào dung dịch Br2 dư. Xác định số mol Br2 đã phản ứng:
A. 0,4 mol B. 0,3 mol C. 0,2 mol D. 0,1 mol
\(\left\{{}\begin{matrix}n_{C_nH_{2n-2}}+n_{H_2}=\dfrac{8,96}{22,4}=0,4\\n_{C_nH_{2n-2}}=n_{H_2}\end{matrix}\right.\)
=> \(n_{C_nH_{2n-2}}=n_{H_2}=0,2\left(mol\right)\)
\(n_{H_2\left(pư\right)}=0,4-\dfrac{6,72}{22,4}=0,1\left(mol\right)\)
Bảo toàn liên kết: \(2.n_{C_nH_{2n-2}}=n_{H_2\left(pư\right)}+n_{Br_2}\)
=> \(n_{Br_2}=0,3\left(mol\right)\)
=> B
Đúng 2
Bình luận (0)
Hỗn hợp X gồm ankin Y và H2 có tỉ khối so với H2 là 6,7. Dẫn X đi qua bột Ni nung nóng cho đến khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp Z có tỉ khối so với H2 là 16,75. Công thức phân tử của Y là: A. C2H2 B. C5H8 C. C3H4 D. C4H6
Đọc tiếp
Hỗn hợp X gồm ankin Y và H2 có tỉ khối so với H2 là 6,7. Dẫn X đi qua bột Ni nung nóng cho đến khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp Z có tỉ khối so với H2 là 16,75. Công thức phân tử của Y là:
A. C2H2
B. C5H8
C. C3H4
D. C4H6
Hỗn hợp X gồm ankin Y và H2 có tỉ khối so với H2 là 6,7. Dẫn X đi qua bột Ni nung nóng cho đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Z có tỉ khối so với H2 là 16,75. Công thức phân tử của Y là A.C4H6. B. C5H8. C.C3H4. D.C2H2.
Đọc tiếp
Hỗn hợp X gồm ankin Y và H2 có tỉ khối so với H2 là 6,7. Dẫn X đi qua bột Ni nung nóng cho đến khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp Z có tỉ khối so với H2 là 16,75. Công thức phân tử của Y là
A.C4H6.
B. C5H8.
C.C3H4.
D.C2H2.
M ¯ z = 16 , 75 . 2 = 33 , 5 , nên có 2 trường hợp có thể xảy ra (do phản ứng xảy ra hoàn toàn):
+ TH1: Nếu ankin dư, H2 hết thì ankin phải có khối lượng mol nhỏ hơn 33,5 và ankan tương ứng phải có khối lượng mol lớn hơn 33,5.
Khi đó không có ankin nào thỏa mãn
+ TH2: Nếu ankin hết và H2 dư thì hỗn hợp Z gồm H2 và ankan CnH2n+2. Chọn 1 mol hỗn hợp X ban đầu thì mX = mZ = 6,7.2 = 13,4 ⇒ nZ = 0,4 ⇒ n H 2 ( p h ả n ứ n g ) = 0 , 6
⇒ n a n k a n = n H 2 ( p h ả n ứ n g ) . 0 , 5 = 0 , 3
⇒ Z chứa 0,1 mol H2 nên 0,1.2+0,3(14n+2) = 13,4
Tìm được n = 3 khi đó ankin cần tìm là C3H4.
Đáp án C
Đúng 0
Bình luận (0)









