Bài 2 Cho 12g Fe và 10g dung dịch chứa Axit clohidric .Tìm khối lượng sao phản ứng

Những câu hỏi liên quan
Cho Ag Fe và Bg dung dịch chứa Axit clohidric .Tìm khối lượng sao phản ứng
Bài 1 Đốt 11.2l Hidro thì thể tích oxi cần dùng là bao nhiêu (các khí đều đo ở đktc)
Bài 2 Cho 12g Fe và 10g dung dịch chứa Axit clohidric .Tìm khối lượng sao phnr ứng
Bài 3 Dẫn luồng khí h2 dư đi qua các ống mức nối tiếp đựng các chất sau CuO,Zno,Fe2O3,Na2O,PbO,CaO,Fe3O4,Ag2O Viết các phương trình phản ứng xảy ra
Câu 1:
Khi đốt khí H2 trong O2 thì:
\(PTHH: 2H2+O2-t^o->2H2O\)
Ta có : \(nH2 (đktc) = \dfrac{11,2}{22,4} = 0,5 (mol)\)
Theo PTHH: nO2 cần dùng = \(\dfrac{1}{2}.nH2 = 0,25 (mol)\)
Vậy thể tích khí O2 cần dùng (đktc) là:
\(V_O2 = nO2.22,4 = 0,25.22,4 =5.6 (l)\)
Đúng 0
Bình luận (0)
Bài 3: Các phương trình hóa học xảy ra:
\(CuO + H2-t^o-> Cu+H2O\)
\(ZnO + H2-t^o->Zn + H2O\)
\(Fe2O3+3H2-t^o-> 2Fe+3H2O\)
\(PbO +H2-t^o->Pb+H2O\)
\(Fe3O4+4H2(dư)-t^o->3Fe+4H2O\)
\(Ag_2O+H_2-t^o-2Ag +H_2O\)
Đúng 0
Bình luận (0)
Câu 2 là tìm khối lượng gì sau phản ứng vậy bạn?
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Cho 2,7 gam hỗn hợp bột X gồm Fe và Zn tác dụng với dung dịch CuSO4. Sau một thời gian, thu được dung dịch Y và 2,84 gam chất rắn Z. Cho toàn bộ Z vào dung dịch H2SO4 (loãng, dư). Sau khi các phản ứng kết thúc thì khối lượng chất rắn giảm 0,28 gam và dung dịch thu được chỉ chứa một muối duy nhất. Phần trăm khối lượng của Fe trong X là: A. 58,52% B. 51,85% C. 48,15% D. 41,48%
Đọc tiếp
Cho 2,7 gam hỗn hợp bột X gồm Fe và Zn tác dụng với dung dịch CuSO4. Sau một thời gian, thu được dung dịch Y và 2,84 gam chất rắn Z. Cho toàn bộ Z vào dung dịch H2SO4 (loãng, dư). Sau khi các phản ứng kết thúc thì khối lượng chất rắn giảm 0,28 gam và dung dịch thu được chỉ chứa một muối duy nhất. Phần trăm khối lượng của Fe trong X là:
A. 58,52%
B. 51,85%
C. 48,15%
D. 41,48%
Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
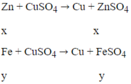
Ta có hệ:
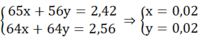
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Cu và Fe có tỉ lệ khối lượng tương ứng là 7 : 3. Lấy m gam X phản ứng hoàn toàn với dung dịch chứa 0,7 mol HNO3. Sau phản ứng còn lại 0,75m gam chất rắn và có 0,25 mol khí Y gồm NO và NO2. Giá trị của m là:
A. 40,5
B. 50,4
C. 50,2
D. 50
Đáp án B
Ta có:
![]()
mCu = 0,7m (g)
Vì Fe phản ứng trước Cu và sau khi phản ứng còn 0,75m (g) chất rắn → Cu chưa phản ứng 0,7m
Fe dư 0,75m - 0,7m = 0,05m → mFe pư = 0,2m - 0,05m = 0,25m (g)
Fe dư → Chỉ tạo muối Fe(NO3)2
HNO3 hết (Lưu ý chỉ H+ hết, NO3- còn trong muối).
Quá trình nhường electron:

Quá trình nhận electron:
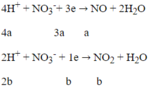
Áp dụng định luật bảo toàn electron:
![]()
→ m = 50,4
Đúng 0
Bình luận (0)
Cho 1 lượng bột Al phản ứng vừa đủ với dung dịch có chứa 44,1g H2so4 ,thu được muối Al2(so4)3 Và Khí H2.
A)tính Khối Lượng Al Phản Ứng
B)tính Thể Tích Khí H2( ở Đktc)
C)tính Khối Lượng AL2(So4)3 Theo 2 Cách
a) $n_{H_2SO_4} = \dfrac{44,1}{98} = 0,45(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
Theo PTHH :
$n_{Al} = \dfrac{2}{3}n_{H_2SO_4} = 0,3(mol)$
$m_{Al} = 0,3.27 = 8,1(gam)$
b) $n_{H_2} = n_{H_2SO_4} = 0,45(mol)$
$\Rightarrow V_{H_2} = 0,45.22,4 =1 0,08(lít)$
c)
Cách 1 : $n_{Al_2(SO_4)_3} = \dfrac{1}{3}n_{H_2SO_4} = 0,15(mol)$
$\Rightarrow m_{Al_2(SO_4)_3} = 0,15.342 = 51,3(gam)$
Cách 2 : Bảo toàn khối lượng, $m_{Al_2(SO_4)_3} = 8,1 + 44,1 - 0,45.2 = 51,3(gam)$
Đúng 2
Bình luận (0)
Bài 1: Cho 5,6g iron tác dụng với dung dịch hydrochloric acid sinh ra 0,2g khí hydrogen và 205g muối iron (II) chloride FeCl2.
1. Dấu hiệu xảy ra phản ứng.
2. Viết phương trình chữ của phản ứng trên
3. Tính khối lượng dung dịch hydrochloric acid đã dùng.
4. Lập PTHH phản ứng trên.
a. Iron tan dần, có khí không màu thoát ra
b. Iron + hydrochloric acid → iron (II) chloride + khí hydrogen
c.
Bảo toàn khối lượng :
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{HCl}=205+0.2-5.6=199.6\left(g\right)\)
d.
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Đúng 1
Bình luận (0)
Cho 0,02 mol Fe vào dung dịch chứa 0,045 mol AgNO3. Khi phản ứng xảy ra hoàn toàn thì khối lượng Ag thu được là:
A. 4,32
B. 2,16
C. 1,08
D. 4,86
Đáp án D
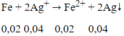
⇒ nAg+ dư = 0,045 - 0,04 = 0,005 mol. Khi đó xảy ra phản ứng:
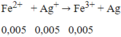
⇒ mAg = (0,04 + 0,005).108 = 4,86g
Đúng 0
Bình luận (0)
Hòa tan kim loại Fe vào dung dịch HCL 20%.Phản ứng vừa đủ thu được 14,874 lit Hydrogen(đktc) 25°C , 1 bar.Tính khối lượng kim loại Fe phản ứng ? a.Tính khối lượng dung dịch HCL 20% phản ứng ? b. Tính nồng độ % dung dịch sau phản ứng? c.Tính số ml dd Ca(OH)2 3M cần để trung hòa lượng acid HCl trên
Hòa tan kim loại Fe vào dung dịch HCL 20%.Phản ứng vừa đủ thu được 14,874 lit Hydrogen(đktc) 25°C , 1 bar.Tính khối lượng kim loại Fe phản ứng ?
a.Tính khối lượng dung dịch HCL 20% phản ứng ?
b. Tính nồng độ % dung dịch sau phản ứng?
c.Tính số ml dd Ca(OH)2 3M cần để trung hòa lượng acid HCl trên
giúp mình vs ạ














