Tỷ số a/b trong phương trình hóa học sau là bao nhiêu?
aFe + bH2SO4 → Fe2(SO4)3 + SO2↑ + H2O
A. 1/2
B. 1/3
C. 1/4
D. 1/5
Cho phương trình hóa học :
aFe + bH2SO4 ->cFe2(SO4)3 + dSO2 + eH2O. Tỷ lệ a : b là :
A. 1 : 3
B. 1 : 2
C. 2 : 3
D. 2 : 9
Chọn A
2Fe + 6H2SO4 -> Fe2(SO4)3 + 3SO2 + 6H2O
1.Cho sơ đồ phản ứng aFe + bH2SO4 --> c Fe2(SO4)3 + d SO2 + e H2O. Hỏi sau khi cân bằng với hệ số nguyên tối giản thì tổng các hệ số (a +b) là bao nhiêu?
(1 Điểm)
8
6
4
10
2.Cho phản ứng Sắt + axit clohidric (HCl) --> Sắt (II) clorua + hidro
Iron + Hydrochloric acid (HCl) --> Iron (II) chloride + hydrogen
Hỏi sau khi cân bằng với hệ số nguyên tối giản thì hệ số của HCl là bao nhiêu?
(1 Điểm)
1
2
3
4
3.Cho phản ứng Sắt (III) oxit + axit sunfuric (H2SO4) --> Sắt (III) sunfat + nước
Iron (III) oxide + Sulfuric acid (H2SO4) --> Iron (III) sulfate + water
Hỏi sau khi cân bằng với hệ số nguyên tối giản thì hệ số của nước là bao nhiêu?
1
2
3
4
4.Cho sơ đồ phản ứng Fe2O3 + H2 --> Fe + H2O. Hỏi sau khi cân bằng với hệ số nguyên tối giản thì tổng các hệ số của chất sản phẩm phản ứng là bao nhiêu?
3
5
7
6
5.Cho sơ đồ phản ứng Al + HCl --> AlCl3 + H2. Hỏi sau khi cân bằng với hệ số nguyên tối giản thì tổng các hệ số của chất tham gia phản ứng là bao nhiêu?
3
6
9
8
1)
\(2Fe+6H_2SO_4->Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
=> a + b = 2 + 6 = 8 (A)
2) Fe + 2HCl --> FeCl2 + H2
=> B
3) Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
=> C
4) Fe2O3 + 3H2 --> 2Fe + 3H2O
=> B
5) 2Al + 6HCl --> 2AlCl3 + 3H2
=> D
Cho phương trình hóa học: aFe + bH2SO4 → cFe2(SO4)3 + dSO2 ↑ + eH2O
Tỉ lệ a : b là
A. 1 : 3.
B. 1 : 2.
C. 2 : 3.
D. 2 : 9.
Đáp án A
Quá trình oxi hóa - khử:
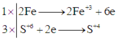
Kết quả
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
⇒ a : b = n Fe : N H 2 SO 4 = 1 : 3
Cho phương trình hóa học:
aFe + bH2SO4 → cFe2(SO4)3 + dSO2 ↑ + eH2O
Tỉ lệ a : b là:
A. 1 : 3.
B. 1 : 2.
C. 2 : 3.
D. 2 : 9.
Cho phương trình hóa học:
aFe + bH2SO4 → cFe2(SO4)3 + dSO2 ↑ + eH2O
Tỉ lệ a : b là
A. 1 : 3.
B. 1 : 2
C. 2 : 3
D. 2 : 9
Cho phương trình hóa học:
aFe + bH2SO4 → cFe2(SO4)3 + dSO2↑ +eH2O
Tỉ lệ a:b là
A. 1:3
B. 1:2
C. 2:3
D. 2:9
Quan sát phương trình phản ứng ta thấy Fe tăng từ mức oxi hóa 0 lên mức oxi hóa +3; S giảm từ mức oxi hóa +6 xuống mức oxi hóa +4 → Fe là chất khử và H2SO4 là chất oxi hóa.
2x F e 0 → F e 3 + + 3 e
3x 4 H + + S + 6 O 4 2 - + 2 e → S + 4 O 2 + 2 H 2 O
Suy ra phương trình phản ứng đã cân bằng như sau:
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ +6H2O
Chọn đáp án A
Giúp tôi
Bài 4: Cân bằng PTHH sau:
Mg + H2SO2 (đ, n) → MgSO4 + SO2 + H2O
Hỏi tổng hệ số các chất phản ứng là bao nhiêu?
A. 2
B. 3
C. 4
D. 5
Bài 5: Chọn hệ số và CTHH thích hợp đặt vào những chỗ có dấu chấm hỏi trong phương trình hóa học sau: ? Na + ? → 2Na2O
A. 4, 1, O2
B. 1, 4, O2
C. 1, 1, O2
D. 2, 2, O2
Bài 6: Cân bằng PTHH sau và cho biết tỉ lệ tổng hệ số của chất phản ứng với sản phẩm.
Na2CO3 + Ca(OH)2 → CaCO3 + NaOH
A. 2:2
B. 3:2
C. 2:3
Bài 4: Cân bằng PTHH sau:
Mg + H2SO4 (đ, n) → MgSO4 + SO2 + H2O
Hỏi tổng hệ số các chất phản ứng là bao nhiêu?
A. 2
B. 3
C. 4
D. 5
Bài 5: Chọn hệ số và CTHH thích hợp đặt vào những chỗ có dấu chấm hỏi trong phương trình hóa học sau: ? Na + ? → 2Na2O
A. 4, 1, O2
B. 1, 4, O2
C. 1, 1, O2
D. 2, 2, O2
Bài 6: Cân bằng PTHH sau và cho biết tỉ lệ tổng hệ số của chất phản ứng với sản phẩm.
Na2CO3 + Ca(OH)2 → CaCO3 + NaOH
A. 2:2
B. 3:2
C. 2:3
Câu 1 Viết phương trình hóa học theo dãy biến hóa sau : ( Ghi rõ điều kiện phản ứng nếu có ). a, CaSO3 --> SO2 --> SO3 --> H2SO4 --> Fe2(SO4)3 Câu 2 Hãy nêu hiện tượng phương trình hóa học nếu có : a, Cho kim loại kẽm vào dung dịch axit clohiđric b, Cho bột đồng ( II ) oxit vào dung dịch axit sunfuric c, Cho bột Ag vào dung dịch sunfuric Câu 3 Cho 25,8g hỗn hợp nhôm và nhôm oxit tác dụng vừa đủ với 400ml dung dịch axit sunfuric thu được 6.72( 1 ) khi H2 ở đktc và dung dịch A. a, Viết PTHH xảy ra b, Tính thành phần phần trăm khối lượng các chất trong hỗn hợp ban đầu ? c, Tính nồng độ mol của dung dịch axit sunfuric tham gia phản ứng ?
Câu 1:
\(a.\left(1\right)CaSO_3+2HCl\rightarrow CaCl_2+SO_2+H_2O\\ \left(2\right)SO_2+\dfrac{1}{2}O_2⇌\left(t^o,xt\right)SO_3\\ \left(3\right)SO_3+H_2O\rightarrow H_2SO_4\\ \left(4\right)Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Câu 2:
a. Hiện tượng: Kẽm tan, tạo thành dung dịch khoomg màu, có sủi bọt khí.
b. Hiện tượng: Bột đồng (II) oxit có màu đen chuyển sang màu đỏ, đồng thời có hơi nước bám ở thành ống nghiệm.
c. Nếu là dung dịch H2SO4 loãng thì không có hiện tượng gì xảy ra. Nhưng nếu là dd H2SO4 đặc, nóng thì bột Ag tan đồng thời có xuất hiện chất khí mùi hắc nhé!
\(PTHH:\\ a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ b.CuO\left(đen\right)+H_2\underrightarrow{t^o}Cu\left(đỏ\right)+H_2O\\ c.2Ag+2H_2SO_4\left(đặc\right)\underrightarrow{t^o}Ag_2SO_4+SO_2\uparrow\left(mùi.hắc\right)+2H_2O\)
Hoàn thành các phương trình hóa học sau (ghi rõ điều kiện, nếu có):
(1) Fe2(SO4)3 + X → K2SO4 + Y
(2) FeS + Z → FeCl2 + T
(3) FeCl3 + A → Fe(NO3)3 + B
(4) Fe + D(lấy dư) → E + SO2 + H2O
(1) Fe2(SO4)3 + 6KOH → 3K2SO4 + Fe(OH)2
(2) FeS + 2HCl → FeCl2 + H2S
(3) FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl
(4) 2Fe + 6H2SO4 đặc(lấy dư) → Fe2(SO4)3 + 3SO2 + 6H2O