trộn V1 lit dung dịch H2SO4 1M với V2 lit dung dịch NaOH 1M được 0,5l dung dịch A, 100ml dung dịch A hòa tan vừa đủ 0,81g Al. Tính V1, V2 nếu sự pha trộn không làm thay đổi thể tích

Những câu hỏi liên quan
Trộn V1 lít dung dịch HCl 0,6M với V2 lít dung dịch NaOH 0,4M thu được 0,6 lít dung dịch A. Biết 0,6 lít dung dịch A có thể hòa tan hết 1,02 gam Al2O3 (xem như sự pha trộn không làm thay đổi thể tích). Tính V1 và V2.
nHCl=0,6V1 mol; n NaOH=0,4V2 mol
Do dd A có thể hòa tan Al2O3=> HCl hoặc NaOH dư
*TH1: HCl dư
Al2O3+6HCl-> 2AlCl3+3H2O nAl2O3=0,01 mol=> nHCl dư =0,06 mol
nHCl phản ứng= n NaOH=0,4V2 mol=>n HCl dư = 0,6V1-0,4V2=0,06 mol
V1+V2=0,6l
giải hpt ra V1=V2=0,3l
*TH2: NaOH dư
2NaOH+Al2O3-> 2NaAlO2+H20 (3)
n NaOH dư=2nAl2O3=0,02 mol
=>nNaOH dư= 0,4V2-0,6V1=0,02 mol
V1+V2=0,6l
giải hpt ra V1=0,22l, V2=0,38l
Đúng 0
Bình luận (1)
Trộn V1 lit dung dịch H2SO4 0,3M với V2 lít dung dịch NaOH 0,4M thu được 0,6 lít dung dịch A. Tính V1, V2. Biết rằng 0,6 lít dung dịch A hoà tan vừa đủ 0,72 gam Mg và các phản ứng xảy ra hoàn toàn.
(Vì sao dung dịch A hoà tan vừa đủ 0,72 gam Mg thì H2SO4 dư vậy ạ?)
trộn v1 l dd h2so4 0,3M với v2 l dd naoh0,4M thu đc 0,6l dung dịch A.tính v1,v2 biết 0,3 l dd A hòa tan vừa đủ 0,51 g al2o3
Coi sự pha trộn không thay đổi thể tích và xảy ra hoàn toàn
Bài 9. Trộn V1 lít dung dịch HCI 1M với V2 lít dung dịch NaOH 2M được dung dịch X. Dung dịch X hoà tan được tối đa a mol Al(OH)3. Tìm biểu thức liên hệ giữa V1, V2, và a?
nHCl = V1 mol
n NaOH = 2V2 mol
Trường hợp 1: Dung dịch X chứa HCl dư
HCl + NaOH → NaCl + H2O
2V2<----2V2
3HCl + Al(OH)3 → AlCl3 + 3H2O
3a<-------a
=> nHCl = 2V2 + 3a = V1
Trường hợp 2: Dung dịch X chứa NaOH
HCl + NaOH → NaCl + H2O
V1------>V1
Al(OH)3 + NaOH → NaAlO2 + 2H2O
a------------> a
n NaOH = V1 + a = 2V2
Đúng 2
Bình luận (0)
X và Y là các dung dịch HCl có nồng độ khác nhau. Lấy V1 lít X trộn với V2 lít Y được 2 lít dungdịch Z (cho rằng sự pha trộn không làm thay đổi thể tích của dung dịch).a. Tính nồng độ mol của dung dịch Z biết rằng V1 lít X phản ứng với dung dịch bạc nitrat dư thì thu được 35,875 gam kết tủa. V2 lít Y phản ứng vừa đủ với 0,5 lít dung dịch NaOH 0,3M.b. Tính nồng độ mol của các dung dịch X và Y, biết rằng nếu cho 0,1 lít X phản ứng hết với sắt thì lượng hiđro thoát ra nhiều hơn so với 0,1 lít Y phả...
Đọc tiếp
X và Y là các dung dịch HCl có nồng độ khác nhau. Lấy V1 lít X trộn với V2 lít Y được 2 lít dungdịch Z (cho rằng sự pha trộn không làm thay đổi thể tích của dung dịch).
a. Tính nồng độ mol của dung dịch Z biết rằng V1 lít X phản ứng với dung dịch bạc nitrat dư thì thu được 35,875 gam kết tủa. V2 lít Y phản ứng vừa đủ với 0,5 lít dung dịch NaOH 0,3M.
b. Tính nồng độ mol của các dung dịch X và Y, biết rằng nếu cho 0,1 lít X phản ứng hết với sắt thì lượng hiđro thoát ra nhiều hơn so với 0,1 lít Y phản ứng hết với sắt là 448 ml (đktc)
\(a.BT\left[Cl\right]:n_{AgCl}=n_{HCl\left(X\right)}=\dfrac{35,875}{143,5}=0,25mol\\ HCl+NaOH->NaCl+H_2O\\ n_{HCl\left(Y\right)}=0,5.0,3=0,15mol\\ C_{M\left(Z\right)}=\dfrac{0,4}{2}=0,2\left(M\right)\\ b.Fe+2HCl->FeCl_2+H_2\\ n_{HCl\left(X\right)}=a;n_{HCl\left(Y\right)}=b\left(mol\right)\\ a-b=\dfrac{0,448}{22,4}.2=0,04mol\\ Từ\left(a\right)\Rightarrow n_{HCl\left(X\right)}:n_{HCl\left(Y\right)}=0,25:0,15=\dfrac{5}{3}=\dfrac{a}{b}\\ \Rightarrow a=0,1;b=0,06\\ C_{M\left(X\right)}=\dfrac{0,1}{0,1}=1M\\ C_{M\left(Y\right)}=\dfrac{0,06}{0,1}=0,6\left(M\right)\)
Đúng 1
Bình luận (0)
trộn V1 lít dung dịch h2so4 0.3M với v2 lít dung dịch natri hidroxit 0.4M thu được 0.6 lít dung dịch A . tính v1, v2 . biết rằng 0.6 lít dung dịch A hòa tan vừa đủ 0.54 gam Nhôm với các phản ứng xảy ra hoàn toàn
Dung dịch A gồm NaOH 1M và Ba(OH)2 0,5 M. Dung dịch B gồm AlCl3 1M và Al2(SO4)3 0,5 M. Cho V1 lit dung dịch A vào V2 lit dung dịch B thu được 427,5V2 gam kết tủa. Tỉ số V1:V2 ? A. 3,5 B. 2,537 và 3,5 C. 3,5 và 3 D. 3
Đọc tiếp
Dung dịch A gồm NaOH 1M và Ba(OH)2 0,5 M. Dung dịch B gồm AlCl3 1M và Al2(SO4)3 0,5 M. Cho V1 lit dung dịch A vào V2 lit dung dịch B thu được 427,5V2 gam kết tủa. Tỉ số V1:V2 = ?
A. 3,5
B. 2,537 và 3,5
C. 3,5 và 3
D. 3
Chọn đáp án B
Ta có
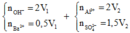
Trường hợp 1 : Nếu V1 > 3V2 → Al(OH)3 bị tan 1 phần và ![]() bị kết tủa hết.
bị kết tủa hết.
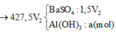
![]()
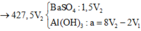
![]()
![]()
![]()
![]()
Trường hợp 1 : Nếu V1 < 3V2 → Al(OH)3 chưa cực đại và Ba2+ bị kết tủa hết
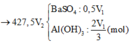
![]()
![]()
![]()
Đúng 0
Bình luận (0)
Hòa tan m gam Fe vào 300 ml dung dịch H2SO4 0,5M thu được dung dịch X và V1 lít H2 ở đktc. Cho dung dịch X tác dụng vừa đủ với V2 ml dung dịch Ba(OH)2 1M thu được 41,7 gam kết tủa. Tính m, V1, V2.
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+Fe\left(OH\right)_2\downarrow\)
Ta có: \(n_{H_2SO_4}=0,3\cdot0,5=0,15\left(mol\right)=n_{Fe}=n_{H_2}=n_{Ba\left(OH\right)_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,15\cdot56=8,4\left(g\right)\\V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\V_{Ba\left(OH\right)_2}=\dfrac{0,15}{1}=0,15\left(l\right)=150\left(ml\right)\end{matrix}\right.\)
*Bạn xem lại đề vì nếu FeSO4 p/ứ hết thì sẽ có nhiều hơn 41,7 gam kết tủa
Đúng 0
Bình luận (1)
Trộn V1 dung dịch H2SO4 3M với V2 ml dung dịch H2SO4 1M thu đc 60 ml dung dịch H2SO4 1,5M .Tính V1,V2
Gọi :
Vdd H2SO4 3M=a(lít);Vdd H2SO4 1M=b(lít)
Ta có :
a + b = 0,09(1)
nH2SO4=3a+b=0,09.1,5(2)
Từ (1)(2) suy ra a = 0,0225 ; b = 0,0675
Đúng 4
Bình luận (0)

















