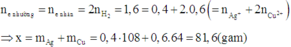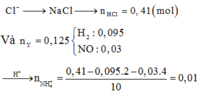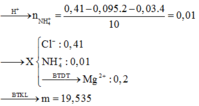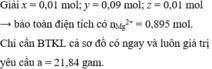Cho m gam rắn A gồm CuO, Cu, Cu(NO3)2 phản ứng với dd HCl. Sau phản ứng thu được 17,92 lít khí G (đktc); biết tỷ khối hơi của G so với H2 bằng 22 và thu được dung dịch B chứa 202,5 gam một chất tan duy nhất. Giá trị m là

Những câu hỏi liên quan
Cho m gam rắn A gồm CuO, Cu, Cu(NO3)2 phản ứng với dd HCl. Sau phản ứng thu được 17,92 lít khí G (đktc); biết tỷ khối hơi của G so với H2 bằng 22 và thu được dung dịch B chứa 202,5 gam một chất tan duy nhất. Giá trị m là
Cho m gam hỗn hợp X gồm Al, Zn và Ni tác dụng hết với dung dịch HCl, thu được 17,92 lít khí H2 (đktc). Nếu cho m gam X tác dụng với dung dịch Y chứa 0,7 mol Cu(NO3)2 và 0,4 mol AgNO3 đến khi phản ứng hoàn toàn thì thu được x gam chất rắn. Giá trị của x là: A. 66,4 B. 88 C. 120 D. 81,6
Đọc tiếp
Cho m gam hỗn hợp X gồm Al, Zn và Ni tác dụng hết với dung dịch HCl, thu được 17,92 lít khí H2 (đktc). Nếu cho m gam X tác dụng với dung dịch Y chứa 0,7 mol Cu(NO3)2 và 0,4 mol AgNO3 đến khi phản ứng hoàn toàn thì thu được x gam chất rắn. Giá trị của x là:
A. 66,4
B. 88
C. 120
D. 81,6
Cho 1 luồng khí O2 qua 8,48 gam hỗn hợp X gồm Fe, Mg, Cu sau một thời gian thu được 10,08 gam hỗn hợp chất rắn Y. Cho Y tan hoàn toàn trong dung dịch HNO3 (dư 20% so với lượng phản ứng). Sau phản ứng thu được dung dịch Z chứa 43,101 gam chất tan và 1,792 lít hỗn hợp khí T gồm NO và NO2 (đktc) có tỷ khối so với H2 là 18. Số mol HNO3 bị khử gần nhất với: A. 0,092 B. 0,087 C. 0,084 D. 0,081
Đọc tiếp
Cho 1 luồng khí O2 qua 8,48 gam hỗn hợp X gồm Fe, Mg, Cu sau một thời gian thu được 10,08 gam hỗn hợp chất rắn Y. Cho Y tan hoàn toàn trong dung dịch HNO3 (dư 20% so với lượng phản ứng). Sau phản ứng thu được dung dịch Z chứa 43,101 gam chất tan và 1,792 lít hỗn hợp khí T gồm NO và NO2 (đktc) có tỷ khối so với H2 là 18. Số mol HNO3 bị khử gần nhất với:
A. 0,092
B. 0,087
C. 0,084
D. 0,081
Định hướng tư duy giải
Có ngay
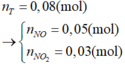
Nhìn thấy Mg nên
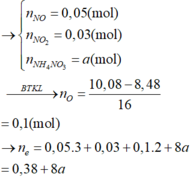


Đúng 0
Bình luận (0)
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và
C
u
(
N
O
3
)
2
, sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và
H
2
. Biết Y có tỷ khối hơi so với
H
2
là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa l...
Đọc tiếp
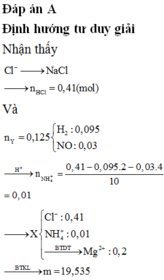
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và C u ( N O 3 ) 2 , sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và H 2 . Biết Y có tỷ khối hơi so với H 2 là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa là 0,41 mol. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là
A. 19,535
B. 18,231
C. 17,943
D. 21,035
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và Cu(NO3)2, sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và H2. Biết Y có tỷ khối hơi so với H2 là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa là 0,41 mol. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là: A. 19,535 B. 18,231 C. 17,943 D. 21,035
Đọc tiếp
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và Cu(NO3)2, sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và H2. Biết Y có tỷ khối hơi so với H2 là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa là 0,41 mol. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 19,535
B. 18,231
C. 17,943
D. 21,035
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và Cu(NO3)2, sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và H2. Biết Y có tỷ khối hơi so với H2 là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa là 0,41 mol. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là: A. 19,535 B. 18,231 C. 17,943 D. 21,035
Đọc tiếp
Nhúng thanh Mg (dư) vào dung dịch chứa HCl và Cu(NO3)2, sau khi kết thúc các phản ứng thu được dung dịch X và 2,8 lít (đktc) hỗn hợp khí Y gồm NO và H2. Biết Y có tỷ khối hơi so với H2 là 4,36. Cho NaOH dư vào X thấy số mol NaOH phản ứng tối đa là 0,41 mol. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 19,535
B. 18,231
C. 17,943
D. 21,035
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với A. 23,0 B. 24,0. C. 21,0. D. 22,0
Đọc tiếp
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với
A. 23,0
B. 24,0.
C. 21,0.
D. 22,0
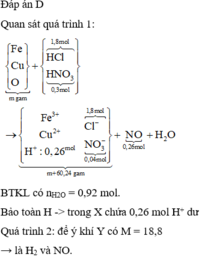
Đáp án D
Quan sát quá trình 1:

BTKL có nH2O = 0,92 mol. Bảo toàn H chứng
tỏ trong X chứa 0,26 mol H+ dư như trên.
♦ Quá trình 2: để ý khí Y có M = 18,8
→ là H2 và NO. Quan sát quá trình chính:
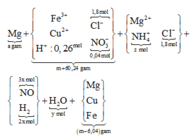
giải tỉ khối Y tìm tỉ lệ 2 khí NO : H2 là 3 : 2 rồi gọi các ẩn như sơ đồ:
• Ghép cụm: nH2O = 2nNO + 3nNH4 ⇄ y = 6x + 3z (1).
• bảo toàn nguyên tố N có: 3x + z = 0,04 mol (2).
• Bảo toàn nguyên tố H có: 4x + 2y + 4z = 0,26 mol (3)
Giải x = 0,01 mol; y = 0,09 mol; z = 0,01 mol ||→ bảo toàn điện tích có nMg2+ = 0,895 mol.
► Chỉ cần BTKL cả sơ đồ có ngay và luôn giá trị yêu cầu a = 21,84 gam
Đúng 0
Bình luận (0)
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với A. 23,0. B. 24,0. C. 21,0. D. 22,0.
Đọc tiếp
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với
A. 23,0.
B. 24,0.
C. 21,0.
D. 22,0.
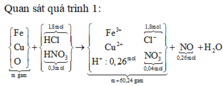
BTKL có nH2O = 0,92 mol. Bảo toàn H chứng tỏ trong X chứa 0,26 mol H+ dư như trên.
♦ Quá trình 2: để ý khí Y có M = 18,8 → là H2 và NO. Quan sát quá trình chính:
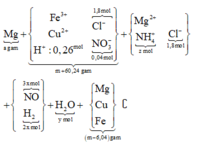
giải tỉ khối Y tìm tỉ lệ 2 khí NO : H2 là 3 : 2 rồi gọi các ẩn như sơ đồ:
• Ghép cụm: nH2O = 2nNO + 3nNH4 ⇄ y = 6x + 3z (1).
• bảo toàn nguyên tố N có: 3x + z = 0,04 mol (2).
• Bảo toàn nguyên tố H có: 4x + 2y + 4z = 0,26 mol (3)
Giải x = 0,01 mol; y = 0,09 mol; z = 0,01 mol
→ bảo toàn điện tích có nMg2+ = 0,895 mol.
► Chỉ cần BTKL cả sơ đồ có ngay và luôn giá trị yêu cầu a = 21,84 gam.
Đáp án D
Đúng 0
Bình luận (0)
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với A. 23,0. B. 24,0. C. 21,0. D. 22,0.
Đọc tiếp
Hòa tan m gam hỗn hợp A gồm FexOy Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m –6,04) gam chất rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với
A. 23,0.
B. 24,0.
C. 21,0.
D. 22,0.