Nguyên tử Canxi (Ca) có bán kính bằng 1,97×10^-8 cm ,khối lượng mol là 40,08 g/mol,khối lượng riêng 1,55 g/cm3.Trong tinh thể kim loại ,các nguyên tử chiếm bao nhiêu phần trăm thể tích ?

Những câu hỏi liên quan
Khối lượng riêng của kim loại canxi là
1
,
55
g
/
c
m
3
. Khối lượng mol của nguyên tử canxi là 40 g/mol. Trong tinh thể canxi, các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng. Bán kính nguyên tử canxi tính theo lí thuyết là A. 0,196 nm. B. 0,185 nm. C. 0,168 nm. D. 0,155nm.
Đọc tiếp
Khối lượng riêng của kim loại canxi là 1 , 55 g / c m 3 . Khối lượng mol của nguyên tử canxi là 40 g/mol. Trong tinh thể canxi, các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng. Bán kính nguyên tử canxi tính theo lí thuyết là
A. 0,196 nm.
B. 0,185 nm.
C. 0,168 nm.
D. 0,155nm.
Chọn A
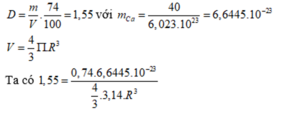
→ R = 1,96.10-8 (cm) = 0,196nm.
Đúng 0
Bình luận (0)
Xác định bán kính của Ca nếu khối lượng riêng của Ca là 1,55 g/cm3 và nguyên tử khối là 40,08. Biết rằng trong tinh thể các nguyên tử Ca chiếm 74% thể tích trong tinh thể?
\(V_{1.mol.Ca\left(tinh.thể\right)}=\dfrac{40,08g}{1,55g/cm^3}=25,858cm^3\)
\(V_{thực.sự.1mol.Ca}=25,858.\dfrac{74}{100}=19,135cm^3\)
\(\Rightarrow V_{1.nguyên.tử.Ca}=\dfrac{19,135}{6,023.10^{23}}=3,18.10^{-23}cm^3\)
Giả sử nguyên tử Ca là khối cầu thì: \(V=\dfrac{4}{3}\pi R^3\Rightarrow R=\sqrt[3]{\dfrac{3V}{4\pi}}\)
\(R_{Ca}=\sqrt[3]{\dfrac{3.3,18.10^{-23}}{4.3,14}}=1,97.10^{-8}cm\) hay \(1,97\) \(A^o\)
Đúng 1
Bình luận (0)
Khối lượng riêng của canxi kim loại là 1,55 g/cm3. Giả thiết rằng, trong tinh thể canxi các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là rỗng. Bán kính nguyên tử canxi theo tính toán là: A. 0,185nm B. 0,196nm C. 0,168nm D. 0,155nm
Đọc tiếp
Khối lượng riêng của canxi kim loại là 1,55 g/cm3. Giả thiết rằng, trong tinh thể canxi các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là rỗng. Bán kính nguyên tử canxi theo tính toán là:
A. 0,185nm
B. 0,196nm
C. 0,168nm
D. 0,155nm
Nguyên tử Au có bán kính và khối lượng mol nguyên tử lần lượt là 1,44. 10-10 và 197g/mol. Biết khối lượng riêng của Au là 19,36g/cm3 Hỏi các nguyên tử Au chiếm bao nhiêu phần trăm thể tích trong tinh thể A . 25% B . 68% C . 76% D. 74%
Đọc tiếp
Nguyên tử Au có bán kính và khối lượng mol nguyên tử lần lượt là 1,44. 10-10 và 197g/mol. Biết khối lượng riêng của Au là 19,36g/cm3 Hỏi các nguyên tử Au chiếm bao nhiêu phần trăm thể tích trong tinh thể
A . 25%
B . 68%
C . 76%
D. 74%
Trong tinh thể, nguyên tử crom chiếm 68% về thể tích. Khối lượng riêng của kim loại crom là 7,19 g/cm3. Bán kính nguyên tử tương đối của nguyên tử Cr là (biết khối lượng mol của Cr 52) A. 1,17. 10-8 cm. B. 1,25.10-8 cm. C. 1,12. 10-8 cm. D. 1,54. 10-8 cm.
Đọc tiếp
Trong tinh thể, nguyên tử crom chiếm 68% về thể tích. Khối lượng riêng của kim loại crom là 7,19 g/cm3. Bán kính nguyên tử tương đối của nguyên tử Cr là (biết khối lượng mol của Cr = 52)
A. 1,17. 10-8 cm.
B. 1,25.10-8 cm.
C. 1,12. 10-8 cm.
D. 1,54. 10-8 cm.
Khối lượng riêng của canxi kim loại là 1,55 g/cm3. Tinh thể canxi có cấu trúc lập phương tâm diện. Bán kính nguyên tử canxi tính theo lý thuyết là: A. 0,196 nm. B. 0,185 nm. C. 0,168 nm. D. 0,155 nm.
Đọc tiếp
Khối lượng riêng của canxi kim loại là 1,55 g/cm3. Tinh thể canxi có cấu trúc lập phương tâm diện. Bán kính nguyên tử canxi tính theo lý thuyết là:
A. 0,196 nm.
B. 0,185 nm.
C. 0,168 nm.
D. 0,155 nm.
Đáp án A.
Trong tinh thể lập phương tâm diện, độ đặc khít là 74%.
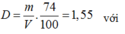
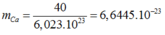
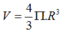
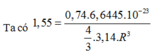
![]()
Đúng 0
Bình luận (0)
Bán kính nguyên tử gần đúng của nguyên tử R ở 25 độ C là 1,965.10-8cm. Biết tại nhiệt độ đó khối lượng riêng của R kim loại là 1,55 g/cm3. Giả thiết rằng, trong tinh thể R các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là rỗng. R là chất gì?
Mong mọi ng giúp e
Một loại tinh thể nguyên tử, có khối lượng riêng là 19,36g/ cm 3 . Trong đó, các nguyên tử chỉ chiếm 74% thể tích của tinh thể, còn lại là các khe rỗng. Bán kính của nguyên tử là 1,44Å. Tính khối lượng riêng của nguyên tử, từ đó suy ra khối lượng mol nguyên tử.
Khối lượng riêng của nguyên tử là:
D = 19,36.100/74 = 26,16(g/ cm 3 )
Khối lượng của 1 mol nguyên tử :
M = V.D.N = 4/3π r 3 .D.N = 4/3. 3,14. 1 , 44 . 10 - 8 3 .26,16. 6,022. 10 23 ≈ 197 (g/mol)
Đúng 0
Bình luận (0)
Khối lượng riêng của canxi kim loại là 1,55g/cm3. Giả thiết rằng trong tinh thể canxi các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng. Bán kính nguyên tử canxi tính theo lý thuyết là: A. 0,196nm. B. 0,185nm. C. 0,168nm. D. 0,155nm.
Đọc tiếp
Khối lượng riêng của canxi kim loại là 1,55g/cm3. Giả thiết rằng trong tinh thể canxi các nguyên tử là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng. Bán kính nguyên tử canxi tính theo lý thuyết là:
A. 0,196nm.
B. 0,185nm.
C. 0,168nm.
D. 0,155nm.
Đáp án A.
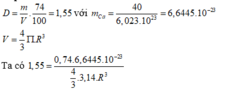
=> R = 1,96.10-8 (cm) = 0,196nm.
Đúng 0
Bình luận (0)










