Cho 19,46g hh gồm Mg,Al,Zn.Trong đó khối lượng Mg bằng khối lượng Al.Tác dụng dd HCl dư thu đc 16,352 lít khí H2(đktc).Tính % về khối lượng của các kim loại
Cho 19,46g hỗn hợp Mg,Al và Zn trong đó khối lượng của Mg bằng khối lượng của Al tác dụng với dung dịch HCl 2M tạo thành 16,352 lít khí H2 thoát ra ở đktc
a.Viết các PT phản ứng
b.Tính % về khối lượng của từng kim loại có trong hỗn hợp
c.Tính V dung dịch HCl cần lấy ban đầu biết người ta dùng dư 10% so vs lượng phản ứng
Cho 19,46g hỗn hợp Mg,Al và Zn trong đó khối lượng của Mg bằng khối lượng của Al tác dụng với dung dịch HCl 2M tạo thành 16,352 lít khí H2 thoát ra ở đktc
a.Viết các PT phản ứng
b.Tính % về khối lượng của từng kim loại có trong hỗn hợp
c.Tính V dung dịch HCl cần lấy ban đầu biết người ta dùng dư 10% so vs lượng phản ứng
Cho 10,2g hh gồm Al và Mg vào dd HCl dư , sau khi PƯ kết thúc thì thu đc 11,2l khí (ở đktc)
a. Hãy tính thành phần % về khối lượng của mỗi kim loại trong hh
b. Dẫn toàn bộ khí H2 thu đc đi qua ống có chứa a gam Fe2O3 đc nung nóng , sau PƯ thì người ta thu đc 60g chất rắn . Hãy tính a
- Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\Rightarrow27a+24b=10,2\left(1\right)\)
Khí thu được sau p/ứ là khí H2: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
2 3 (mol)
a 3/2 a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
1 1 (mol)
b b (mol)
Từ hai PTHH trên ta có: \(\dfrac{3}{2}a+b=0,5\left(2\right)\)
\(\left(1\right),\left(2\right)\) ta có hệ: \(\left\{{}\begin{matrix}27a+24b=10,2\\\dfrac{3}{2}a+b=0,5\end{matrix}\right.\)
Giải ra ta có \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
a) \(\%Al=\dfrac{m_{Al}}{m_{hh}}.100\%=\dfrac{0,2.27}{10,2}.100\%\approx52,94\%\)
\(\%Mg=100\%-\%Al=100\%-52,94=47,06\%\)
b)
\(3H_2+Fe_2O_3\rightarrow^{t^0}2Fe+3H_2O\)
3 1 2 (mol)
0,5 1/6 1/3 (mol)
\(m_{Fe}=\dfrac{1}{3}.56=\dfrac{56}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(pứ\right)}=\dfrac{1}{6}.160=\dfrac{80}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(dư\right)}=60-m_{Fe}=60-\dfrac{56}{3}=\dfrac{124}{3}\left(g\right)\)
\(a=\dfrac{124}{3}+\dfrac{80}{3}=68\left(g\right)\)
Cho 18,6g hhX (Mg, Fe, Al) tác dụng vừa đủ với 7,841l O2 (đktc). Mặt khác cứ 0,275 mol hh trên tác dụng với dd HCl dư thu đc 7,28l H2( đktc). Tính % khối lượng mỗi kim loại trong hh X
Cho 19,46g hỗn hợp Mg, Al, Zn trong đó khối lượng của Mg bằng khối lượng Al td với dd HCl 2M tạo thành 16,352 lít H2 thoát ra ở đktc
a) Tính % về khối lượng của từng kim loại có trong hỗn hợp
b) Tính thể tích dd HCl đã dùng biết người ta dùng dư 10% so với lý thuyết
a)\(Mg+2HCl--.MgCl2+H2\)
X------------------------------------x(mol)
\(2Al+6HCl-->2AlCl3+3H2\)
y--------------------------------------1,5y(mol)
\(Zn+2HCl-->ZnCl2+H2\)
z-------------------------------------z(mol)
\(n_{H2}=\frac{16,352}{22,4}=0,73\left(mol\right)\)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}24x+27y+65z=19,46\\24x-27y=0\\x+1,5y+z=0,73\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,27\\y=0,24\\z=0,1\end{matrix}\right.\)
\(\%m_{Mg}=\frac{0,27.24}{19,46}.100\%=33,3\%\)
\(\%m_{Al}=\frac{0,24.27}{19,46}.100\%=33,3\%\)
\(\%m_{Zn}=100-33,3-33,3=33,4\%\)
b)\(n_{HCl}=2n_{H2}=1,46\left(mol\right)\)
\(V_{HCl}=\frac{1,46}{2}=0,73\left(l\right)\)
nH2 = 0.73
gọi nMg=x mol ,nAl=y mol,nZn = z mol
Có hệ sau :24x+27y+65z=19,46
24x=27y
2x+y+2z=0,73.2
=>x = 0.27 mol,
y = 0.24mol
,z = 0.1 mol
mMg = mAl = 6.48 => % Al = %Mg = 33.3%
=> % Zn = 33.4%
Cho 11,5 gam hh ( Na , Mg, Al ) hoà tan vào nước thu được 4,48 lit khí đo ở đktc , 6,15 gam chất rắn không tan và dd Y. lấy chất rắn không tan tavs dụng với dd HCl dư thu được 0.275 mol H2 . Tính % về khối lượng kim loại Na, Mg , Al trong 11,5 gam ban đầu
na+2h20->2naoh+h2
nh2=4.48/22.4=0.2mol
->nNa=0.2mol
bt e
2nMg+3nAl=2*0.275
bt kl
24nMg+27nAl=6.15
->nMg=0.2mol
nAl=0.05mol
->kl tung cai roi tinh phan tram
Hòa tan hoàn toàn 3,87g hỗn hợp X gồm Al và Mg bằng một lượng HCl (dư) thu được dung dịch X và 4,368 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong X.
\(n_{H_2}=\dfrac{4,368}{22,4}=0,195mol\)
\(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\Rightarrow27x+24y=3,87\left(1\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(\Rightarrow1,5x+y=0,195\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
\(m_{Al}=0,09\cdot27=2,43g\)
\(m_{Mg}=0,06\cdot24=1,44g\)
Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc. Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
$2Al + 2H_2O + 2NaOH \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}. \dfrac{6,72}{22,4} = 0,2(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} +n_{Mg}$
$\Rightarrow n_{Mg} = \dfrac{8,96}{22,4} - 0,2.\dfrac{3}{2} = 0,1(mol)$
Suy ra :
$m_{Mg} = 0,1.24 = 2,4(gam) ; m_{Al} = 0,2.27 = 5,4(gam)$
Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc.
Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
Gọi x, y (mol) lần lượt là số mol Mg, Al trong hỗn hợp.
Phương trình phản ứng:
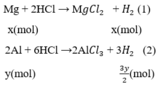
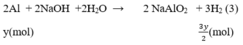
Số mol H2
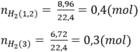
Theo bài ra ta có hệ phương trình:
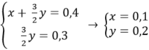
mMg = 24.0,1 = 2,4(g)
mAl = 27.0,2 = 5,4(g)