Hỗn hợp A có N2 và 2 hidrocacbon nối tiếp , có khối lượng mA=13.8g và VA LÀ 11.2L. Trộn A với O2 dư rồi đốt , đc 11.7g H2O và 21.28l CO2
Xđ CTPT ,tình % khối lượng của từng hidrocacbon trong A
Đốt cháy hỗn hợp hai hidrocacbon đồng đẳng kế tiếp nhau thu được 11.7g H2O và 17.6g CO2.Xác định CTPT của hai hidrocacbon trên.Tính % khối lượng mỗi ankan trong hỗn hợp.?
\( n_{H_2O} = \dfrac{11,7}{18} = 0,65\ mol\\ n_{CO_2} = \dfrac{17,6}{44} = 0,4\ mol\\ \Rightarrow Hidrocacbon :\ C_nH_{2n+2}\\ n_{hidrocacbon} = n_{H_2O} - n_{CO_2} = 0,65 - 0,4 = 0,25(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_{hidrocacbon}} = \dfrac{0,4}{0,25} = 1,6\\ 1< n=1,6<2\Rightarrow Hidrocacbon:\ CH_4,C_2H_6\\ n_{CH_4} = a\ mol ; n_{C_2H_6} = b(mol)\\ \Rightarrow a + b = 0,25 ; n_{CO_2} =a + 2b = 0,4\\ \Rightarrow a = 0,1 ; b = 0,15\\ \Rightarrow \%m_{CH_4} = \dfrac{0,1.16}{0,1.16+0,15.30}.100\% = 26,23\%\)
\(\%m_{C_2H_6} = 100\% - 26,23\% = 73,77\%\)
Hỗn hợp khí A chứa N2 và hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 gam và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam H2O và 21,28 lít CO2. Các thể tích khí đo ở điều kiện chuẩn. CTPT của 2 hiđrocacbon là:
A. C3H4; C4H6
B. C4H6; C5H8
C. C3H2; C4H4
D. C4H4; C5H6
Đốt cháy hoàn toàn hỗn hợp Z gồm 2 hidrocacbon liên tiếp trong dãy đồng đẳng thu được 48,4g CO2 và 29,7g H2O. Xác định CTPT và tính phần trăm khối lượng của mỗi hidrocacbon
\(n_{CO_2}=\dfrac{48,4}{44}=1,1\left(mol\right)\\ n_{H_2O}=\dfrac{29,7}{18}=1,65\left(mol\right)\\ Vì:n_{H_2O}>n_{CO_2}\Rightarrow hhZ:hh.ankan\\ CTTQ:C_aH_{2a+2}\\ Ta.có:1< \dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1,65}{1,1}=1,5< 2\\ \Rightarrow hh.Z:50\%V_{CH_4},50\%V_{C_2H_6}\\ \Rightarrow\%m_{\dfrac{CH_4}{hhZ}}=\dfrac{16}{16+28}.100\approx36,364\%\\ \Rightarrow\%m_{\dfrac{C_2H_6}{hhZ}}\approx63,636\%\)
Cho hỗn hợp khí A gồm 4 hidrocacbon thuộc các dãy dãy đồng đẳng khác nhau A1 A2, A3, A4 và hỗn hợp khí B gồm O2 và O3 có tỉ khối so với He bằng 9,5. Trộn A với B theo tỉ lệ thể tích VA : VB = 1,5 :3,2 rồi đốt cháy hỗn hợp thu được, sau phản ứng chỉ có CO2 và H2O với tỉ lệ thể tích tương ứng là 1,3 :1,2. Tỉ khối của hỗn hợp khí A so với He là:
A.6.
B.5.
C.7.
D.8.
Với bài toán cho tỉ lệ thể tích, số mol như vậy thì đầu tiên ta sẽ dùng phương pháp tự chọn lượng chất để giải cho đơn giản:
+ Chọn nA =1,5 mol; nB = 3,2 mol
-------------\\\\\\\\\\\O2 : 32 48 – 38 =10
= 9,5.4 = 38
O3 : 48 38 – 32 = 6

Ta có: 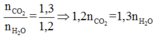
+ Thấy ngay dấu hiệu bảo toàn nguyên tố O:
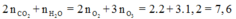
Ta có hệ phuơng trình sau:
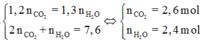
+ Bảo toàn khối luợng kết hợp bảo toàn nguyên tố C, H ta có:
![]()
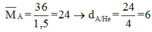
Đáp án A
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hidrocacbon mạch hở có số liên kết pi nhỏ hơn 3. Trộn X và Y theo tỷ lệ mol nx:ny=1:5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17g hỗn hợp Z cần vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2,H2 và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của hidrocacbon có phân tử khối lớn hơn trong Y gần nhất với giá trị nào?
A. 71%
B. 79%
C. 57%
D. 50%
Đáp án A
nO2=0,3125 mol
BTKL=>mN2=3,17+0,3125.32-12,89=0,28 gam=>nN2=0,01 mol=>n amin=0,02 mol => n hiđrocacbon=0,1 mol
- Giả sử số mol CO2 và H2O lần lượt là x, y
44x+18y=12,89
0,3125.2=2x+y (BTNT: O)
=>x=0,205; y=0,215
Ctb=0,205/0,12=1,7 => CH4
Htb=0,215/0,12=1,8 => C2H2 (Do số liên kết pi nhỏ hơn 3)
Đặt:
C2H7N: a
C3H9N: 0,02-a
CH4: b
C2H2: 0,1-b
+ BTNT C: 2a+3(0,02-a)+b+2(0,1-b)=0,205
+ BTNT H: 7a+9(0,02-a)+4b+2(0,1-b)=0,215.2
=>a=0,015;b=0,04 => CH4 (0,04 mol) C2H2 (0,06 mol)
=>%mC2H2=0,06.26/(0,06.26+0,04.16)=71%
Hỗn hợp khí A chứa nitơ và hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 g và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam H 2 O và 21,28 lít C O 2 . Các thể tích đo ở đktc.
Hãy xác định công thức phân tử và phần trăm về khối lượng của từng hiđrocacbon trong hỗn hợp A.
Số mol
C
O
2
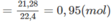
Khối lượng C trong A là: 0,95.12 = 11,4 (g).
Số mol
H
2
O
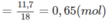
Khối lượng H trong A là: 0,65.2 = 1,3 (g).
Tổng khối lượng của C và H chính là tổng khối lượng 2 hiđrocacbon. Vậy, khối lượng N2 trong hỗn hợp A là : 18,30 - (11,4 + 1,3) = 5,6 (g)
Số mol
N
2
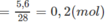
Số mol 2 hidrocacbon 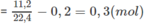
Đặt lượng C x H y là a mol, lượng C x + 1 H y + 2 là b mol :
a + b = 0,2 (1)
Số mol C = số mol C O 2 , do đó :
xa + (x + 1)b = 0,95 (2)
Số mol H = 2.số mol H 2 O , do đó :
ya + (y + 2)b = 2. 0,65= 1,3
Từ (2) ta có x(a + b) + b = 0,95 ⇒ b = 0,95 - 0,3x
Vì 0 < b < 0,3, nên 0 < 0,95 - 0,3x < 0,3
Từ đó tìm được 2,16 < x < 3,16 ⇒ x = 3.
⇒ b = 0,95 − 3.0,3 = 5. 10 - 2
⇒ a = 0,3 − 0,05 = 0,25
Thay giá trị tìm được của a và b vào (3), ta có y = 4.
% về khối lượng của C 3 H 4 trong hỗn hợp A:

% về khối lượng của C 4 H 6 trong hỗn hợp A :

đốt cháy hoàn toàn 3gr hidrocacbon A thu đc 5.4 gr H2o biết khối lượng mol của A là 30g
a) lập CTPT của A
b) viết CTCT có thể có của A
đốt cháy hoàn toàn hỗn hợp A gồm 1 hidrocacbon ở thể khí và oxi dư thu dduocj hỗn hợp B có thành phần thể tích là 30%co2 20%h2o 50%o2 xác định ctpt của h-c
\(Coi\ n_B = 1(mol) \\ n_{CO_2} = 1.30\% =0,3(mol) ; n_{H_2O} = 1.20\% = 0,2(mol)\\ A: C_nH_{2n+2-2k}\\\ n_C = n_{CO_2} = 0,3(mol)\\ n_H = 2n_{H_2O} = 0,4(mol)\\ Ta có : \dfrac{n}{2n+2-2k} = \dfrac{0,3}{0,4}\\ \Leftrightarrow 0,4n = 0,6n + 0,6 - 0.6k\\ \Leftrightarrow 0,6k -0,2n = 0,6\\ \Leftrightarrow 6k - 2n = 6\)
Với k = 1 thì n = 0(loại)
Với k = 2 thì n = 3(chọn)
Với k = 3 thì n = 6(chọn)
.....
Vậy hidrocacbon có thể là : \(C_3H_4 ; C_6H_8,...\)
\(Coi\ n_B = 1(mol)\\ \Rightarrow n_{CO_2} = 1.30\% = 0,3(mol) ; n_{H_2O} = 20\% = 0,2(mol) ; n_{O_2} = 50% = 0,5(mol)\)
Vì \(n_{CO_2} > n_{H_2O} \Rightarrow A: C_nH_{2n-2}\)
\(n_A = n_{CO_2} - n_{H_2O} = 0,3 - 0,2 = 0,1(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_A} = \dfrac{0,2}{0,1} = 2\\ CTPT\ A: C_2H_2\)
Cho hỗn hợp khí X gồm 3 hidrocacbon và hỗn hợp khí Y gồm O2, O3 (tỉ khối hơi so với hidro bằng 19). Trộn X với Y theo tỉ lệ Thể tích VX : VY = 1 : 2 rồi đốt cháy hỗn hợp thu được, sau phản ứng chỉ có CO2 và H2O theo tỉ lệ
A. 10,75
B. 43,00
C. 21,50
D. 16,75
Đáp án A
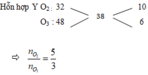
Giả sử số mol của Y = 0,8 mol => nX = 0,4mol
Bảo toàn nguyên tố O => 2nO2 + 3nO3 = 2nCO2 + nH2O = 1,9
nCO2 : nH2O = 6:7
=> nCO2 = 0,6 và nH2O = 0,7 mol
mX = mC + mH = 0,6 . 12 + 0,7 . 2 = 8,6g
=> MX = 8,6 : 0,4 = 21,5
dX/H2 = 10,75