Đốt cháy hoàn toàn 12,2 gam hợp chất X cần 3,36 lít khí oxi tạo thành hỗn hợp khí nitơ và khí cacbonic có tỉ lệ số mol tương ứng là 1:2 và 5,4 gam nước. Tỉ khối của hỗn hợp X so với không khí nhỏ hơn 2,5. Tìm X

Những câu hỏi liên quan
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 220 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là A. 16,464 B. 16,686 C. 16,576 D. 17,472
Đọc tiếp
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 220 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là
A. 16,464
B. 16,686
C. 16,576
D. 17,472
Đáp án A
có nO ÷ nN = 24 ÷ 11 ||→ X dạng CnHmN11O24; X + HCl là phản ứng của –NH2 + HCl → –NH3Cl.
nHCl = 0,22 mol ||→ nX = 0,02 mol. Đốt X → 0,62 mol CO2 ||→ n = 31.
19,62 gam X, nX = 0,02 mol → MX = 981 → m = 71 → nH2O = 0,71 mol.
Bảo toàn O có nO2 = 0,735 mol ||→ V = 16,464 lít
Đúng 0
Bình luận (0)
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 200 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là A. 16,464. B. 16,686. C. 16,576. D. 17,472.
Đọc tiếp
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 200 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là
A. 16,464.
B. 16,686.
C. 16,576.
D. 17,472.
Chọn đáp án A
có nO ÷ nN = 24 ÷ 11 ||→ X dạng CnHmN11O24; X + HCl là phản ứng của –NH2 + HCl → –NH3Cl.
nHCl = 0,22 mol ||→ nX = 0,02 mol. Đốt X → 0,62 mol CO2 ||→ n = 31.
19,62 gam X, nX = 0,02 mol → MX = 981 → m = 71 → nH2O = 0,71 mol.
Bảo toàn O có nO2 = 0,735 mol ||→ V = 16,464 lít. Chọn A
Đúng 0
Bình luận (0)
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 200 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là: A. 16,464. B. 16,686. C. 16,576. D. 17,472.
Đọc tiếp
Hỗn hợp X gồm một số amino axit. Trong X, tỉ lệ khối lượng của oxi và nitơ tương ứng là 192:77. Để tác dụng vừa đủ với 19,62 gam hỗn hợp X cần 200 ml dung dịch HCl 1M. Mặt khác đốt cháy hoàn toàn 19,62 gam hỗn hợp X cần V lít khí O2 (đktc) thu được N2, H2O và 27,28 gam CO2. Giá trị của V là:
A. 16,464.
B. 16,686.
C. 16,576.
D. 17,472.
Chọn đáp án A.
Có nO ÷ nN = 24 ÷ 11
→ X dạng CnHmN11O24; X + HCl là phản ứng của –NH2 + HCl → –NH3Cl.
nHCl = 0,22 mol
→ nX = 0,02 mol.
Đốt X → 0,62 mol CO2
→ n = 31.
19,62 gam X, nX = 0,02 mol
→ MX = 981
→ m = 71
→ nH2O = 0,71 mol.
Bảo toàn O có nO2 = 0,735 mol
→ V = 16,464 lít.
Đúng 0
Bình luận (0)
Đun hỗn hợp gồm ancol A và axit B (đều là chất có cấu tạo mạch hở, không phân nhánh) thu được este X. Đốt cháy hoàn toàn m gam X thu được 1,344 lít khí CO2 (đktc) và 0,72 gam nước. Lượng oxi cần dùng là 1,344 lít (đktc). Biết tỉ khối hơi của X so với không khí nhỏ hơn 6. Công thức phân tử của X là: A. C3H4O2 B. C6H8O4 C. C3H2O2 D. Đáp án khác
Đọc tiếp
Đun hỗn hợp gồm ancol A và axit B (đều là chất có cấu tạo mạch hở, không phân nhánh) thu được este X. Đốt cháy hoàn toàn m gam X thu được 1,344 lít khí CO2 (đktc) và 0,72 gam nước. Lượng oxi cần dùng là 1,344 lít (đktc). Biết tỉ khối hơi của X so với không khí nhỏ hơn 6. Công thức phân tử của X là:
A. C3H4O2
B. C6H8O4
C. C3H2O2
D. Đáp án khác
Hỗn hợp khí X gồm
N
H
3
và etylamin có tỉ khối so với
C
H
4
là 1,4125. Đốt cháy hoàn toàn m gam X bằng lượng không khí vừa đủ (giả sử trong không khí oxi chiếm 20%, còn lại là khí nitơ) thì thu được hỗn hợp gồm
C
O
2
, hơi nước và
N
2
có tổng khối lượng là 43,4 gam. Trị số của m...
Đọc tiếp
Hỗn hợp khí X gồm N H 3 và etylamin có tỉ khối so với C H 4 là 1,4125. Đốt cháy hoàn toàn m gam X bằng lượng không khí vừa đủ (giả sử trong không khí oxi chiếm 20%, còn lại là khí nitơ) thì thu được hỗn hợp gồm C O 2 , hơi nước và N 2 có tổng khối lượng là 43,4 gam. Trị số của m là
A. 3,39
B. 4,52
C. 5,65
D. 3,42
Hỗn hợp X gồm 2 rượu ( ancol ) CH3OH, C2H5OH có cùng số mol và 2 axit C2H5COOH, C4H8(COOH)2. Đốt cháy hoàn toàn 11,16 gam X cần vừa đủ 60,48 lít không khsi (đktc, không khí chứa 20% oxi và 80% nitơ theo thể tích) thu được hỗn hợp Y gồm khí và hơi nước. Dẫn toàn bộ Y đi qua dung dịch nước vôi trong dư, sau khi các phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch giảm m gam so với dung dịch ban đầu. Biết khí nitơ không tan trong nước, tìm giá trị của m.
Đọc tiếp
Hỗn hợp X gồm 2 rượu ( ancol ) CH3OH, C2H5OH có cùng số mol và 2 axit C2H5COOH, C4H8(COOH)2. Đốt cháy hoàn toàn 11,16 gam X cần vừa đủ 60,48 lít không khsi (đktc, không khí chứa 20% oxi và 80% nitơ theo thể tích) thu được hỗn hợp Y gồm khí và hơi nước. Dẫn toàn bộ Y đi qua dung dịch nước vôi trong dư, sau khi các phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch giảm m gam so với dung dịch ban đầu. Biết khí nitơ không tan trong nước, tìm giá trị của m.
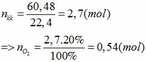
CH3OH và C2H5OH có CT chung là CnH2n+2O.
CH3OH và C2H5OH có cùng số mol nên:
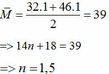
Vậy CT chung của 2 ancol là: C1,5H5O
2 axit có công thức phân tử là: C3H6O2 và C6H10O4
Nhận xét: C1,5H5O ; C3H6O2 và C6H10O4 đều có số nguyên tử C gấp 1,5 lần số nguyên tử O
Gọi số mol của CO2: x (mol) ; nH2O = y (mol)
=> nO (trong hh đầu) = 2/3 nC =2/3 nCO2 = 2x/3 (mol) ( Vì nguyên tử C gấp 1,5 lần số nguyên tử
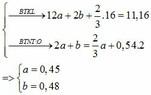
Khối lượng dung dịch giảm: ∆ = mCaCO3 – mCO2 – mH2O = 0,45.100 – 0,45.44 – 0,48.18 = 16,56 (g)
Đúng 0
Bình luận (0)
Để đốt cháy 4,7 gam hỗn hợp khí M gồm Hidro và Nitơ thì cần dùng 2,8 lít khí Oxi điều kiện tiêu chuẩn biết rằng khí nitơ không tham gia phản ứng cháy
a Tính khối lượng mỗi chất trong hỗn hợp M
b tính tỉ khối của hỗn hợp khí M đối với khí heli
a) nO2=\(\dfrac{2,8}{22,4}\)=0,125 mol
PTHH: 2H2 + O2 --to--> 2H2O
0,25<-0,125
=> mH2 = 0,25.2 = 0,5 (g)
=> mN2 = 4,7 - 0,5 = 4,2 (g)
nN2=\(\dfrac{4,2}{28}=0,15mol\)
=> ¯M=\(\dfrac{4,7}{0,15+0,25}\)=11,75 g\mol
dhh/He=\(\dfrac{11,75}{4}=\text{2 , 9375}\)
Đúng 2
Bình luận (0)
) Cho 13,44 lít hỗn hợp khí X gồm Hiđro và Axetilen(C2H2) có tỉ khối so với Nitơ bằng 0,5. Mặt khác đốt cháy hoàn toàn 5,6 gam hỗn hợp X có thành phần như trên trong bình kín chứa 28,8 gam Oxi. Phản ứng xong làm lạnh để ngưng tụ hết hơi nước thu được khí Y(thể tích các khí đo ở đktc) a. Viết PTHH b. Tính thành phần phần trăm theo thể tích và theo khối lượng của hỗn hợp Y. (Cho Al 27; C 12;Cu 64; F e 56; H 1; Mg 24; Na 23; N 14; O 16; Zn 65)
Đọc tiếp
) Cho 13,44 lít hỗn hợp khí X gồm Hiđro và Axetilen(C2H2) có tỉ khối so với Nitơ bằng 0,5. Mặt khác đốt cháy hoàn toàn 5,6 gam hỗn hợp X có thành phần như trên trong bình kín chứa 28,8 gam Oxi. Phản ứng xong làm lạnh để ngưng tụ hết hơi nước thu được khí Y(thể tích các khí đo ở đktc) a. Viết PTHH b. Tính thành phần phần trăm theo thể tích và theo khối lượng của hỗn hợp Y. (Cho Al =27; C = 12;Cu = 64; F e = 56; H = 1; Mg = 24; Na = 23; N = 14; O = 16; Zn =65)
11,2 lít hỗn hợp X gồm hiđro và metan CH4 (đktc) có tỉ khối so với oxi là 0,325.
a/ Xác định % thể tích các khí trong X?
b/ Đốt cháy hoàn toàn hỗn hợp với 32 gam khí oxi. Phản ứng xong, làm lạnh để hơi nước ngưng tụ hết được hỗn hợp khí Y.
- Viết phương trình hoá học xảy ra.
- Tính thể tích các khí trong Y.
a) Gọi số mol H2, CH4 là a, b
=> \(a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(M_X=\dfrac{2a+16b}{a+b}=0,325.32=10,4\)
=> a = 0,2 ; b = 0,3
=> \(\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,2}{0,5}.100\%=40\%\\\%V_{CH_4}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
b) \(n_{O_2}=\dfrac{32}{32}=1\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,3--->0,6------->0,3
2H2 + O2 --to--> 2H2O
0,2-->0,1
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,3.22,4=6,72\left(l\right)\\V_{O_2\left(dư\right)}=\left(1-0,6-0,1\right).22,4=6,72\left(l\right)\end{matrix}\right.\)
Đúng 4
Bình luận (0)














