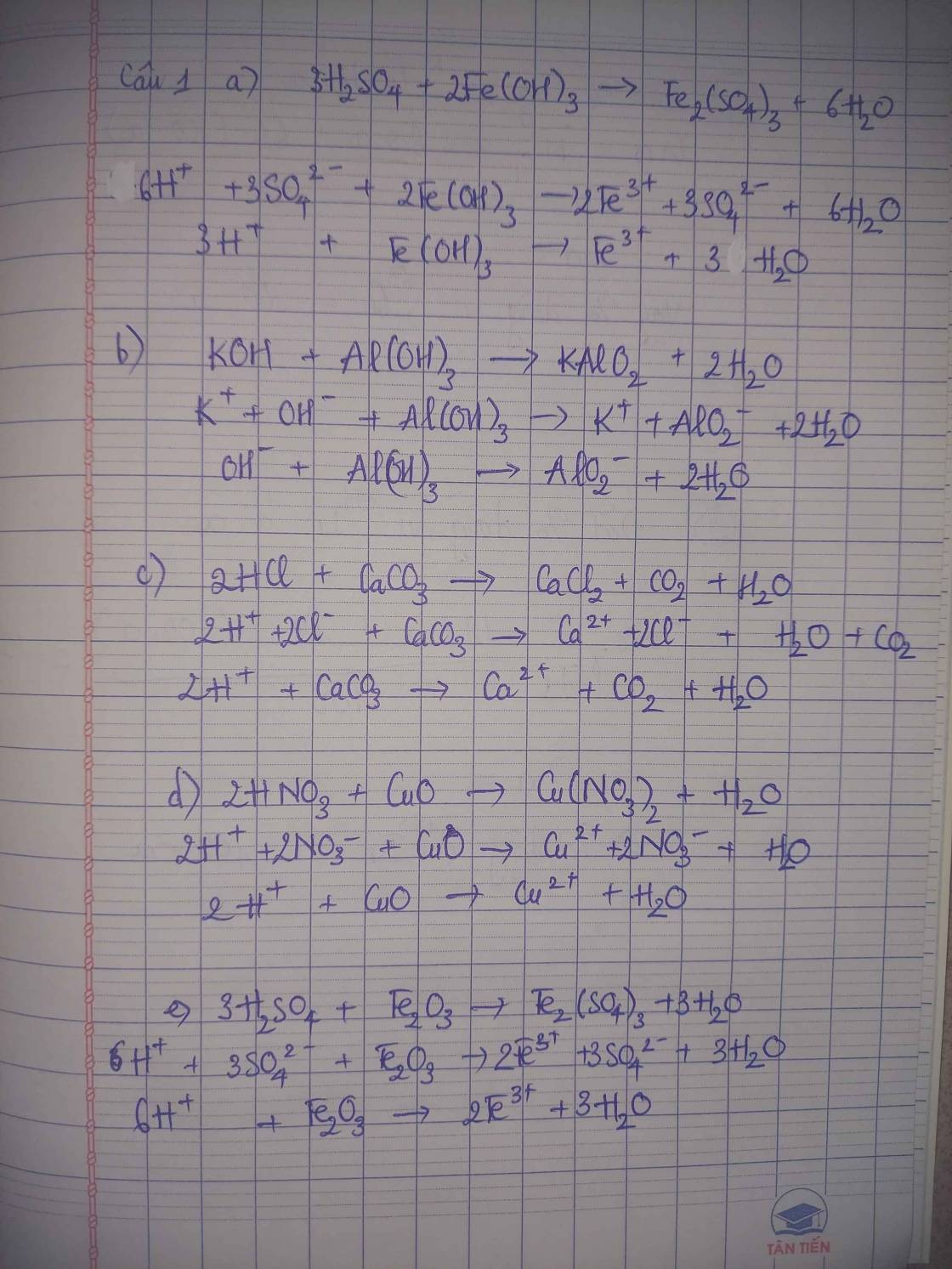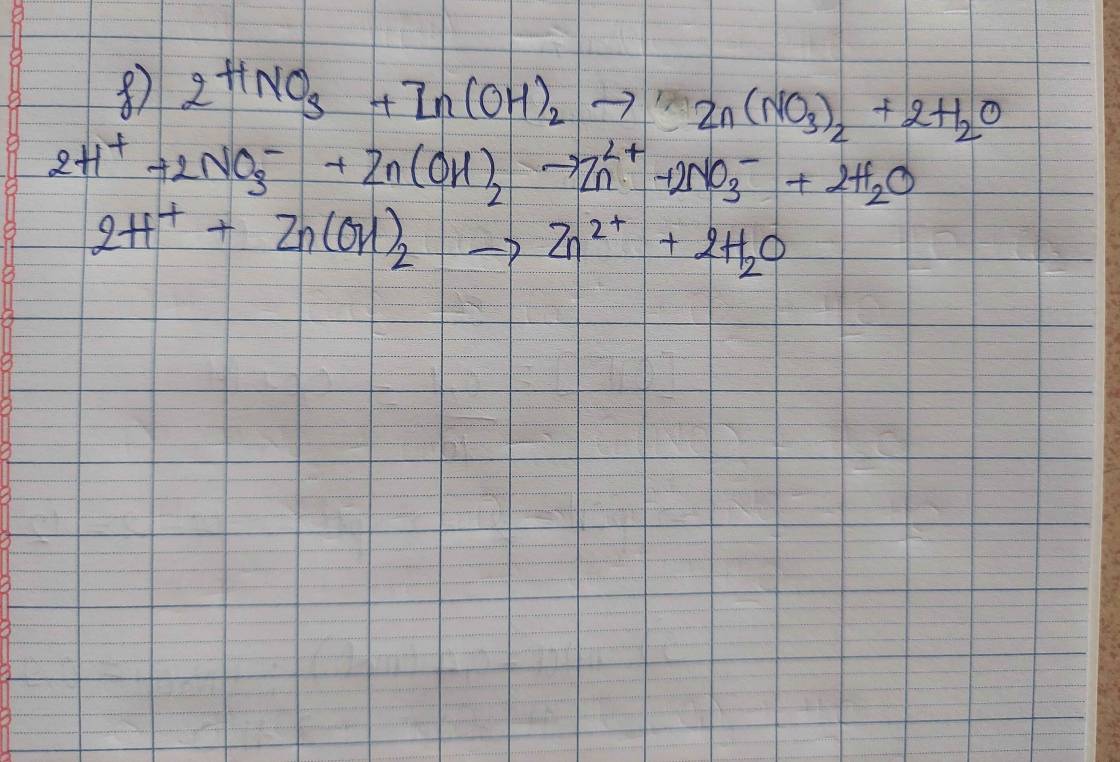viết phương trình hóa học( ghi rõ điều kiện nếu có) của phản úng Cu với HNO3 đặc nóng
Bài 4: Phản ứng trao đổi trong dung dịch các chất điện li
\(Cu+4HNO_{3\left(đ\right)}\underrightarrow{t^o}Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
Đúng 1
Bình luận (0)
Cho phản ứng: CO_{left(gright)}+Cl_{2left(gright)}⇌COCl_{2left(gright)} được thực hiện trong bình kín ở nhiệt độ không đổi, nồng độ ban đầu của CO và Cl2 bằng nhau và bằng 0,4Ma) Tính hằng số cân bằng của phản ứng biết rằng khi hệ đạt trạng thái cân bằng thì chỉ còn 50% lượng CO ban đầub) Sau khi cân bằng được thiết lập ta thêm 0,1 mol CO vào 1 lít hỗn hợp. Tính nồng độ các chất lúc cân bằng mới được thiết lập
Đọc tiếp
Cho phản ứng: \(CO_{\left(g\right)}+Cl_{2\left(g\right)}⇌COCl_{2\left(g\right)}\) được thực hiện trong bình kín ở nhiệt độ không đổi, nồng độ ban đầu của CO và Cl2 bằng nhau và bằng 0,4M
a) Tính hằng số cân bằng của phản ứng biết rằng khi hệ đạt trạng thái cân bằng thì chỉ còn 50% lượng CO ban đầu
b) Sau khi cân bằng được thiết lập ta thêm 0,1 mol CO vào 1 lít hỗn hợp. Tính nồng độ các chất lúc cân bằng mới được thiết lập
Em muốn câu trả lời từ a đến f ạ 
 Câu 2 và câu 3 ạ Giải nhanh giúp mình với ạ Mình cần gấp lắm
Câu 2 và câu 3 ạ Giải nhanh giúp mình với ạ Mình cần gấp lắm
Câu 2:
Gọi \(\left\{{}\begin{matrix}n_{Na_2CO_3}=x\left(mol\right)\\n_{Na_2SO_4}=y\left(mol\right)\end{matrix}\right.\)
PTHH:
\(Na_2CO_3+BaCl_2\rightarrow BaCO_3\downarrow+2NaCl\)
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
\(\xrightarrow[]{BT\text{ }SO_4^{2-},CO_3^{2-}}\left\{{}\begin{matrix}n_{BaCO_3}=x\left(mol\right)\\n_{BaSO_4}=y\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}106x+142y=\dfrac{6,63}{1,7}=3,9\\197x+233y=6,63\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,01\\y=0,02\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}C_{M\left(Na_2CO_3\right)}=\dfrac{0,01}{0,25}=0,04M\\C_{M\left(Na_2SO_4\right)}=\dfrac{0,02}{0,25}=0,08M\end{matrix}\right.\)
Câu 3:
Gọi \(\left\{{}\begin{matrix}n_{NaOH}=x\left(mol\right)\\n_{Na_2CO_3}=y\left(mol\right)\\n_{Na_2SO_4}=z\left(mol\right)\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}n_{HCl}=0,2.0,08=0,016\left(mol\right)\\n_{BaCl_2}=\dfrac{4,16}{208}=0,02\left(mol\right)\end{matrix}\right.\)
PTHH:
\(NaOH+HCl\rightarrow NaCl+H_2O\\ Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\\ Na_2CO_3+BaCl_2\rightarrow BaCO_3\downarrow+2NaCl\\ Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
\(\xrightarrow[]{BT\text{ }Na^+,Cl^-,CO_3^{2-},SO_4^{2-}}\left\{{}\begin{matrix}x+2y=0,016\\y+z=0,02\\208y+233z=4,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,0016\\y=0,0072\\z=0,0128\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}C\%_{NaOH}=\dfrac{0,0016.40}{80}.100\%=0,08\%\\C\%_{Na_2CO_3}=\dfrac{0,0072.106}{80}.100\%=0,954\%\\C\%_{Na_2SO_4}=\dfrac{0,0128.142}{80}.100\%=2,272\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 100ml dung dịch A chứa HCl 0,5M và H2SO4 0,5M tác dụng với 100ml dung dịch B chứa KOH 0,6M, Ba(OH)2 0,1M. Thu được dung dịch C và m(g) kết tủa. Tính pH của C và tính m.
$n_{HCl} = 0,1.0,5 = 0,05(mol)$
$n_{H_2SO_4} = 0,1.0,5 = 0,05(mol)$
$\Rightarrow n_{H^+} = 0,05 + 0,05.2 = 0,15(mol)$
$n_{KOH} = 0,1.0,6 = 0,06(mol)$
$n_{Ba(OH)_2} = 0,1.0,1 = 0,01(mol)$
$\Rightarrow n_{OH^-} = 0,06 + 0,01.2 = 0,08(mol)$
$H^+ + OH^- \to H_2O$
$n_{H^+\ pư} = n_{OH^-} = 0,08(mol) \Rightarrow n_{H^+\ dư} = 0,07(mol)$
$V_{dd\ sau\ pư} = 0,1 + 0,1 = 0,2(lít)$
$[H^+] = \dfrac{0,07}{0,2} = 0,35M$
$pH = -log(0,35) = 0,456$
$n_{SO_4^{2-}} = n_{H_2SO_4} = 0,05 > n_{Ba^{2+}} = n_{Ba(OH)_2} = 0,01$
nên $SO_4^{2-}$ dư
$n_{BaSO_4} = n_{Ba^{2+}} = 0,01(mol) \Rightarrow m = 0,01.233 = 2,33(gam)$
Đúng 2
Bình luận (0)
Tính pH của các dung dịch sau:
a/ \(HCl\) 0,0001M
b/ \(H_2SO_4\) 0,0005M
c/ \(Ba\left(OH\right)_2\) 0,0005M
`a)C_[M_[HCl]]=0,0001(M)=10^[-4](M)`
`=>[H^+ ]=10^[-4](M)`
`=>pH=4`
_____________________________________________
`b)C_[M_[H_2 SO_4]]=0,0005(M)=5.10^[-4](M)`
`=>[H^+ ]=2.5.10^[-4]=10^[-3](M)`
`=>pH=3`
_____________________________________________
`c)C_[M_[Ba(OH)_2]]=0,0005(M)=5.10^[-4](M)`
`=>[OH^- ]=2.5.10^[-4]=10^[-3](M)`
`=>[H^+ ]=[10^[-14]]/[10^[-3]]=10^[-11](M)`
`=>pH=11`
Đúng 1
Bình luận (2)
Câu 1: Viết PT dạng phân tử và ion rút gọn của các PƯ trong dd theo sơ đồ sau:a) Pbleft(NO3right)_2 + ? → PbCl_2downarrow + ?b) left(NH_4right)_2CO_3 + ? → ? + NH_3uparrow + H_2OCâu 2: Pha 80 ml dd Baleft(OHright)_2 0,25M với 20 ml dd hỗn hợp HNO_3 0,5M và H_2SO_4 0,5M, thu được dd A.a) Tìm nồng độ mol ion của dung dịch A (bỏ qua sự điện li của nước)?b) Tìm pH dung dịch A?
Đọc tiếp
Câu 1: Viết PT dạng phân tử và ion rút gọn của các PƯ trong dd theo sơ đồ sau:
a) \(Pb\left(NO3\right)_2\) + ? → \(PbCl_2\downarrow\) + ?
b) \(\left(NH_4\right)_2CO_3\) + ? → ? + \(NH_3\uparrow\) + \(H_2O\)
Câu 2: Pha 80 ml dd \(Ba\left(OH\right)_2\) 0,25M với 20 ml dd hỗn hợp \(HNO_3\) 0,5M và \(H_2SO_4\) 0,5M, thu được dd A.
a) Tìm nồng độ mol ion của dung dịch A (bỏ qua sự điện li của nước)?
b) Tìm \(pH\) dung dịch A?
Câu 1:
a) \(Pb\left(NO_3\right)_2+CaCl_2\rightarrow PbCl_2\downarrow+Ca\left(NO_3\right)_2\)
\(Pb^{2+}+2Cl^-\rightarrow PbCl_2\downarrow\)
b) \(\left(NH_4\right)_2CO_3+2KOH\rightarrow K_2CO_3+2NH_3\uparrow+H_2O\)
\(NH_4^++OH^-\rightarrow NH_3\uparrow+H_2O\)
Câu 2:
a) Ta có:
\(\left\{{}\begin{matrix}n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,08.0,25.2=0,04\left(mol\right)\\n_{H^+}=n_{HNO_3}+2n_{H_2SO_4}=0,5.0,02+0,02.0,5.2=0,03\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,08.0,25=0,02\left(mol\right)\\n_{SO_4^{2-}}=0,02.0,5=0,01\left(mol\right)\end{matrix}\right.\)
PTHH: \(H^++OH^-\rightarrow H_2O\)
0,03--->0,03
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\downarrow\)
0,01<---0,01
`=>` \(ddA:\left\{{}\begin{matrix}n_{OH^-\left(dư\right)}=0,04-0,03=0,01\left(mol\right)\\n_{Ba^{2+}\left(dư\right)}=0,02-0,01=0,01\left(mol\right)\\n_{NO_3^-}=n_{HNO_3}=0,02.0,5=0,01\left(mol\right)\end{matrix}\right.\)
Ta có: \(V_{ddA}=0,08+0,02=0,1\left(l\right)\)
`=>` \(\left[OH^-\right]=\left[Ba^{2+}\right]=\left[NO_3^-\right]=\dfrac{0,01}{0,1}=0,1M\)
b) \(pOH=-\text{log}\left(0,1\right)=1\)
`=>` \(pH=14-1=13\)
Đúng 2
Bình luận (0)
Câu 1: Trộn 30 ml dd hỗn hợp \(KOH\) 0,1 mol/l và \(Ba\left(OH\right)_2\) 0,025 mol/l với 20 ml dd \(H_2SO_4\) có nồng độ x mol/l thu được m gam kết tủa và 50 ml dd có pH = 1. Hãy tìm m và x. Giả sử \(H_2SO_4\) điện li hoàn toàn cả hai nấc.
$n_{KOH} = 0,03.0,1 = 0,003(mol)$
$n_{Ba(OH)_2} = 0,03.0,025 = 0,00075(mol)$
$\Rightarrow n_{OH^-} = 0,003 + 0,00075.2 = 0,0045(mol)$
$n_{H^+\ dư} = 0,05.10^{-1} = 0,005(mol)$
$OH^- + H^+ \to H_2O$
$n_{H^+\ pư} = n_{OH^-} = 0,0045(mol)$
$\Rightarrow n_{H^+} = 0,0045 + 0,005 = 0,0095(mol)$
$n_{H_2SO_4} = \dfrac{1}{2}n_{H^+} = 0,00475(mol)$
$x = \dfrac{0,00475}{0,02} = 0,2375M$
$Ba^{2+} + SO_4^{2-} \to BaSO_4$
$n_{BaSO_4} = n_{SO_4^{2-}} = n_{Ba(OH)_2} = 0,00075(mol)$
$m = 0,00075.233 = 0,17475(gam)$
Đúng 3
Bình luận (0)
I, Viết PTPT ứng với phương trình ion thu gọn của các PỨ sau:
(1) \(Ca^{2+}+SO_3^{2-}\rightarrow_{ }CaSO_3\downarrow\)
(2) \(NH_4^++OH^-\rightarrow_{ }NH_3\uparrow+H_2O\)
(3) \(Mg^{2+}+2OH^-\rightarrow_{ }Mg\left(OH\right)_2\downarrow\)
$(1) Ca(OH)_2 + Na_2SO_3 \to CaSO_3 + 2NaOH$
$(2) NH_4NO_3 + NaOH \to NaNO_3 + NH_3 + H_2O$
$(3) MgCl_2 + 2KOH \to Mg(OH)_2 + 2KCl$
Đúng 3
Bình luận (0)
(1) \(CaCl_2+Na_2SO_3\rightarrow CaSO_3\downarrow+2NaCl\)
(2) \(NH_4F+LiOH\rightarrow LiF+NH_3\uparrow+H_2O\)
(3) \(MgSO_4+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+K_2SO_4\)
Đúng 0
Bình luận (0)
Nhờ mng giải thích em chỗ mục 2 ạ. Em kh hiểu tại sao chỗ pt ion đầy đủ lại để nguyên Cu(OH)2 mà kh viết thành Cu2+ + OH- ạ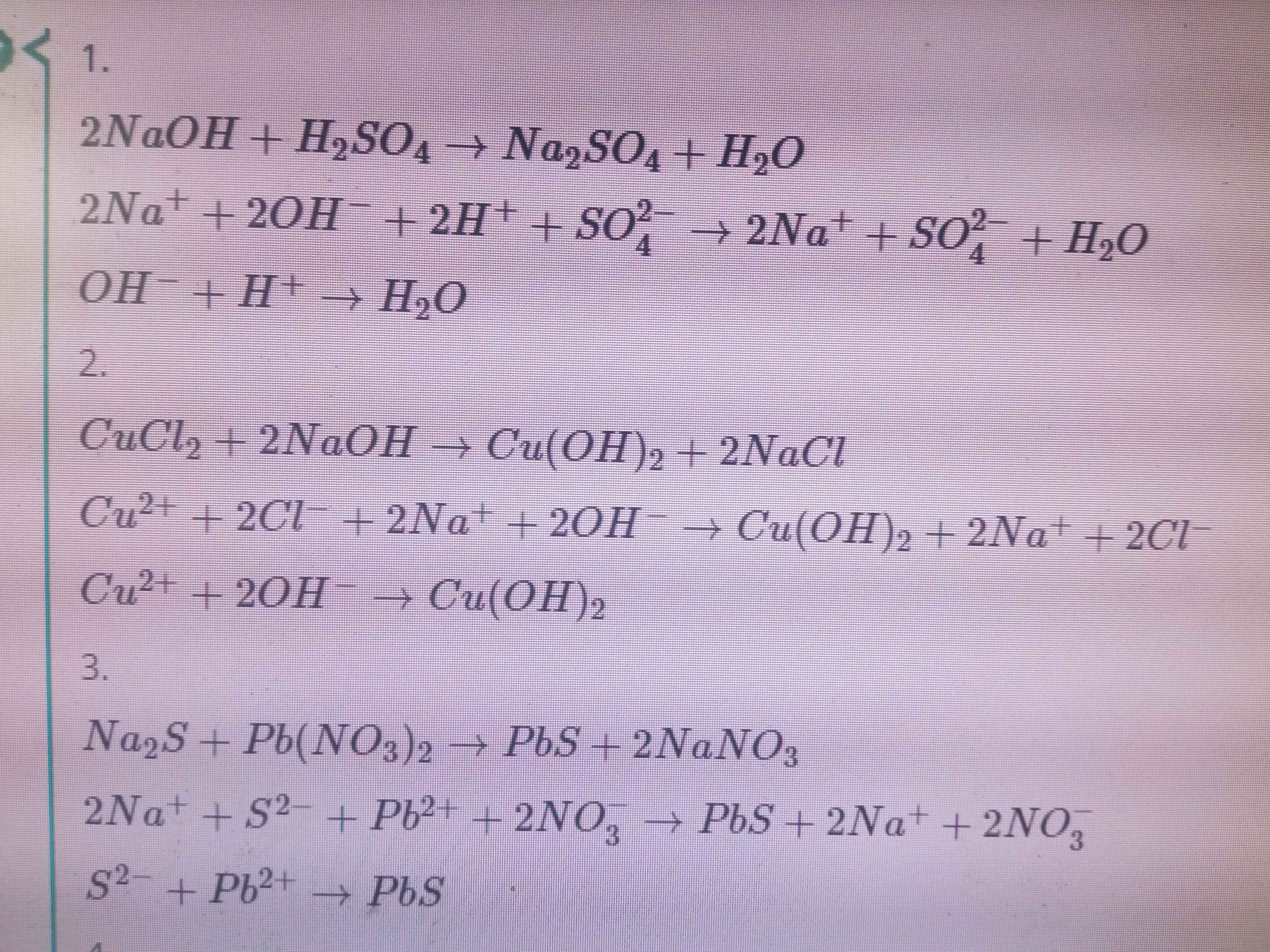
$Cu(OH)_2$ là chất điện li yếu nên khi viết phương trình ion phải giữ nguyên
Đúng 0
Bình luận (1)