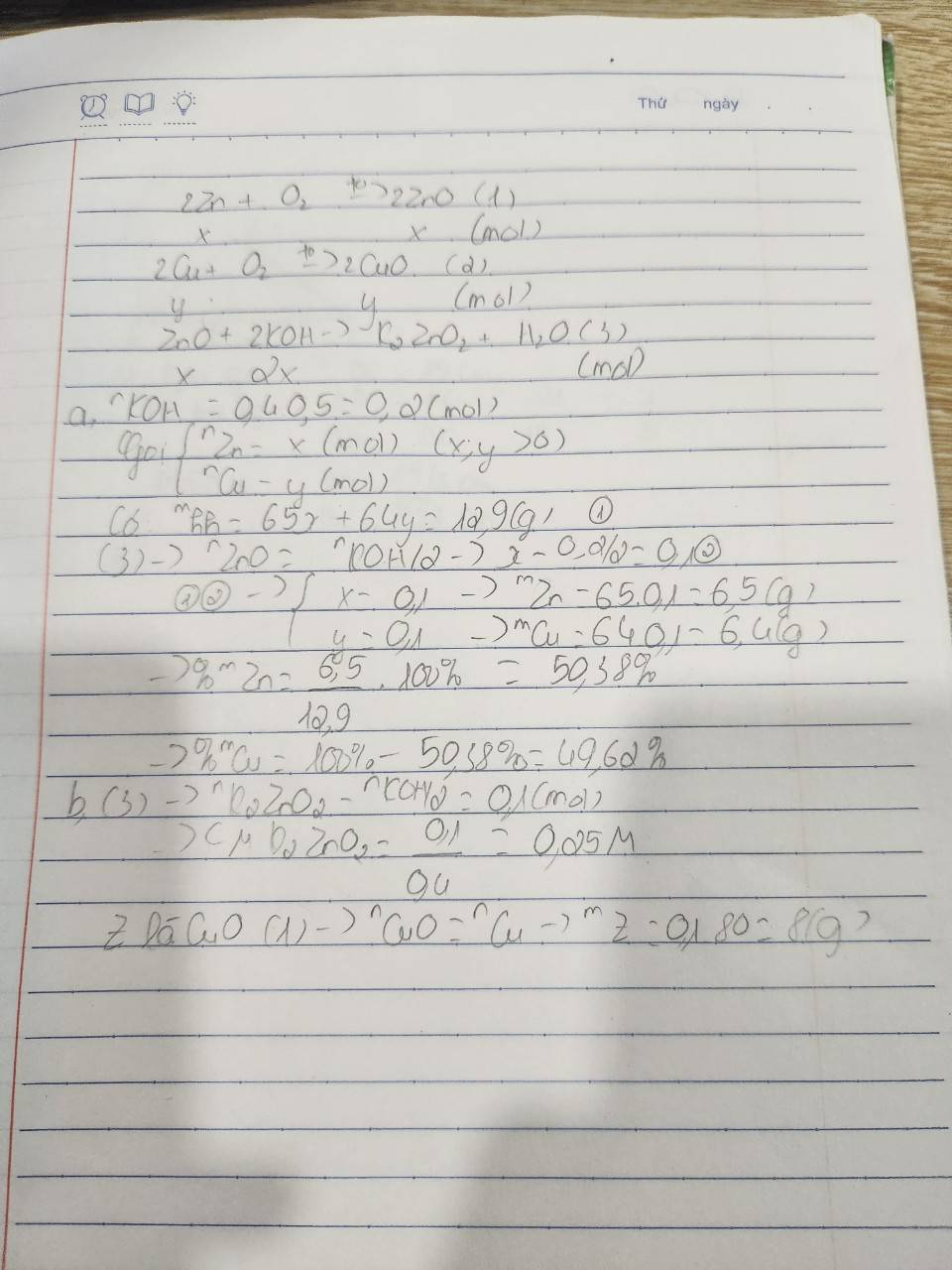nung 12,9 g hh gồm zn và cu trong oxi vừa đủ đc chất rắn X cho X td vừa đủ với 400 ml dd KOH 0,5 M đc dd Y và chất rắn Z
a, tính % mỗi kim loại trong hh ban đầu
b, tính Cm của dd Y ( giả sử thể tích dd ko đổi ) và mZ = ?
Ôn tập học kỳ II
Vì Cu là kim loại đứng sau Mg nên Cu k t/d vs axit
PTHH: Zn + H2SO4 → ZnSO4 + H2↑
Số mol của hiđrô là: 2,24 : 22,4 = 0,1 (mol)
Số mol của Zn là: 0,1 . 1 = 0,1(mol)
Khối lượng của Zn là: 0,1 . 65 = 6,5 (gam)
a) % Zn trong hỗn hợp ban đầu là:
(6,5 : 12,9) . 100% = 50,3876%
% Cu trong hỗn hợp ban đầu là:
100% - 50,3876% = 49,6124%
b) Số mol của axit là: 0,1 . 1 = 0,1(mol)
Khối lượng của axit là: 0,1 . 98 = 9,8 (gam)
C% = (9,8 : 400) . 100% = 2,45%
c) Tiếp theo áp dụng định luật bảo toàn khối lượng để tính khối lượng dung dịch muối sau phản ứng bằng cách Tính tổng khối lượng các chất phản ứng trừ đi khối lượng khí bay hơi... Từ đó ta tính được khối lượng dung dịch muối sau pứ là: 406,3(gam)
Khối lượng chất tan (khối lượng muối) là:
0,1 . 161 = 16,1 (gam)
C% của dung dịch muối sau pứ là:
16,1 : 406,3 = 3,9626%
được ko mấy pen
Đúng 0
Bình luận (1)
\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
0,1 <--------- 0,1
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(ZnO+2KOH\rightarrow K_2ZnO_2+H_2O\)
0,1<----- 0,2 --------> 0,1
\(n_{KOH}=0,4.0,5=0,2\left(mol\right)\)
\(X\left\{{}\begin{matrix}CuO\\ZnO\end{matrix}\right.+\underrightarrow{KOH}\left[{}\begin{matrix}Y:K_2ZnO_2\\Z:CuO\end{matrix}\right.\)
\(\%_{m_{Zn}}=\dfrac{65.0,1.100}{12,9}=50,39\%\)
\(\%_{m_{Cu}}=100\%-50,39\%=49,61\%\)
\(CM_{K_2ZnO_2}=\dfrac{0,1}{0,4}=0,25M\)
\(m_{Cu}=12,9-m_{Zn}=12,9-0,1.65=6,4\left(g\right)\Rightarrow n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)=n_{CuO}\)
\(m_Z=m_{CuO}=0,1.80=8\left(g\right)\)
Đề không đề cập axit, chỉ có câu a b bạn có nhầm gì không.
Đúng 1
Bình luận (0)
lấy 5,4 g nhôm cho vào V (ml) dd HCl 1M được dd X và V(l) khí Y ở đktc . Cho 200 ml dd NaOH 3,5 M vào dd X được kết tủa Z tính klg của Z
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH :
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,2
\(n_{NaOH}=0,2.3,5=0,7\left(mol\right)\)
\(3NaOH+AlCl_3\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\)
0,7 0,2 0,2
NaOH dư
\(m_{Al\left(OH\right)_3}=0,2.78=15,6\left(g\right)\)
Đúng 0
Bình luận (4)
lấy 5,4 g nhôm cho vào V (ml) dd HCl 1M được dd X và V(l) khí Y ở đktc . Cho 200 ml dd NaOH 3,5 M vào dd X được kết tủa Z tính klg của Z
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{NaOH}=0,2.3,5=0,7\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 --------------> 0,2
Nếu HCl không dư.
\(\Rightarrow ddX:AlCl_3\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3+3NaCl\)
0,2 -----> 0,6 -------> 0,2
\(\dfrac{0,2}{1}< \dfrac{0,7}{3}\) => NaOH dư.
\(n_{NaOH.dư}=0,7-0,6=0,1\left(mol\right)\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
0,1 <-------- 0,1
\(\dfrac{0,2}{1}>\dfrac{0,1}{1}\) => Kết tủa \(Al\left(OH\right)_3dư\) (hay chưa bị hòa tan hết)
\(m_Z=0,1.78=7,8\left(g\right)\)
Nếu HCl dư thì thiếu dữ kiện làm bài vì không biết ban đầu HCl bao nhiêu, nếu đề chỉ có vậy thì nói mình xem làm vì có thể nhiều trường hợp nữa lắm.
Đúng 2
Bình luận (0)
Hòa tan 11,53g hỗn hợp gồm Ba , K vào lượng nước dư , sau phản ứng xảy ra hoàn toàn thu được dung dịch và 2,464 lít khí H2 điều kiện tiêu chuẩn . Khối lượng chất tan trong dung dịch là ? Giúp em với ạ , em cần gấp
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{2,464}{22,4}=0,11\left(mol\right)\)
Đặt \(\left\{{}\begin{matrix}n_{Ba}=a\left(mol\right)\\n_K=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(PTHH:Ba+2H_2O->Ba\left(OH\right)_2+H_2\left(1\right)\)
tỉ lệ 1 ; 2 : 1 : 1
n(mol) a--------->2a----------->a---------->a
\(PTHH:2K+2H_2O->2KOH+H_2\left(2\right)\)
tỉ lệ 2 : 2 : 2 ; 1
n(mol) b---------->b---------->b------------>1/2b
Ta có Hệ phương trình sau
\(\left\{{}\begin{matrix}137a+39b=11,53\\a+\dfrac{1}{2}b=0,11\end{matrix}\right.\\ < =>\left\{{}\begin{matrix}a=0,05\\b=0,12\end{matrix}\right.\\ < =>\left\{{}\begin{matrix}n_{Ba}=0,05\left(mol\right)\\n_K=0,12\left(mol\right)\end{matrix}\right.\)
Theo Phương trình (1) ta có: \(n_{Ba\left(OH\right)_2}=a=0,05\left(mol\right)\\ =>m_{Ba\left(OH\right)_2}=n\cdot M=0,05\cdot171=8,55\left(g\right)\)
Theo phương trình (2) ta có
\(n_{KOH}=b=0,12\left(mol\right)\\ m_{KOH}=n\cdot M=0,12\cdot56=6,72\left(g\right)\\ =>m_{ct}=8,55+6,72=15,27\left(g\right)\)
Đúng 4
Bình luận (1)
Em hãy cho biết đặc điểm chung nổi bật của các nước Anh , Pháp , Đức , Mỹ vào cuối thế kỷ XIX đầu thế kỷ XX là gì ? Giúp mik vs ! Mik cảm ơn nhìu ạ 🥰
1. Tăng trưởng kinh tế: Các nước này đều đã trải qua một giai đoạn tăng trưởng kinh tế mạnh mẽ, với sự phát triển của các ngành công nghiệp, nông nghiệp và thương mại.
2. Đổi mới công nghệ: Các quốc gia này đều đã đổi mới công nghệ và ứng dụng các công nghệ tiên tiến nhất của thời đại đó như máy móc, đường sắt, tàu hỏa, ô tô...
3. Đổi mới xã hội: Các nước này đã trải qua các thay đổi xã hội đáng kể, với sự phát triển của các phong trào xã hội, các chính sách xã hội và bảo vệ lao động.
4. Tư tưởng cách mạng: Các nước này đã được ảnh hưởng bởi các tư tưởng cách mạng, như chủ nghĩa dân tộc, chủ nghĩa xã hội và chủ nghĩa tự do cá nhân.
5. Đối ngoại: Các nước này đã mở rộng quan hệ với nhiều nước.
Đúng 0
Bình luận (0)
Cho A: R2X3, X chiếm 64%, tích hạt n của A=1344, trong R (n=p+1),X(n=p). Tìm A
Cần 200 ml dung dịch HNO 3 2M và H 2 SO 4 1M để trung hòa vừa đủ V (ml) dung dịch KOH aM và Ba(OH) 2 0,5M. Sau phản ứng hoàn toàn thu được dung dịch X, cô cạn dung dịch X thu được 87g chất rắn khan. Tính V
\(n_{HNO_3}=n_{NO_3^{^-}}=0,2.2=0,4mol\\ n_{H_2SO_4}=n_{SO_4^{2-}}=0,2.1=0,2mol\\ n_{KOH}=x\left(mol\right);V_{ddBase}=v\left(L\right)\\ H^++OH^-->H_2O\\ 0,4+0,4=x+2.0,5.v\\ x+v=0,8\left(I\right)\\ m_{rắn}=62.0,4+96.0,2+39x+137.v.0,5=87\\ 39x+68,5v=43\left(II\right)\\ \Rightarrow x=v=0,4\\ V=1000v=400\left(mL\right)\)
Đúng 3
Bình luận (0)
1 dung dịch NaCl có khối lượng là 120g có C% là 40%. Xác định C% của dung dịch thu được khi:
a) Thêm 40g H2O(nước)
b) Cô đặc cho đến khi chỉ còn 100g
\(m_{NaCl\left(bd\right)}=120.0,4=48g\\ a.C\%=\dfrac{48}{120+40}.100\%=30\%\\ b.C\%=\dfrac{48}{100}.100\%=48\%\)
Đúng 2
Bình luận (0)
Cau 15: Cho khí H_{2} (dư) khử hoàn toàn 36,36 gam hỗn hợp rắn X gồm RO và F*e_{2}*O_{3} (tỉ lệ mol tương ứng là 2/1 ) thu được 31,56 gam chất rắn Y gồm 2 kim loại. Xác định kim loại R?
Gọi \(\left\{{}\begin{matrix}n_{RO}=2x\\n_{Fe_2O_3}=x\end{matrix}\right.\)
Theo đề:
\(R.2x+56.2x=31,56\)
\(\Rightarrow2x.R=31,56-112x\)
Mặt khác: \(2x.\left(R+16\right)+160x=36,36\)
\(\Leftrightarrow2xR+32x+160x=36,6\Leftrightarrow31,56-112x+32x+160x=36,36\)
=> x = 0,06
\(\Rightarrow R=\dfrac{31,56-112.0,06}{2.0,06}=207\)
Vậy kim loại R là Pb (chì).
Đúng 1
Bình luận (0)
Cho | 20°C | 100°C S CuSO4 | 75,4 | 20,7 a) Cho 400(g) dd CuSO4 bão hoà ở 100°C . Đưa về 20°C tính KL CuSO4 .5H2O tách ra? b) cho m(g) dd CuSO4 bão hoà ở 100°C đưa về 20° C có 6,25(g) CuSO4 .5H2O tách ra.Tính m?