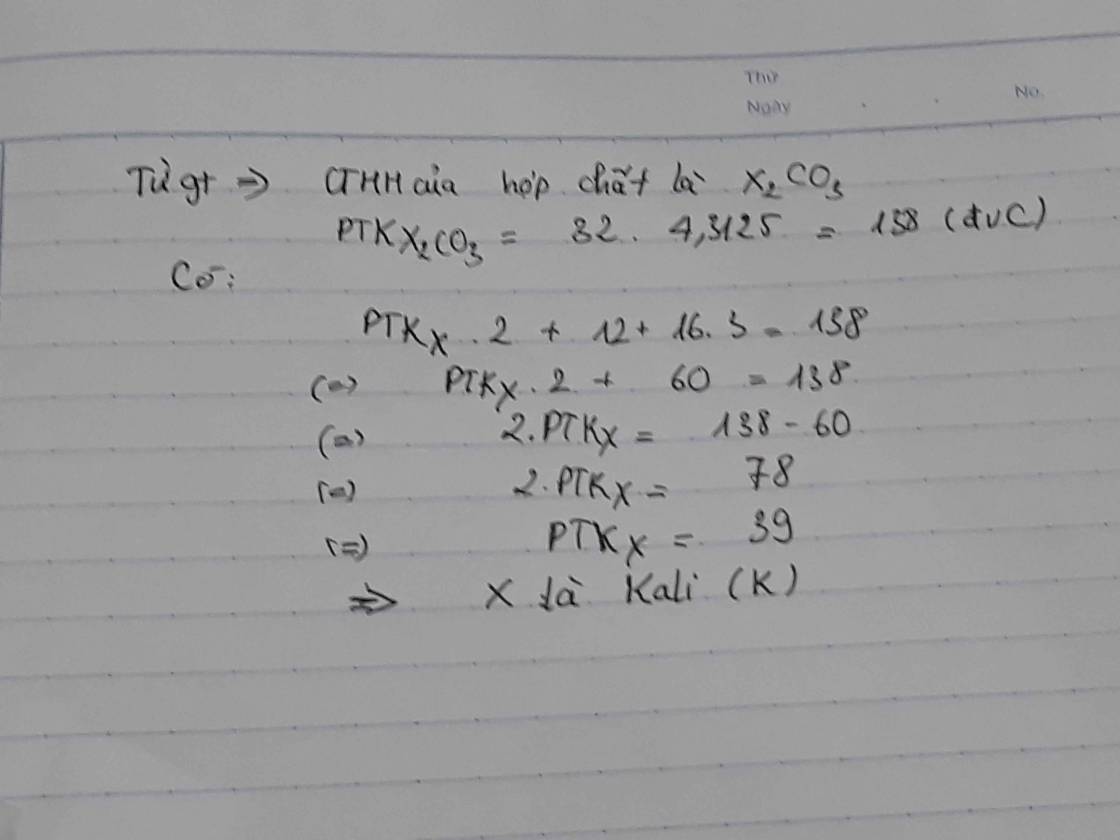Nung 20 gam calcium carbonate (thành phần chính là đá vôi) thu đc khí carbondioxit và m gam vôi sống.giải thiết hiệu xuất phản ứng là 80% xác định m.
Kiểm tra 1 tiết chương I-Đề 1
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
PT: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
Theo PT: \(n_{CaO\left(LT\right)}=n_{CaCO_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{CaO\left(LT\right)}=0,2.56=11,2\left(g\right)\)
Mà: H = 80%
\(\Rightarrow m=m_{CaO\left(TT\right)}=11,2.80\%=8,96\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan 15g BaCl vào nước đẻ được 200g dung dịch . HÃy tính nồng độ phân trăm của dung dịch thu được
\(m_{ddBaCl_2}=15+200=215\left(g\right)\)
\(C\%=\dfrac{15}{215}.100\%\approx6,98\%\)
Đúng 2
Bình luận (0)
phan tu hop chat gon 2 nguyen tu cua nguyen to x lien ket voi 1 nguyen tu carbon va 3 nguyen tu oxygen .biet khoi luong phan tu nang hon phan tu oxygen la 4,3125 lan.tim KHHH cua x
Ta có: Hợp chất gồm 2 nguyên tử nguyên tố X liên kết với 1 nguyên tử C và 3 nguyên tử O.
→ Hợp chất có CTHH là X2CO3.
Mà: \(M_{hc}=4,3125.32=138\left(g/mol\right)\)
\(\Rightarrow2M_X+12+16.3=138\Rightarrow M_X=39\left(g/mol\right)\)
Vậy: X là K.
Đúng 2
Bình luận (0)
Hãy lập PTHH cho các sơ đồ sau : NaOH+Fe2(SO4)3--->Fe(OH)3+Na2SO4 . Mg+AgNO3--->Mg(NO3)2+Ag
\(6NaOH+Fe_2\left(SO_4\right)_3->2Fe\left(OH\right)_3+3Na_2SO_4\)
\(Mg+2AgNO_3->Mg\left(NO_3\right)_2+2Ag\)
Đúng 2
Bình luận (0)
1,5 mol phân tử khối của hợp chất CaCO3 có số phân tử là bao nhiêu
1,5 mol phân tử khối hợp chất CaCO\(_3\)chứa: 1,5.6.10\(^{23}\)=9.10\(^{23}\)phân tử
Đúng 2
Bình luận (1)
một vận động vien xe đạp thực hiện cuộc đua vượt đèo như sau :
-đoạn lên đèo dài 45 km chạy hết 2 giờ 30 phút
-đoạn xuống đèo dài 30 km chạy hết 30 phút
hãy tính vận tốc trung bình của vận động viên này trên doạn lân đèo , trên đoạn xuống đèo và trên cả quãng đường đua
đốt cháy hoàn toàn 2,7 gam (al) cần dùng m trên gam khí oxygen (o2)thu đc 5,1 gam al2o3)
a)tính giá trị m của khí oxygen
\(PTHH:4Al+3O_2-^{t^o}>2Al_2O_3\)
áp dụng ĐLBTKL ta có
\(m_{Al}+m_{O_2}=m_{Al_2O_3}\\ =>m_{O_2}=m_{Al_2O_3}-m_{Al}\\ =>m_{O_2}=5,1-2,7\\ =>m_{O_2}=2,4\left(g\right)\)
Đúng 2
Bình luận (0)
thực hiện các yêu cầu sau:
a.tính khối lượng của 0,1 mol CaO
b.tính thể tích của 0,3 molkhis O2 (đktc )
c.tính sô mol của 13 gram kim lọi kẽm (Zn)
d.quả bóng bay nếu bơm bằng khí carbonic CO2rồi cột chặt ,khi ta thả tay ra bóng sẽ bay lên hay rơi xuống ?vì sao ?
a) \(m_{CaO}=n.M=0,1.56=5,6\left(g\right)\)
b) \(V_{O_2\left(đktc\right)}=n.22,4=0,3.22,4=6,72\left(l\right)\)
c) \(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
d) Vì \(d_{CO_2/kk}=\dfrac{44}{29}=1,517\)
=> CO2 nặng hơn không khí nên bóng sẽ rơi xuống
Đúng 2
Bình luận (0)
\(a)m_{CaO}=n.M=0,1.56=5,6\left(g\right)\)
\(b)V_{O_2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
\(c)n_{Zn}=m:M=13:65=0,2\left(mol\right)\)
Đúng 0
Bình luận (0)
Cần dùng bao nhiêu lít O2 ở (đktc) để đốt cháy hoàn toàn 23,4 gam hỗn hợp nhôm và Magie. Biết tỷ lệ về khối lượng của nhôm và magie là 9:4. (hướng dẫn A + O2 -- >A2Ox x là hoá trị của A)
Gọi a là số mol Al
⇒ \(m_{Mg}=27a.\dfrac{4}{9}=12a\left(g\right)\)
\(\Rightarrow n_{Mg}=\dfrac{12a}{24}=0,5a\left(mol\right)\)
\(m_{hh}=27a+12a=23,4\left(g\right)\)
⇒ a = 0,06
\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
\(2Mg+O_2\xrightarrow[]{t^o}2MgO\)
\(n_{O_2}=\dfrac{3}{4}n_{Al}+\dfrac{1}{2}n_{Mg}=\dfrac{3}{4}.0,06+\dfrac{1}{2}.0,03=0,06\left(mol\right)\)
\(V_{O_2\left(đktc\right)}=0,06.22,4=1,344\left(l\right)\)
Đúng 1
Bình luận (0)
Câu 7. Điền công thức hóa học thích hợp vào chỗ trống?a/ Na (I)Mg (II)Al (III)Cu (II)H (I)Ag (I)OH (I) SO4 (II) Cl (I) PO4 (III) b/ K (I)Zn (II)Mg (II)Fe (III)Ba (II)Cl (I) CO3 (II) NO3 (I)
Đọc tiếp
Câu 7. Điền công thức hóa học thích hợp vào chỗ trống?
a/
| Na (I) | Mg (II) | Al (III) | Cu (II) | H (I) | Ag (I) |
OH (I) |
|
|
|
|
|
|
SO4 (II) |
|
|
|
|
|
|
Cl (I) |
|
|
|
|
|
|
PO4 (III) |
|
|
|
|
|
|
b/
| K (I) | Zn (II) | Mg (II) | Fe (III) | Ba (II) |
Cl (I) |
|
|
|
|
|
CO3 (II) |
|
|
|
|
|
NO3 (I) |
|
|
|
|
|
| Na (I) | Mg (II) | Al (III) | Cu (II) | H (I) | Ag (I) |
OH (I) | NaOH | Mg(OH)2 | Al(OH)3 | Cu(OH)2 | H2O | AgOH |
SO4 (II) | Na2(SO)4 | Mg(SO)4 | Al2(SO4)3 | Cu(SO4) | H2(SO4) | Ag2(SO4) |
Cl (I) | NaCl | MgCl2 | AlCl3 | CuCl2 | HCl | AgCl |
PO4 (III) | Na3(PO4) | Mg3(PO4)2 | Al(PO4) | Cu3(PO4)2 | H3(PO4) | Ag3(PO4) |
Đúng 2
Bình luận (0)
| K (I) | Zn (II) | Mg (II) | Fe (III) | Ba (II) |
Cl (I) | KCl | ZnCl2 | MgCl2 | FeCl3 | Cl2Ba |
CO3 (II) | K2(CO3) | Zn(CO3) | Mg(CO3) | Fe2(CO3)3 | Ba(CO3) |
NO3 (I) | K(NO3) | Zn(NO3)2 | Mg(NO3)2 | Fe(NO3)3 | Ba(NO3)2 |
Đúng 1
Bình luận (0)
a/
| Na (I) | Mg (II) | Al (III) | Cu (II) | H (I) | Ag (I) |
OH (I) | NaOH | Mg(OH)2 | Al(OH)3 | Cu(OH)2 | HOH | AgOH |
SO4 (II) | \(Na_2SO_4\) | \(MgSO_4\) | \(Al_2\left(SO_4\right)_3\) | \(CuSO_4\) | \(H_2SO_4\) | \(Ag_2SO_4\) |
Cl (I) | \(NaCl\) | \(MgCl_2\) | \(AlCl_3\) | \(CuCl_2\) | \(HCl\) | \(AgCl\) |
PO4 (III) | \(Na_3PO_4\) | \(Mg_3\left(PO_4\right)_2\) | \(AlPO_4\) | \(Cu_3\left(PO_4\right)_2\) | \(H_3PO_4\) | \(Ag_3PO_4\) |
b/
| K (I) | Zn (II) | Mg (II) | Fe (III) | Ba (II) |
Cl (I) | \(KCl\) | \(ZnCl_2\) | \(MgCl_2\) | \(FeCl_3\) | \(BaCl_2\) |
CO3 (II) | \(K_2CO_3\) | \(ZnCO_3\) | \(MgCO_3\) | \(Fe_2\left(CO_3\right)_3\) | \(BaCO_3\) |
NO3 (I) | \(KNO_3\) | \(Zn\left(NO_3\right)_2\) | \(Mg\left(NO_3\right)_2\) | \(Fe\left(NO_3\right)_3\) | \(Ba\left(NO_3\right)_2\) |
Đúng 1
Bình luận (1)