Câu 1
a. Có một hỗn hợp rắn gồm KHCO3 và K2CO3, hòa tan hỗn hợp này vào nước được dung dịch A chứa x mol KHCO3 và y mol K2CO3.
- Nếu cho thêm (x+y) mol BaCl2 vào dung dịch A thu được m1 gam kết tủa.
- Nếu cho thêm (x+y) mol Ba(OH)2 vào dung dịch A thu được m2 gam kết tủa.
Hãy so sánh m1 và m2. Giải thích.




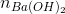 + n
+ n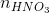 )
)







