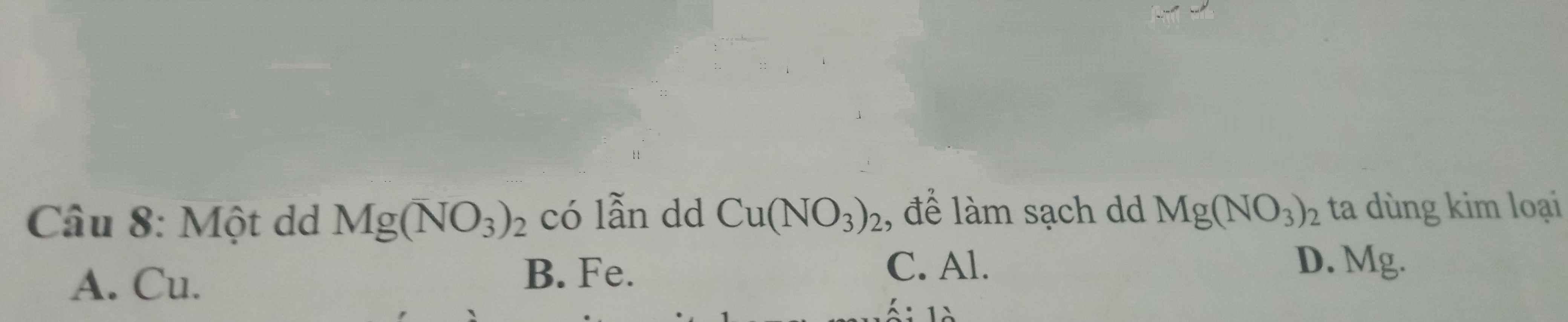Đề kiểm tra cuối học kì II
Đáp án C
- mẫu thử nào tạo kết tủa trắng là $H_2SO_4$
- mẫu thử không hiện tượng là HCl
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
Đúng 0
Bình luận (0)
tạo kết tủa : H2SO4
không hiện tượng HCl
\(PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow2HCl\)
Đúng 0
Bình luận (0)
`A. Ca(OH)_2`
`Ca(OH)_2 + SO_2 -> CaSO_3 + H_2O`
Đúng 0
Bình luận (0)
Câu 9 A
vì để loại bỏ khí SO2 ta cần cho chúng tác dụng với 1 trong những chất trên
\(PTHH:Ca\left(OH\right)_2+SO_2\rightarrow CaSO_3+H_2O\)
Đúng 0
Bình luận (0)
Đáp án A
$Ca(OH)_2 + SO_2 \to CaSO_3 + H_2O$
Khí $SO_2$ bị hấp thụ hết khi đi qua dung dịch $Ca(OH)_2$
Đúng 0
Bình luận (0)
cho Đồng (II) oxit vào dung dịch axit clohiđric có hiện tượng gì xảy ra? A.sủi bọt B.xuất hiện dung dịch màu xanh C.xuất hiện dung dịch không màu D.xuất hiện dung dịch màu nâu đỏ
B
\(PTHH:CuO+HCl\rightarrow CuCl_2+H_2O\)
Đúng 0
Bình luận (1)
Cho 150 ml dung dịch H2SO4 1m vào 300 ml dung dịch NaOH 0,5 m. Nếu cho quỳ tím vào dung dịch sau phản ứng thì quỳ tím chuyển sang: A. màu tím B. màu đỏ C.màu vàng nhạt D. màu đỏ
`2NaOH + H_2 SO_4 -> Na_2 SO_4 + 2H_2 O`
`n_[H_2 SO_4]=0,15.1=0,15(mol)`
`n_[NaOH]=0,5.0,3=0,15(mol)`
Có: `[0,15]/2 < [0,15]/1->H_2 SO_4` dư
Vậy nếu cho quỳ tím vào dd sau p/ứ thì quỳ tím sẽ chuyển sang màu đỏ do `H_2 SO_4` dư
`->\bb D`
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 200 ml dung dịch KOH trong 200 gam dung dịch axit sunfuric (H2SO4) 4,9% thu được dung dịch muối natri sunfat Ka2SO4 và nước a/ viết phương trình hóa học của phản ứng b/ Tính nồng độ mol của dung dịch KOH đã tham gia phản ứng? c/Tính khối lượng K2SO4 tạo thành?
`a)PTHH:`
`2KOH + H_2 SO_4 -> K_2 SO_4 + 2H_2 O`
`0,2` `0,1` `0,1` `(mol)`
`b)n_[H_2 SO_4]=[4,9.200]/[98.100]=0,1(mol)`
`=>C_[M_[KOH]]=[0,2]/[0,2]=1(M)`
`c)m_[K_2 SO_4]=0,1.174=17,4(g)`
Đúng 0
Bình luận (0)
Chọn D. Mg
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
Lọc lấy kết tủa ra, ta thu được dung dịch Mg(NO3)2 tinh khiết
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,0 gam MgO cần dùng V lít dd HCl 0,4M. Giá trị của V là: A.0,5 B.0,25 C. 2,24 D.4, 48
`MgO + 2HCl -> MgCl_2 + H_2 O`
`0,1` `0,2` `(mol)`
`n_[MgO]=4/40=0,1(mol)`
`=>V_[dd HCl]=[0,2]/[0,4]=0,5(l)`
`->\bb A`
Đúng 0
Bình luận (0)
$n_{MgO} = \dfrac{4}{40} = 0,1(mol)$
$MgO + 2HCl \to MgCl_2 + H_2O$
$n_{HCl} = 2n_{MgO} = 0,2(mol)$
$\Rightarrow V_{dd\ HCl} = \dfrac{0,2}{0,4} = 0,5(lít)$
Đáp án A
Đúng 0
Bình luận (0)
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- mẫu thử nào hoá xanh là $NaOH$
Cho dung dịch $BaCl_2$ vào hai mẫu thử còn
- mẫu thử nào tạo kết tủa trắng là $Na_2SO_4$
$Na_2SO_4 + BaCl_2 \to BaSO_4 + 2NaCl$
- mẫu thử nào không tạo hiện tượng gì là $NaCl$
Đúng 0
Bình luận (0)
11-A
\(H_2SO_4+Na_2SO_3\rightarrow Na_2SO_4+SO_2+H_2O\)
Đúng 1
Bình luận (0)
Câu 14 :
$Ba(OH)_2 + Na_2SO_4 \to BaSO_4 + 2NaOH$
Ta thấy :
$n_{Ba(OH)_2} = 0,1.1 = 0,1 > n_{Na_2SO_4} = 0,1.0,8 = 0,08$ nên $H_2SO_4$ dư
$n_{BaSO_4} = n_{Na_2SO_4} = 0,08(mol) \Rightarrow m_{BaSO_4} = 0,08.233 = 18,64(gam)$
Đáp án B
Câu 15 :
$Na_2CO_3 + H_2SO_4 \to Na_2SO_4 + CO_2 + H_2O$
Ta thấy :
$n_{CO_2} = n_{H_2SO_4} = 0,1(mol)$
$V_{CO_2} = 0,1.22,4 = 2,24(lít)$
Đáp án A
Đúng 1
Bình luận (0)
\(14.n_{Ba\left(OH\right)_2}=0,1\left(mol\right),n_{Na_2SO_4}=0,08\left(mol\right)\\ Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\\ LTL:\dfrac{0,1}{1}>\dfrac{0,08}{1}\Rightarrow Ba\left(OH\right)_2dư\\ m_{kt}=0,08.233=18,64\left(g\right)\\ \Rightarrow ChọnB\\ 15.n_{H_2SO_4}=0,1\left(mol\right)\\ H_2SO_4+Na_2CO_3\rightarrow Na_2SO_4+CO_2+H_2O\\ n_{CO_2}=n_{H_2SO_4}=0,1\left(mol\right)\\ \Rightarrow V_{CO_2}=0,1.22,4=2,24\left(l\right)\\ \Rightarrow ChọnA\)
Đúng 0
Bình luận (0)