

Đề kiểm tra 1 tiết chương I: Oxit-Axit -Đề 1
1A
2C
3C
4A
5D
6/
a)\(2Cu + O_2 \rightarrow^{t^o} 2CuO\)
b)\(CuCl_2 + 2NaOH \rightarrow Cu(OH)_2 + 2NaCl\)
c)\(Fe_2(SO_4)_3 + 3BaCl_2 \rightarrow 3BaSO_4 + 2FeCl_3\)
d)\(2Fe(OH)_3 \rightarrow^{t^o} Fe_2O_3 + 3H_2O\)
e)\(Fe + 2HCl \rightarrow FeCl_2 + H_2\)
Đúng 0
Bình luận (0)
hoà tan hoàn toàn 16 gam hỗn hợp bột mgo và cuo cần 24,5 gam dung dịch h2so4 tính khối lượng mỗi oxit trong hỗn hợp?
Cho 38 g gam MgCl2 tác dụng với NaOH thu được chất kết tủa Mg(OH)2 + NaCl sau phản ứng lọc kết tủa nung đến khối lượng không đổi m gam chất rắn a) Viết phương trình phản ứng xảy ra b) Tính khối lượng Mg(OH)2 thu được ở phản trình 1 c) Tính khối lượng m nhỏ thu được ở phản ứng 2 Biết Mg bằng 24 Cl bằng 35,5 o2 bằng 16 H bằng 1 Na bằng 23
\(a,n_{MgCl_2}=\dfrac{38}{24+35,5\cdot2}=0,4\left(mol\right)\\ PTHH:MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\\ TL:......1........2........1.......2\\ BR:.....0,4.......0,8........0,4........0,8\left(mol\right)\)
\(b,m_{Mg\left(OH\right)_2}=0,4\cdot\left(24+17\cdot2\right)=23,2\left(g\right)\\ c,PTHH:Mg\left(OH\right)_2\rightarrow^{t^0}MgO+H_2O\)
Theo PTHH ta có \(n_{Mg\left(OH\right)_2}=n_{MgO}=0,4\left(mol\right)\)
\(\Rightarrow m_{đề}=m_{MgO}=40\cdot0,4=16\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 38 g gam MgCl2 tác dụng với NaOH thu được chất kết tủa Mg(OH)2 + NaCl sau phản ứng lọc kết tủa nung đến khối lượng không đổi m gam chất rắn a) Viết phương trình phản ứng xảy ra b) Tính khối lượng MgOH thu được ở phản trình 1 c) Tính khối lượng m nhỏ thu được ở phản ứng 2 Biết Mg bằng 24 Cl bằng 35,5 o2 bằng 16 H bằng 1 Na bằng 23
a)
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
$Mg(OH)_2 \xrightarrow{t^o} MgO + H_2O$
b)
$n_{Mg(OH)_2} = n_{MgCl_2} = \dfrac{38}{95} = 0,4(mol)$
$m_{Mg(OH)_2} = 0,4.58 = 23,2(gam)$
c)
$n_{MgO} = n_{MgCl_2} = 0,4(mol)$
$m_{MgO} = 0,4.40 = 16(gam)$
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 17,6g hỗn hợp bột Cu và Fe vào 200g dung dịch HCl sau phản ứng thu được 6,4g chất rắn a) Viết PTHH b) Tính thể tích H2 (đktc) và phần trăm theo khối lượng của mỗi KL trong hỗn hợp ban đầu c) Hãy tính nồng độ % dd muối thu được sau phản ứng
Câu 16: Cho một lượng sắt vào 150 ml dung dịch H2SO4 loãng. Phản ứng xong thu được 6,72 lít khí ở đkxc. a) Viết phương trình hóa học. b) Tính khối lượng sắt đã tham gia phản ứng. c) Tính nồng độ mol của dung dịch axit đã dùng và khối lượng muối thu được sau phản ứng.
Đọc tiếp
Câu 16: Cho một lượng sắt vào 150 ml dung dịch H2SO4 loãng. Phản ứng xong thu được 6,72 lít khí ở đkxc. a) Viết phương trình hóa học. b) Tính khối lượng sắt đã tham gia phản ứng. c) Tính nồng độ mol của dung dịch axit đã dùng và khối lượng muối thu được sau phản ứng.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
a)\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3 0,3 0,3
b) \(m_{Fe}=0,3\cdot56=16,8\left(g\right)\)
c) \(C_{M_{H_2SO_4}}=\dfrac{n_{H_2SO_4}}{V_{H_2SO_4}}=\dfrac{0,3}{0,15}=2M\)
\(m_{FeSO_4}=0,3\cdot\left(56+32+4\cdot16\right)=45,6\left(g\right)\)
Đúng 2
Bình luận (2)
Đọc tiếp
Do Cu không pư HCl
\(Zn + 2HCl \rightarrow ZnCl_2 + H_2\)
\(n_{H_2}= \dfrac{1,12}{22,4}= 0,05 mol\)
Theo PTHH:
\(n_{Zn}= n_{H_2}= 0,05 mol\)
\(\Rightarrow m_{Zn}= 0,05 . 65=3,25g\)
\(\rightarrow m_{Cu}= 6,45 - 3,25 =3,2 g\)
Đúng 0
Bình luận (0)
Một loại muối có thành phần các nguyên tố38,6%;k 13,8%;N 47,6 còn lại là oxi .Hãy xác định công thức hóa học của muối đó.Biết khối lượng mol của muối là 101g
Bạn có thể ghi rõ lại % từng nguyên tố được không bạn
Đúng 0
Bình luận (0)
Làm e từ câu 14 đến 23 ạ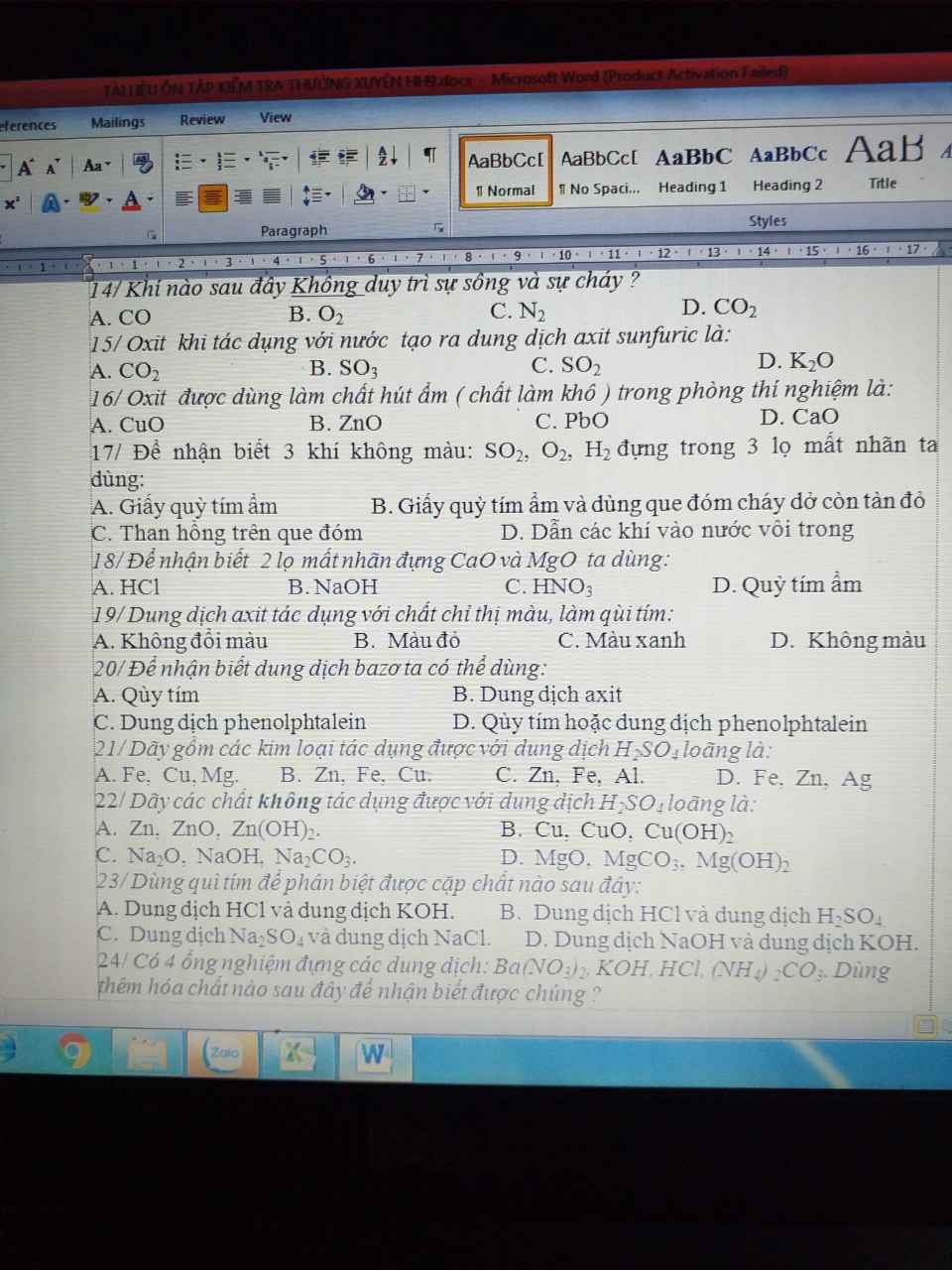
Câu 3 : Cho 7,437 lit SO2 (ở 25 0C, 1 bar) tác dụng vừa đủ với dd Ba(OH)2 2M để tạo kết tủa
Viết phương trình hóa học.
Tính thể tích dd Ba(OH)2 đã phản ứng
Tính khối lượng kết tủa thu được
(Ba = 137, O =16, H = 1)
























