Có hợp chất công thức là K2 Cr2 O7. Muối R2 Cr2 O7 có khổi lượng phân tử là 252 amu. Tìm công thức và cho biết số nguyên tử có trong một phân tử muối trên
CHƯƠNG I: CHẤT - NGUYÊN TỬ - PHÂN TỬ
\(M_{R_2Cr_2O_7}=252\)
=>2R+52*2+7*16=252
=>2R=36
=>R=18
=>R là Ag
Công thức là \(Ag_2Cr_2O_7\)
Đúng 0
Bình luận (0)
Ta có:
PTK(\(R_2Cr_2O_7\)) = 252 amu
\(\Rightarrow2.M_R+52.2+16.7=252\\ \Leftrightarrow M_R=108\left(amu\right)\)
⇒R là Ag (Argentum)
Đúng 0
Bình luận (0)
tính khối lượng ra g của 2 phân tử khí oxygen
Ta có: \(n_{O_2}=\dfrac{2}{6.10^{23}}\left(mol\right)\)
\(\Rightarrow m_{O_2}=\dfrac{2}{6.10^{23}}.32\approx1,067.10^{-22}\left(g\right)\)
Đúng 1
Bình luận (0)
Tổng số hạt trong nguyên tử là 28,trong đó số hạt không mang điện chiếm xấp xỉ 35%.Tính số hạt mỗi loại.Vẽ sơ đồ cấu tạo nguyên tử
Số hạt không mang điện :
\(n=28.35\%\approx10\) ( hạt )
Số hạt mang điện :
\(28-10=18\) ( hạt )
\(\rightarrow p=e=9\) ( hạt )
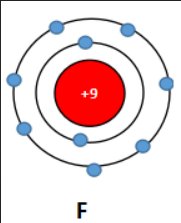
Đúng 2
Bình luận (0)
Tổng số hạt trong nguyên tử là 28, có:
\(2p+n=28\left(1\right)\)
Số hạt không mang điện chiếm xấp xỉ 35%, có:
\(\dfrac{n}{2p+n}.100\%=35\%\\ \Leftrightarrow0,7p-0,65n=0\left(2\right)\)
Từ (1), (2) có hệ phương trình: \(\left\{{}\begin{matrix}2p+n=28\\0,7p-0,65n=0\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}2p+n=28\\2p-\dfrac{13}{7}n=0\end{matrix}\right.\)
\(\Leftrightarrow\dfrac{20}{7}n=28\Rightarrow n=28:\dfrac{20}{7}=10\left(hạt\right)\) (do lấy xấp xỉ 35% nên làm tròn 9,8 thành 10)
\(\Rightarrow p=e=\dfrac{28-n}{2}=\dfrac{28-10}{2}=9\) (hạt)
Do có p = 9 nên nguyên tử là F (Flo) và F có 9 electron, 2 e lớp trong cùng và 7 e lớp ngoài cùng (bạn tự vẽ sơ đồ cấu tạo nguyên tử há: )
Đúng 0
Bình luận (0)
Nguyên tử M có số n nhiều hơn số p là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10.Xác định cấu tạo nguyên tử.Đối chiếu bảng các nguyên tố hóa học xem M là nguyên tố nào
Nguyên tử M có số n nhiều hơn số p là 1, có:
\(n-p=1\left(1\right)\)
Số hạt mang điện nhiều hơn số hạt không mang điện là 10 trong nguyên tử M, có:
\(2p-n=10\Leftrightarrow-n+2p=10\left(2\right)\)
Từ (1), (2) có hệ phương trình: \(\left\{{}\begin{matrix}n-p=1\\-n+2p=10\end{matrix}\right.\)
<=> p = 1+ 10 = 11
=> n = p + 1 = 11 + 1 = 12
Do có p = 11 nên nguyên tử M có 11 electron, 2 e lớp trong cùng, 8 e lớp giữa và 1 e lớp ngoài cùng (bạn tự vẽ cấu tạo há: )
Đối chiếu bảng tuần hoàn hóa học, M có số proton là 11 nên M là nguyên tố Na.
Đúng 2
Bình luận (0)
Bài 1 : Phân tử oxit X ( hóa trị III) nặng bằng tổng của 2 phân tử canxi và 11 phân tử khí hidro. Hãy xác định nguyên tố X.
\(CTTQ:X_2O_3\\ PTK_{X_2O_3}=2.NTK_{Ca}+11.PTK_{H_2}=2.40+11.2=102\left(đ.v.C\right)\\ Mà:PTK_{X_2O_3}=2NTK_X+3.NTK_O=2.NTK_X+3.16=2.NTK_X+48\\ \Rightarrow2NTK_X+48=102\\ \Rightarrow NTK_X=\dfrac{102-48}{2}=27\left(đ.v.C\right)\\ \Rightarrow X:Nhôm\left(Al=27\right)\)
Đúng 2
Bình luận (2)
tính hàm lượng đạm trong các loại phân bón
a) phân đạm 1 lá (NH4)2 SO4
b) phân đạm 2 lá NH4 NO3
c) phân đạm wrea (NH4)2 CO
a) \(\%N\left(\left(NH_4\right)_2SO_4\right)=\dfrac{28}{132}.100\%=21,21\%\)
b) \(\%N\left(NH_4NH_3\right)=\dfrac{28}{80}.100\%=35\%\)
c) \(\%N\left(\left(NH_4\right)_2CO\right)=\dfrac{28}{60}.100\%\approx46,67\%\)
Đúng 0
Bình luận (0)
Bạn kiểm tra lại đề. Urea có công thức là CO(NH2)2 chứ không có gốc ammonium nhé.
Đúng 0
Bình luận (0)
Hãy phân loại và gọi tên các chất sau: CuO, H2CO3, SO2, Cu(OH)2, NaOH, NaHCO3, HCl, Fe(NO3)2
Oxit axit: SO2 : lưu huỳnhđioxit
Oxit bazơ: CuO: Đồng(II)oxit
Axit:
H2SO3: axit sunfurơ
HCl: axit clohiđric
Bazơ:
Cu(OH)2: Cu(II)hriđroxit
NaOH: Natri hiđroxit
Muối:
NaHCO3 : Natri hiđrocacbonat
Fe(NO3)2: Sắt (II)nitrat
Đúng 0
Bình luận (0)
PO3 đọc là gì Thuộc nhóm oxit gì
PO3 đọc là Photphat
Thuộc nhóm Oxit axit
Đúng 0
Bình luận (1)
Cho 9,75gam kim loại Zn tác dụng với dung dịch axit HCl dư, thủ được dùng dịch muối ZnCl² và khí H². Tính a. Thể tích khí H² thu được (đktc) b. Khối lượng dung dịch muối ZnCl² tạo thành
a, \(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, \(m_{ZnCl_2}=0,15.136=20,4\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 11,2 gam kim loại sắt trong không khí. a,tính thể tích không khí cần dùng ( biết khí O² chiếm 20% thể tích không khí )
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}=\dfrac{2}{15}\left(mol\right)\Rightarrow V_{O_2}=\dfrac{2}{15}.22,4=\dfrac{224}{75}\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=\dfrac{224}{15}\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(PTHH:4Fe+3O_2\xrightarrow[t^0]{}2Fe_2O_3\)
tỉ lệ :4 3 2
số mol :0,2 0,15 0,1
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
\(V_{kk}=2,24.20\%=0,448\left(l\right)\)
Đúng 1
Bình luận (0)
























