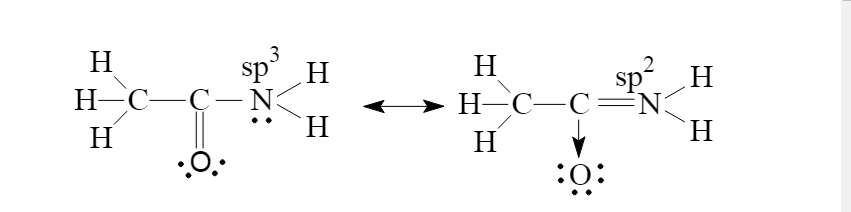
Trong phân tử axetamit, 3 liên kết với nguyên tử nitơ đều nằm trong cùng một mặt phẳng. Vì sao?
Chương 3. Liên kết hóa học
Trong phân tử axetamit, 3 liên kết với nguyên tử nitơ đều nằm trong cùng một mặt phẳng vì liên kết giữa N với C mang 1 phần đặc điểm của liên kết đôi
Đúng 0
Bình luận (0)
Công thức hợp chất khí với hiđro của nguyên tố nhóm VA có dạng là
Vận dụng thuyết lai và sự xen phủ AO, mô tả sự hình thành liên kết trong các phân tử N2, CO2 (thẳng), C2H4 (góc HCH=1200) , BF3 (FBF=1200), NH3 (HNH=1070)
Hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp, có tổng số proton là 32.
a, Hãy xác định công thức phân tử, công thức cấu tạo và cho biết kiểu liên kết trong A.
b,Trình bày tính chất hóa học của A và viết PTPƯ minh họa.
a) Vì 2 nguyên tố có tổng số proton là 32
=> 2 nguyên tố thuộc chu kì nhỏ
Gọi 2 nguyên tố cần tìm trong A là X, Y
Vì hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp => CT của A : XY2
Ta có : \(\left\{{}\begin{matrix}Z_X+2Z_Y=32\\\left|Z_X-Z_Y\right|=8\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_X=16\left(S\right)\\Z_Y=8\left(O\right)\end{matrix}\right.\)
=> CTPT của hợp chất : SO2
CT cấu tạo :
SO2 là liên kết cộng hóa trị có cực
b) Lưu huỳnh đioxit (SO2) mang đầy đủ tính chất hóa học của một oxit axit.
Tính chất hóa học của SO2:
- Tác dụng với nước tạo thành dung dịch axit.
Ví dụ: SO2 + H2O → H2SO3
- Tác dụng với dung dịch bazơ tạo thành muối và nước.
Ví dụ: SO2 + 2NaOH → Na2SO3 + H2O
- Tác dụng với oxit bazơ tạo thành muối.
Ví dụ: SO2 + Na2O → Na2SO3
Đúng 2
Bình luận (0)
Viết công thức electron, công thức cấu tạo của SO42-
Phân tử nào có liên kết phân cực mạnh nhất, vì sao ? CH4, NH3, H2O, HCl
H
CH4 H-C-H liên kết cộng hóa trị không phân cực
H
NH3 H-N-H hiệu độ âm điện=3.04-2.2=0.84
H
H2O H-O-H hiệu độ âm điện 3.44-2.2=1.24
HCl H-CL là có hiệu độ âm điện=3.16-2.2=0.96
-->H2O là liên kết phân cực mạnh nhất
Đúng 3
Bình luận (0)
Viết công thức cấu tạo của NaNO3 , K2SO4
C1: Cho 3,6g Mg va 2,7g Al tác dụng vừa đủ với V l (dktc) Cl2 và O2. Biết dx/h2=22,5. Tìm v
m Mg = 3,6/24 = 0,15(mol)
n Al = 2,7/27 = 0,1(mol)
n Cl2 = a(mol) ; n O2 = b(mol)
M X = 22,5.2 = 45(g/mol)
=> 71a + 32b = (a + b)45
<=> 26a - 13b = 0(1)
Bảo toàn electron :
2n Mg + 3n Al = 2n Cl2 + 4n O2
<=> 2a + 4b = 0,15.2 + 0,1.3 = 0,6(2)
Từ (1)(2) suy ra a = 0,06 ; b = 0,12
=> V = (0,06 + 0,12).22,4 = 4,032 lít
Đúng 2
Bình luận (0)
đun nóng 12,64g KMno4 sau 1 thời gian thu được 12,32g hỗn hợp rắn x. Hiệu suất của phản ứng nhiệt phân KMno4 là?
\(m_{O_2} = 12,64 -12,32 = 0,32(mol)\Rightarrow n_{O_2} = \dfrac{0,32}{32} = 0,01(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4\ pư} = 2n_{O_2} = 0,02(mol)\\ \Rightarrow H = \dfrac{0,02.158}{12,64}.100\% = 25\%\)
Đúng 1
Bình luận (0)
1. Xác định nhiệt của phản ứng: CH4(k) + Cl2(k) --> CH3Cl(k) + HCl(k)
Cho biết nhiệt của các phản ứng sau đây:
H2(k) + 1/2O2(k) --> H2O(l) ΔH1 = -68,32 kcal
CH4 + 2O2(k) --> CO2(k) + H2O(l) ΔH2 = -212,79 kcal
1/2 H2(k) + 1/2Cl2(k) --> HCl(k) ΔH3 = -22,06 kcal
CH3Cl(k) + 3/2O2(k) --> CO2(k) + 2H2O(k) ΔH4 = -164,0 kcal


















