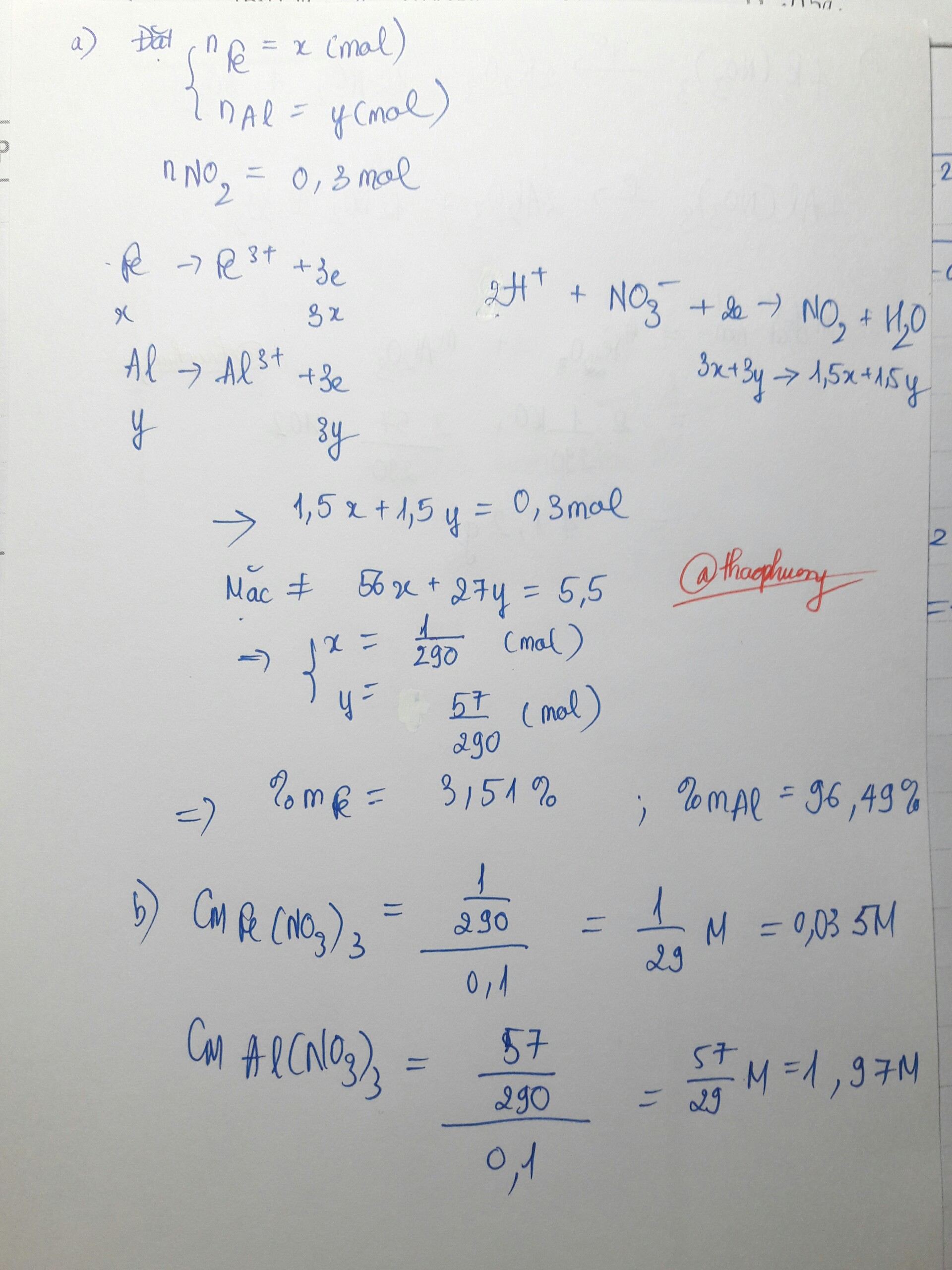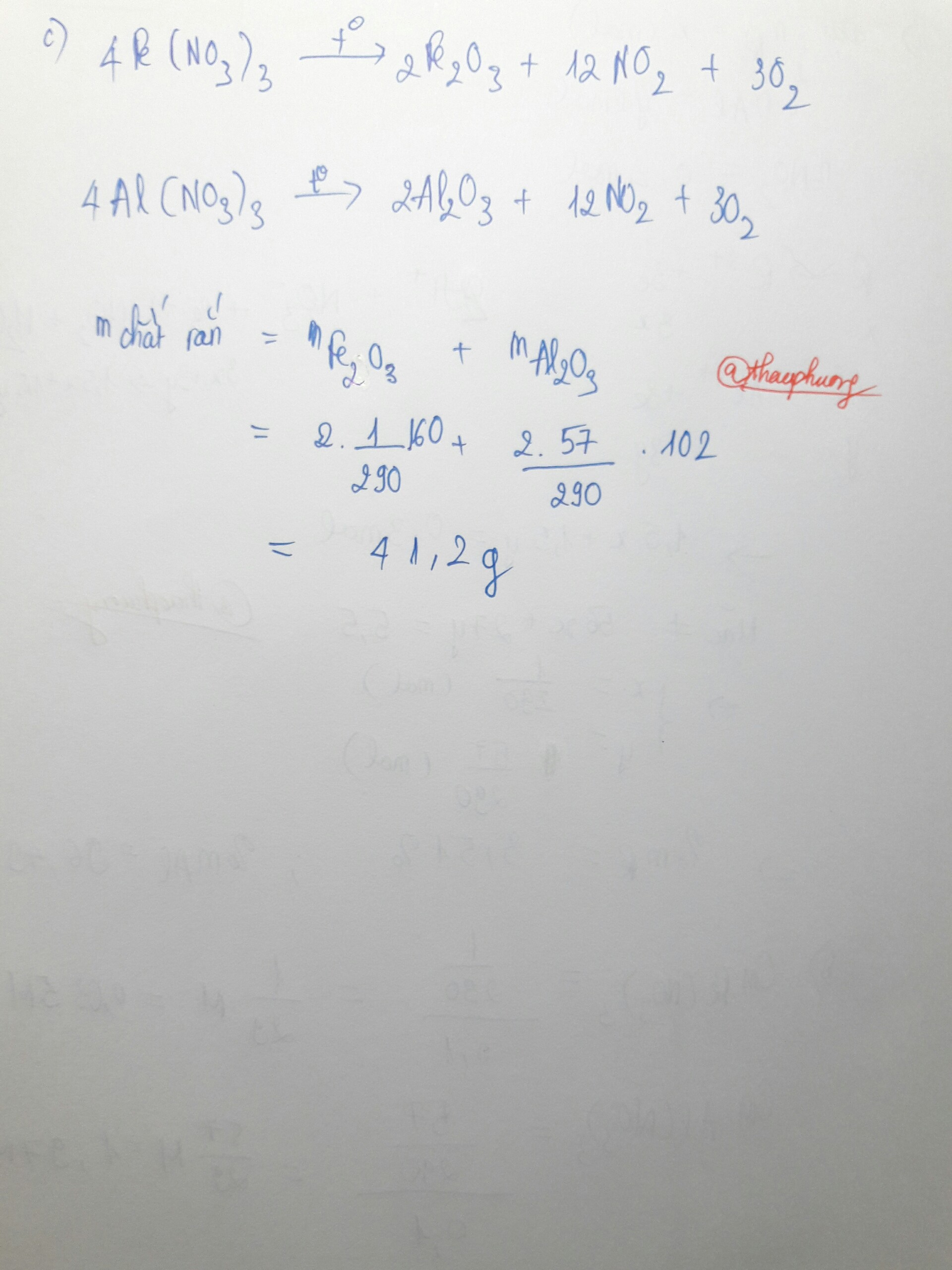Trộn 100ml dung dịch axit HCl 0,01M với 200ml dung dịch NaOH 0,5M thu được dung dịch A sau phản ứng.Viết phương trình phân tử và ion rút gọn của phản ứng và tính pH của dung dịch sau phản ứng.
Chương 2. Nhóm nitơ
a)
$NaOH + HCl \to NaCl + H_2O$
$OH^- + H^+ \to H_2O$
b)
$n_{HCl} = 0,1.0,01 = 0,001(mol)$
$n_{NaOH} = 0,2.0,5= 0,1(mol)$
$\Rightarrow$ NaOH dư, HCl hết
$n_{NaOH\ pư} = 0,001 \Rightarrow n_{NaOH\ dư} = 0,1 - 0,001 = 0,099(mol)$
$\Rightarrow [OH^-] = \dfrac{0,099}{0,1 + 0,2} = 0,33M$
$\Rightarrow pOH = -log(0,33) = 0,48 $
$pH = 14 - pOH = 14 - 0,48 = 13,52$
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 5,5g hỗn hợp Fe và Al bằng 100ml dung dịch HNO3 đặc, nóng, dư. Sau phản ứng thu được 6,72 lit khí NO2 màu nâu đỏ (đktc).a)Tính % khối lượng mỗi kim loại trong hỗn hợp đầu.b)Tính Cm các muối trong dung dịch sau phản ứng, coi thể tích dung dịch thay đổi không đáng kể.c)Nhiệt phân hoàn toàn lượng muối thu được ở trên. Tính khối lượng chất rắn và thể tích khí (đktc) thu được sau phản ứng
Đọc tiếp
Hòa tan hoàn toàn 5,5g hỗn hợp Fe và Al bằng 100ml dung dịch HNO3 đặc, nóng, dư. Sau phản ứng thu được 6,72 lit khí NO2 màu nâu đỏ (đktc).
a)Tính % khối lượng mỗi kim loại trong hỗn hợp đầu.
b)Tính Cm các muối trong dung dịch sau phản ứng, coi thể tích dung dịch thay đổi không đáng kể.
c)Nhiệt phân hoàn toàn lượng muối thu được ở trên. Tính khối lượng chất rắn và thể tích khí (đktc) thu được sau phản ứng
Trộn 200ml dung dịch axit H2SO4 0,05M với 100ml dung dịch KOH 0,2M. Viết phương trình phân tử và ion rút gọn của phản ứng và tính pH của dung dịch sau phản ứng .
\(2KOH+H_2SO_4->K_2SO_4+2H_2O\)
\(OH^-+H^+->H_2O\)
\(n_{H_2SO_4}=0,05.0,2=0,01\left(mol\right);n_{KOH}=0,2.0,1=0,02\left(mol\right)\)
PTHH: \(2KOH+H_2SO_4->K_2SO_4+2H_2O\)
_____0,02------->0,01
=> KOH, H2SO4 phản ứng vừa đủ, tạo ra dd K2SO4
=> pH = 7
Đúng 3
Bình luận (0)
Các bạn giúp mik vs ạ
Mik cảm ơn các bn rất nhiều❤
Em cần bài nào đăng lên 1 bài đó nha
Đúng 0
Bình luận (0)
Cho m gam Cu tan hết trong dd HNO3 đặc, nóng thu được 4,48 lít khí NO2 (ở đktc) duy nhất. Giá trị của V là ?
\(n_{NO_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ \Rightarrow n_{Cu}=\dfrac{1}{2}n_{NO_2}=0,1(mol)\\ \Rightarrow m_{Cu}=0,1.64=6,4(g)\)
Đúng 0
Bình luận (1)
Cho các phát biểu sau:1. Dung dịch NH3 có tính chất của một dung dịch bazơ, do đó nó có thể tác dụng với dung dịch axit.2. Nitơ tác dụng với một số kim loại mạnh trong điều kiện nhiệt độ cao tạo muối nitrat kim loại.3. Phản ứng tổng hợp NH3 từ N2 và H2 là phản ứng thuận nghịch.4. Nhiệt phân muối nitrat của kim loại mạnh thu được oxit kim loại + khí nitơ đioxit + khí oxi.5. Khi cho mảnh đồng kim loại vào dung dịch HNO3 đặc, dung dịch thu được có màu xanh, có khí màu nâu bay ra.Số phát biểu đúng l...
Đọc tiếp
Cho các phát biểu sau:
1. Dung dịch NH3 có tính chất của một dung dịch bazơ, do đó nó có thể tác dụng với dung dịch axit.
2. Nitơ tác dụng với một số kim loại mạnh trong điều kiện nhiệt độ cao tạo muối nitrat kim loại.
3. Phản ứng tổng hợp NH3 từ N2 và H2 là phản ứng thuận nghịch.
4. Nhiệt phân muối nitrat của kim loại mạnh thu được oxit kim loại + khí nitơ đioxit + khí oxi.
5. Khi cho mảnh đồng kim loại vào dung dịch HNO3 đặc, dung dịch thu được có màu xanh, có khí màu nâu bay ra.
Số phát biểu đúng là A. 2. B. 3 C. 4. D. 5.
1 đúng: \(NH_3+HCl->NH_4Cl\)
2 sai
3: đúng: \(3H_2+N_2⇌2NH_3\)
4: sai
5: đúng: \(Cu+4HNO_3->Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
=> B
Đúng 1
Bình luận (0)
Cho phản ứng hóa học: KOH + HCl→ KCl + H2O. Phản ứng nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A.NaOH +HNO3→ NaNO3 + H2O.
B.2KOH + MgCl2→ Mg(OH)2+ 2KCl.
C.Ba(OH)2 + H2SO4→ BaSO4 + 2H2O.
D.Na2S + 2HCl→ 2NaCl + H2S
Cho phản ứng hóa học: KOH + HCl→ KCl + H2O. Phản ứng nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A.NaOH +HNO3→ NaNO3 + H2O.
B.2KOH + MgCl2→ Mg(OH)2+ 2KCl.
C.Ba(OH)2 + H2SO4→ BaSO4 + 2H2O.
D.Na2S + 2HCl→ 2NaCl + H2S
Trộn lẫn 30 ml dung dịch NaOH 2M và 20 ml dung dịch H2SO41,5 M. Vậy dung dịch thu được có tính:A.Axit B.Bazơ C.Trung hoà D.Lưỡng tính
Đọc tiếp
Trộn lẫn 30 ml dung dịch NaOH 2M và 20 ml dung dịch H2SO41,5 M. Vậy dung dịch thu được có tính:
A.Axit
B.Bazơ
C.Trung hoà
D.Lưỡng tính
Phản ứ ng hoá học nào sau đây khôngđúng:
A.2KNO30 →2KNO2+ O2
B.Cu(NO3)20→CuO + 2NO2 + 1/2O2
C.4AgNO30→2Ag2O + 4NO2+ O2
D.4Fe(NO3)30t→2Fe2O3+ 12NO2+ 3O2