. Tổng số hạt trong phân tử X3Y là 264 hạt, trong đó tổng số hạt không mang điện là 96. Tỉ lệ về số hạt mang điện trong hạt nhân giữ nguyên tử X và nguyên tử Y là 13:3. Xác định công thức của X3Y
Chủ đề 2: Đồng vị-Xác định nguyên tử khối trung bình
Ta có: \(\left\{{}\begin{matrix}p_{X_3Y}+e_{X_3Y}+n_{X_3Y}=264\\n_{X_3Y}=96\\p_{X_3Y}=e_{X_3Y}\end{matrix}\right.\)
=> \(p_{X_3Y}=e_{X_3Y}=\dfrac{264-96}{2}=84\)
=> \(\left\{{}\begin{matrix}3p_X+p_Y=84\\\dfrac{p_X}{p_Y}=\dfrac{13}{3}\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}p_X=26\\p_Y=6\end{matrix}\right.\)
=> X là Fe, Y là C
X3Y: Fe3C
Đúng 1
Bình luận (0)
cho biết khối lượng nguyên tử trung bình của chlorate là 35,5. biết có 2 đồng vị là 35Cl và 37Cl. tính phần trăm số nguyên tử mỗi loại đồng vị
Gọi phần trăm số nguyên tử đồng vị của 35Cl là x(%)
=>phần trăm số nguyên tử đồng vị của 37Cl là 100-x(%)
Theo đề, ta có:
\(\dfrac{35x+37\left(100-x\right)}{100}=35.5\)
=>x=75%
=>Phần trăm số nguyên tử của 37Cl là 25%
Đúng 2
Bình luận (0)
Cho 2 loại đồng vị 79br và 81br biết M=79.91
a.tính phần trăm của mỗi đồng vị
b.tính số ngtử của 79br có trong 100ml dd br2 1M
Trong tự nhiên Liti có 2 đồng vị bền: 94% 7Li và ALi. Nguyên tử khối trung bình của Liti là 6,94. Giá trị của A là
A. 6. B. 8. C. 5. D. 9.
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Đúng 3
Bình luận (1)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
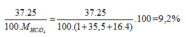
Đúng 1
Bình luận (2)
Trong tự nhiên, nguyên tố R có 2 đồng vị bền. Tổng số các hạt p, n và e trong đồng vị thứ nhất là 60, ít hơn tổng số hạt p, n và e trong đồng vị thứ hai là 2 hạt. Biết rằng các loại hạt trong đồng vị thứ nhất bằng nhau và nguyên tử khối trung bình của nguyên tố R là 40,08. Tính % khối lượng của đồng vị thứ nhất trong hợp chất RSO4?
2. Gọi nguyên tử khối của đồng vị còn lại là X
Ta có: \(\overline{M}=\dfrac{11.80+X.20}{100}=10,8\)
=> X=10
=> Chọn C
Câu 3. \(\overline{M}=\dfrac{35.75,77+37.24,23}{100}=35,4846\)
Đúng 1
Bình luận (0)
A. 10,5g.
B. 33,3g.
C. 11,1g.
D. 31,5g.
\(\%^{35}Cl=a\left(a>0\right),\%^{37}Cl=100\%-a\\ \overline{NTK}_{Cl}=35,5\\ \Leftrightarrow35a+37.\left(100\%-a\right)=35,5\\ \Leftrightarrow a=75\%\\ \Rightarrow\%^{35}Cl=75\%\\ m_{^{35}Cl}=\dfrac{106,5}{162,5}.75\%.65=31,95\left(g\right)\)
Đúng 0
Bình luận (0)
Các bác giúp em với 😢
Trong tự nhiên bạc có hai đồng vị bền là 107Ag và 109Ag. Nguyên tử khối trung b8nhf của Ag là 107,87. Tính phần trăm khối lượng của 107Ag có trông AgNO3


























