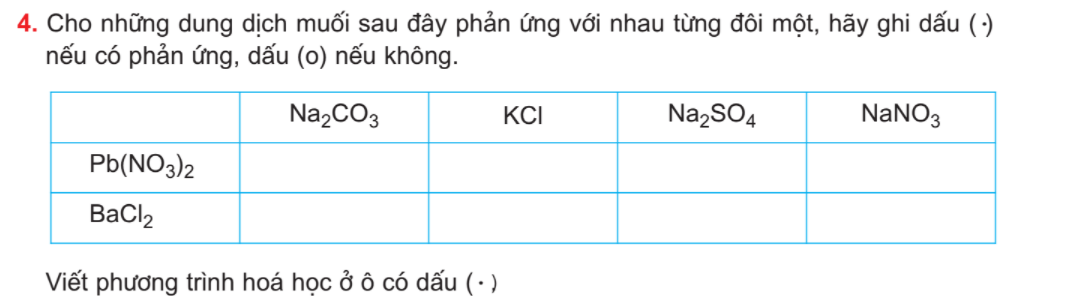
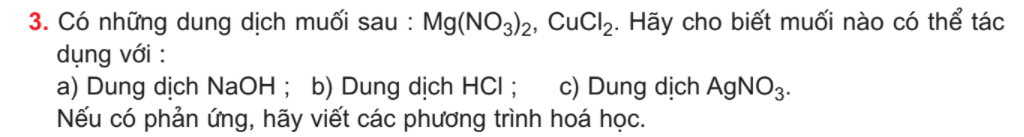
Bài 9. Tính chất hóa học của muối
Lấy một mẫu nhôm tác dụng vừa đủ với 600 ml dung dịch HCl 0,5M ta thu được một dung dịch A không màu và khí B thoát ra.
a. Tính thể tích khí B sinh ra và khối lượng mẫu nhôm cần dùng?
600ml = 0,6l
\(n_{HCl}=0,5.0,6=0,3\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
0,1 0,3 0,15
a) \(n_{H2}=\dfrac{0,3.3}{6}=0,15\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.22,4=3,36\left(l\right)\)
b) \(n_{Al}=\dfrac{0,3.2}{6}=0,1\left(mol\right)\)
⇒ \(m_{Al}=0,1.27=2,7\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
khi cho 200 g dung dịch HC1 tác dụng với CaCO, ( dư) thi thu được 4,48 lit khí ( ở đktc). a. Viết phương trình phản ứng xảy ra. b. Tinh khối lượng muối thu được sau phản ứng. b. Tính nồng độ phần trăm của dung dịch HCI.
a) \(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Đúng 0
Bình luận (0)
1)Hòa tan hoàn toàn 9,6 gam sắt (III) oxit bằng dung dịch axit sunfuric 9,8% ta thu dung dịch A màu nâu đỏ.a. Tính khối lượng dung dịch axit cần dùng? b. Tính nồng độ phần trăm của dung dịch A thu được? C. Lấy toàn bộ dung dịch A tác dụng vừa đủ bằng dung dịch BaCl2 10,4%ta thu được một chất rắn màu trắngD. Tính khối lượng chất rắn D vàkhối lượng dung dịch BaCl2 cần dùng?
Đọc tiếp
1)Hòa tan hoàn toàn 9,6 gam sắt (III) oxit bằng dung dịch axit sunfuric 9,8% ta thu dung dịch A màu nâu đỏ.
a. Tính khối lượng dung dịch axit cần dùng?
b. Tính nồng độ phần trăm của dung dịch A thu được?
C. Lấy toàn bộ dung dịch A tác dụng vừa đủ bằng dung dịch BaCl2 10,4%
ta thu được một chất rắn màu trắng
D. Tính khối lượng chất rắn D vàkhối lượng dung dịch BaCl2 cần dùng?
Ta có: \(n_{Fe_2O_3}=\dfrac{9,6}{160}=0,06\left(mol\right)\)
a. PTHH: Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 + 3H2O (1)
Theo PT(1): \(n_{H_2SO_4}=3.n_{Fe_2O_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{H_2SO_4}=0,18.98=17,64\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{17,64}{m_{dd_{H_2SO_4}}}.100\%=9,8\%\)
=> \(m_{dd_{H_2SO_4}}=180\left(g\right)\)
b. Ta có: \(m_{dd_{Fe_2\left(SO_4\right)_3}}=9,6+180=189,6\left(g\right)\)
Theo PT(1): \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,06\left(mol\right)\)
=> \(m_{Fe_2\left(SO_4\right)_3}=0,06.400=24\left(g\right)\)
=> \(C_{\%_{Fe_2\left(SO_4\right)_3}}=\dfrac{24}{189,6}.100\%=12,66\%\)
c. PTHH: Fe2(SO4)3 + 3BaCl2 ---> 3BaSO4↓ + 2FeCl3 (2)
Theo PT(2): \(n_{BaSO_4}=3.n_{Fe_2\left(SO_4\right)_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{BaSO_4}=0,18.233=41,94\left(g\right)\)
Theo PT(2): \(n_{BaCl_2}=n_{BaSO_4}=0,18\left(mol\right)\)
=> \(m_{BaCl_2}=0,18.208=37,44\left(g\right)\)
Ta có: \(C_{\%_{BaCl_2}}=\dfrac{37,44}{m_{dd_{BaCl_2}}}.100\%=10,4\%\)
=> \(m_{dd_{BaCl_2}}=360\left(g\right)\)
Đúng 0
Bình luận (0)
cho các base sau: Fe(OH)3,NaOH,Cu(OH)2,Mg(OH)2,Ba(OH)2,Al(OH)3
Những base nào bị nhiệt phân hủy? viết PTHH minh họa
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$
$Mg(OH)_2 \xrightarrow{t^o} MgO + H_2O$
$2Al(OH)_3 \xrightarrow{t^o} Al_2O_3 + 3H_2O$
Đúng 0
Bình luận (0)
Mình chưa hiểu phương trình này các cậu giải thích cho mình với
NA2CO3 + 2HCL----------> 2NaCl + Co2 + H2O
Ban đầu xảy ra phản ứng giữa muối và axit sinh ra axit mới yếu hơn axit ban đầu :
$Na_2CO_3 + 2HCl \to 2NaCl + H_2CO_3$
$H_2CO_3$ là axit yếu, dễ bị phân hủy ngay ở nhiệt độ phòng :
$H_2CO_3 \to CO_2 + H_2O$
Viết gộp :
$Na_2CO_3 + 2HCl \to 2NaCl + CO_2 + H_2O$
Đúng 1
Bình luận (1)
Hòa tan a gam hỗn hợp A (CaCO3 và K2CO3) vào nước được 80 gam dung dịch B có nồng độ 3,45% và chất rắn D, lọc D đem nung hoàn toàn thu được 2,8 g chất rắn X. a)Tính a? b)cho toàn bộ dung dịch B phản ứng vừa đủ với m gam dung dịch BaCl2 10,4% thu được dung dịch Y có nồng độ Y% Tính m và Y
-Đặc điểm cấu tạo của muối: Kim loại - gốc acid (-Cl; Br; S; SO4 SO3; CO3; -NO3; PO4)Vd: I. Tinh tan trong nước của 1 số muối:- Muối của Na, K, NO3: tất cả đều tanVd:- Muối của gốc Cl2 SO4: đa số tan (Trừ AgCl ko tan PbCl2, ít tan BaSO4 ko tan PbSO4 ko tan: Ag2SO4 ít tan, CaSO4 ít tan)Vd:- Muối của CO2, SO3, gốc PO4: KHÔNG TAN (Trừ muối của Na, K)Vd:II. Phản ứng trao đổi:- Khái niệm phản ứng trao đổi:- Điều kiện để phản ứng trao đổi xảy ra:III. Tính chất hóa học của muối * Sơ lược về dãy hoạt...
Đọc tiếp
-Đặc điểm cấu tạo của muối: Kim loại - gốc acid (-Cl; Br; =S; =SO4 =SO3; CO3; -NO3; PO4)
Vd:
I. Tinh tan trong nước của 1 số muối:
- Muối của Na, K, NO3: tất cả đều tan
Vd:
- Muối của gốc Cl2 = SO4: đa số tan (Trừ AgCl ko tan PbCl2, ít tan BaSO4 ko tan PbSO4 ko tan: Ag2SO4 ít tan, CaSO4 ít tan)
Vd:
- Muối của CO2, SO3, gốc PO4: KHÔNG TAN (Trừ muối của Na, K)
Vd:
II. Phản ứng trao đổi:
- Khái niệm phản ứng trao đổi:
- Điều kiện để phản ứng trao đổi xảy ra:
III. Tính chất hóa học của muối * Sơ lược về dãy hoạt động động hóa học của kim loại:
K Na Mg Al Zn Fe Pb H Cu Ag Pt Au
- Kim loại đứng trước mạnh hơn kim loại đứng sau.
1/ Muối + 1 số kim loại
Điều kiện pứ
Vd:
2/ Muối + Base
Điều kiện pứ:
Vd:
3/ Muối +Muối
Điều kiện pứ
Vd:
4/ Muối + Acid
Điều kiện cử:
Vd:
5/ 1 số muối bị nhiệt phân hủy
Vd: