So sánh khối lượng chất rắn sinh ra khi nung 9 gam Fe(OH)2 trong không khí và trong điều
kiện không có không khí.
Bài 26: Oxit
\(n_{Fe\left(OH\right)_2}=\dfrac{9}{90}=0,1\left(mol\right)\)
- Nếu nung trong không khí
PTHH: 4Fe(OH)2 + O2 --to--> 2Fe2O3 + 4H2O
0,1------------------>0,05
=> \(m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
- Nếu nung không có không khí
PTHH: Fe(OH)2 --to--> FeO + H2O
0,1----------->0,1
=> mFeO = 0,1.72 = 7,2 (g)
=> Khối lượng chất rắn sinh ra khi nung trong không khí nhiều hơn khối lượng rắn sinh ra khi nung trong điều kiện không có không khí
Đúng 1
Bình luận (0)
help me !!!Bài 1: Phân loại và đọc tên các chất sau: BaO, SO2, Fe2O3, ZnO, P2O5, Na2O, SO3, N2O5, CaO,FeO?Bài 2: Hoàn thành các PTHH sau:a, ... + O2 → ZnOb, ... + O2 → SO2c, H2 + PbO → ... + ...d, C3H8 + O2 → ... + ...e, ... + .... → MgSO4 + H2Bài 3: Đốt cháy 4,8 gam Mg. Tính :a/ Thể tích không khí cần dùng (đktc)?b/ Khối lượng sản phẩm thu được?Bài 4: Cho 13 gam Zn vào 14,6 gam HCl. Tính:a/ Thể tích khí thu được ở đktc?b/ Khối lượng chất còn dư sau phản ứng?Bài 5: Đốt cháy 13,5 gam Al trong 6,7...
Đọc tiếp
help me !!!
Bài 1: Phân loại và đọc tên các chất sau: BaO, SO2, Fe2O3, ZnO, P2O5, Na2O, SO3, N2O5, CaO,
FeO?
Bài 2: Hoàn thành các PTHH sau:
a, ... + O2 → ZnO
b, ... + O2 → SO2
c, H2 + PbO → ... + ...
d, C3H8 + O2 → ... + ...
e, ... + .... → MgSO4 + H2
Bài 3: Đốt cháy 4,8 gam Mg. Tính :
a/ Thể tích không khí cần dùng (đktc)?
b/ Khối lượng sản phẩm thu được?
Bài 4: Cho 13 gam Zn vào 14,6 gam HCl. Tính:
a/ Thể tích khí thu được ở đktc?
b/ Khối lượng chất còn dư sau phản ứng?
Bài 5: Đốt cháy 13,5 gam Al trong 6,72 lít khí O2 (đktc). Tính % khối lượng chất rắn thu
được sau phản ứng?
Bài 6: Hòa tan hoàn toàn 4g một kim loại hóa trị II bằng dung dịch HCl thu được 2,24 lít khí
H2 (đktc). Xác định tên kim loại đã dùng?
2.
\(2Zn+O_2\rightarrow\left(t^o\right)2ZnO\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(H_2+PbO\rightarrow Pb+H_2O\)
\(C_3H_8+5O_2\rightarrow\left(t^o\right)3CO_2+4H_2O\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
Đúng 2
Bình luận (0)
Bài 1: Phân loại và đọc tên các chất sau: BaO, SO2, Fe2O3, ZnO, P2O5, Na2O, SO3, N2O5, CaO,
FeO?
BaO ; Fe2O3 ZnO Na2O CaO FeO => oxit bazo
còn lại là oxit axit
Bài 2: Hoàn thành các PTHH sau:
a, ...2Zn + O2 → 2ZnO
b, ..S. + O2 → SO2
c, H2 + PbO → ..Pb. + ...H2O
d, C3H8 + 2O2 → 3C... + ...4H2O
e, ..H2SO4. + ..Mg.. → MgSO4 + H2
Đúng 1
Bình luận (0)
4.
\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{13}{65}=0,2mol\)
\(n_{HCl}=\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 = 0,4 ( mol )
0,2 0,2 ( mol )
=> KL chất dư bằng 0
\(V_{H_2}=n_{H_2}.22,4=0,2.22,4=4,48l\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
\(n_S=\dfrac{1,28}{32}=0,04mol\)
\(n_O=\dfrac{0,672}{22,4}=0,03mol\)
\(S+O_2\underrightarrow{t^o}SO_2\)
bđ 0,04 0,03 0
pư 0,03 0,03 0,03
kt 0,01 0 0,03
Chất còn dư là \(S\) và dư 0,01 mol.
\(m_{Sdư}=0,01\cdot32=0,32g\)
\(m_{SO_2}=0,03\cdot64=1,92g\)
Đúng 2
Bình luận (0)
\(n_S=\dfrac{m_S}{M_S}=\dfrac{1,28}{32}=0,04mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{0,672}{22,4}=0,03mol\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
1 1 1 ( mol )
0,04 > 0,03 ( mol )
0,03 0,03 0,03 ( mol )
\(m_{S\left(du\right)}=n_{S\left(du\right)}.M_S=\left(0,04-0,03\right).32=0,32g\)
\(m_{SO_2}=n_{SO_2}.M_{SO_2}=0,03.64=1,92g\)
Đúng 0
Bình luận (0)
Đốt cháy 22,4g Fe trong bình chứa 4,48 l khí o2 (đktc) Tính khhois lượng chất còn dư sau phản ứng
Ta có: nFe = 22,4/56 = 0,4 (mol)
nO2 = 4,48/22,4 = 0,2 (mol)
PTHH: 3Fe + 2O2 -> Fe3O4
3 mol 2mol 1mol
SS: 0,4/3mol > 0,2/2mol -> Fe dư , O2 hết
Ta có: nFe p/ứng là: 0,2.3/2 = 0,3 mol
=> mFe phản ứng: 0,3.56 =16,8 (g)
=> mFe dư: 22,4 - 16,8 = 5,6 (g)
Đúng 1
Bình luận (0)
Oxi hoá sắt trong bình chứa 1,12 lít khí oxi(đktc) thu đc Fe3O4.Sau khi phản ứng kết thúc. a.Tính khối lượng sắt tham gia phản ứng ? b.Tính khối lượng Fe304 thu đc khi phản ứng kết thúc ?
nO2 = 1,12/22,4 = 0,05 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,075 <--- 0,05 ---> 0,025
mFe = 0,075 . 56 = 4,2 (g)
mFe3O4 = 0,025 . 232 = 5,8 (g)
Đúng 3
Bình luận (0)
3Fe+2O2-to>Fe3O4
0,075-0,05------0,025 mol
n O2=\(\dfrac{1,12}{22,4}\)=0,05 mol
=>m Fe=0,075.56=4,2g
=>m Fe3O4=0,025.232=5,8g
Đúng 1
Bình luận (0)
Cho oxit của kim loại B hoá trị 2 phản ứng vừa đủ với dd H2SO4 10%. Sau phản ứng
thu được dung dịch A, biết C% của dd A là 11,765%. Xác định kim loại B
CTHH: BO
Gọi số mol BO là a(mol)
PTHH: BO + H2SO4 --> BSO4 + H2O
a--->a----------->a
=> \(m_{H_2SO_4}=98a\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{98a.100}{10}=980a\left(g\right)\)
mdd sau pư = a(MB + 16) + 980a (g)
\(m_{BSO_4}=a\left(M_B+96\right)\left(g\right)\)
=> \(C\%=\dfrac{a\left(M_B+96\right)}{a\left(M_B+16\right)+980a}.100\%=11,765\%\)
=> MB = 24 (g/mol)
=> B là Mg
Đúng 1
Bình luận (0)
ứng dụng của oxygen trong lĩnh vực nào cho hai ví dụ mỗi loại
Tham khảo:
Các ứng dụng của khí oxygen trong đời sống và trong sản xuất:
Khí oxygen dùng để duy trì sự sống của con người
Được dùng trong y tế để làm chất duy trì hô hấp, hoặc dùng trong các bình lặn của thợ lặn, ngoài ra còn dùng để cung cấp cho phi công trong những trường hợp không khí loãng,...
Cung cấp nhiệt và cần thiết cho quá trình đốt cháy nhiên liệu trong quá trình đun nấu,...
Oxi cũng được dùng nhiều trong công nghiệp hóa chất, luyện thép, hàn cắt kim loại (đèn xì axetylen), sản xuất rượu , làm thuốc nổ,....
Đúng 1
Bình luận (0)
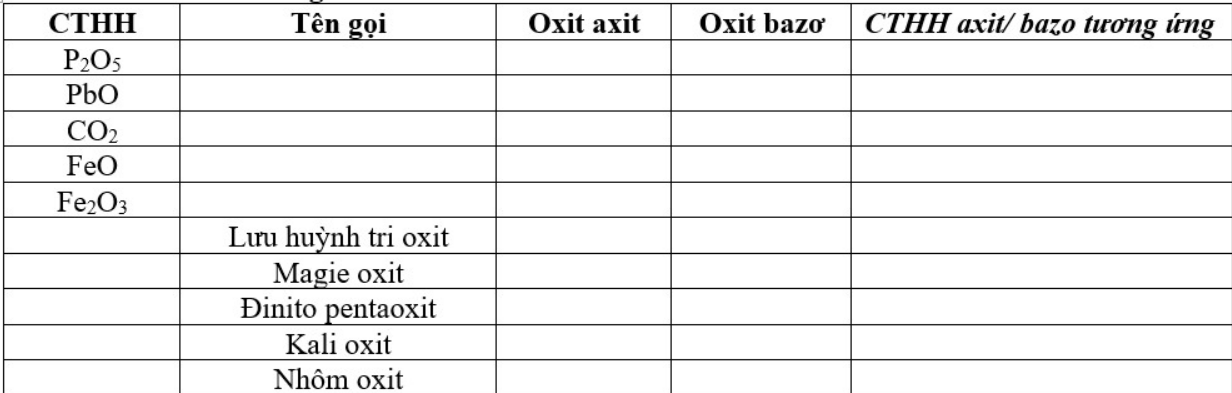
P2O5: điphotpho pentaoxit: oxit axit: H3PO4
PbO: chì (II) oxit: oxit bazơ: Pb(OH)2
CO2: cacbon đioxit: oxit axit: H2CO3
FeO: sắt (II) oxit: oxit bazơ: Fe(OH)2
Fe2O3: sắt (III) oxit: oxit bazơ: Fe(OH)3
SO3: lưu huỳnh trioxit: oxit axit: H2SO4
MgO: magie oxit: oxit bazơ: Mg(OH)2
N2O5: đinitơ pentaoxit: oxit axit: HNO3
K2O: kali oxit: oxit bazơ: KOH
Al2O3: nhôm oxit: oxit lưỡng tính: Al(OH)3
Đúng 2
Bình luận (0)
Cho các chất sau:
N2O3,KClO3, ZnCl2, FeO, ZnO, H2SO3, SO2, NaOH
a) cho biết chất nào là oxit?
b) Phân loại và gọi tên các oxit ở câu hỏi a.
N2O3: oxit axit: đinitơ trioxit
FeO: oxit bazơ: sắt (II) oxit
ZnO: oxit lưỡng tính: kẽm oxit
SO2: oxit axit: lưu huỳnh đioxit
Đúng 2
Bình luận (0)
N2O3,KClO3, ZnCl2, FeO, ZnO, H2SO3, SO2, NaOH
oxit axit:
N2O3 : đinitotrioxit
SO2: lưu huỳnh đioxit
oxit bazo
FeO : sắt 2oxit
ZnO: kẽm oxit
Đúng 0
Bình luận (0)
nêu 3 phương pháp hóa học giúp nhận ra co2 và o2
Đó là
-Quỳ tím
- đóm còn cháy
-tàn đóm còn đỏ
Đúng 1
Bình luận (0)
Dùng quỳ tím ẩm trong đó CO2 sẽ hóa đỏ và O2 không đổi màu nhé =)
Đúng 0
Bình luận (1)