Phát biểu nào sau đây sai? A.Nguyên tử trung hoà về điện B.Hạt nhân nguyên tử có kích thước rất bé nhưng lại có khối lượng rất lớn C..Nguyên tử cí cấu tạo rỗng D.Khối lượng của nguyên tử gần bằng khối lượng của hạt nhân nguyên tử
Bài 2. Hạt nhân nguyên tử. Nguyên tố hóa học. Đồng vị
Phát biểu nào sau đây sai?
A.Nguyên tử trung hoà về điện
B.Hạt nhân nguyên tử có kích thước rất bé nhưng lại có khối lượng rất lớn
C..Nguyên tử có cấu tạo rỗng
D.Khối lượng của nguyên tử gần bằng khối lượng của hạt nhân nguyên tử
Đúng 1
Bình luận (1)
Mình thấy B,C sai
Vì câu B nó không có kích thước lớn, câu C cấu tạo nguyên tử đặc khít mới đúng
Đúng 1
Bình luận (0)
Hoặc có thể C sai rõ ràng
Nhưng câu B thì khối lượng rất lớn (và rất lớn đó là so với tổng KL nguyên tử)
Nên chọn C là hợp lí nhất
Đúng 1
Bình luận (0)
Tổng số p, n, e trong ng tử X bằng 10. Số khối của X là
A. 6 B. 8 C. 9 D. 7
Ta có:
\(\dfrac{S}{3,5}\le Z\le\dfrac{S}{3}\)
\(\Leftrightarrow\) \(\dfrac{10}{3,5}\le Z\le\dfrac{10}{3}\)
\(\Leftrightarrow\) \(2,9\le Z\le3,3\)
\(\Rightarrow Z=3=P=E\)
\(\Rightarrow N=10-2Z=10-2\cdot3=4\)
Vậy \(A=Z+N=3+4=7\)
Chọn D
Chúc bn học tốt!
Đúng 1
Bình luận (0)
Đồng có 2 đồng vị bền là: 65Cu , 63Cu . Nguyên tử khối trung bình của đồng là 63,54.
Thành phần phần trăm của đồng vị 65Cu là:
A. 30%. B. 27%. C. 28%. D. 27,5%
Đồng có 2 đồng vị bền là: 65Cu , 63Cu . Nguyên tử khối trung bình của đồng là 63,54.
Thành phần phần trăm của đồng vị 65Cu là
Nguyên tố R có cấu hình electron 1s22s22p63s23p63d34s2. R thuộc họ nguyên tố nào
Nguyên tố R có cấu hình electron1s22s22p63s23p63d34s2
=> ZR=23
=> R là Vanadi (V) thuộc ô 23, chu kì 4, nhóm VB, thuộc khối các nguyên tố d
Đúng 1
Bình luận (0)
Mg là nguyên tố nhóm IIA, oxit cao nhất của nó có công thức là
Nguyên tố R có cấu hình e 1s22s2p3 công thức hợp chất khí hidro và công thức hợp chất oxit cao nhất là
R có cấu hình e: 1s22s22p3
Nên R thuộc ô 7, nhóm VA, chu kì 2
CT hợp chất khí với H: NH3
CT hợp chất oxit cao nhất: N2O5
Đúng 0
Bình luận (0)
Hợp chất RH3, trong đó Hirdro chiếm 17,65% về khối lượng. Nguyên tố R là
Ta có: \(\%_{H_{\left(RH_3\right)}}=\dfrac{1.3}{NTK_R+1.3}.100\%=17,65\%\)
\(\Rightarrow NTK_R\approx14\left(đvC\right)\)
Vậy R là nguyên tố nitơ (N)
Đúng 1
Bình luận (0)
Giải hộ mình bài này với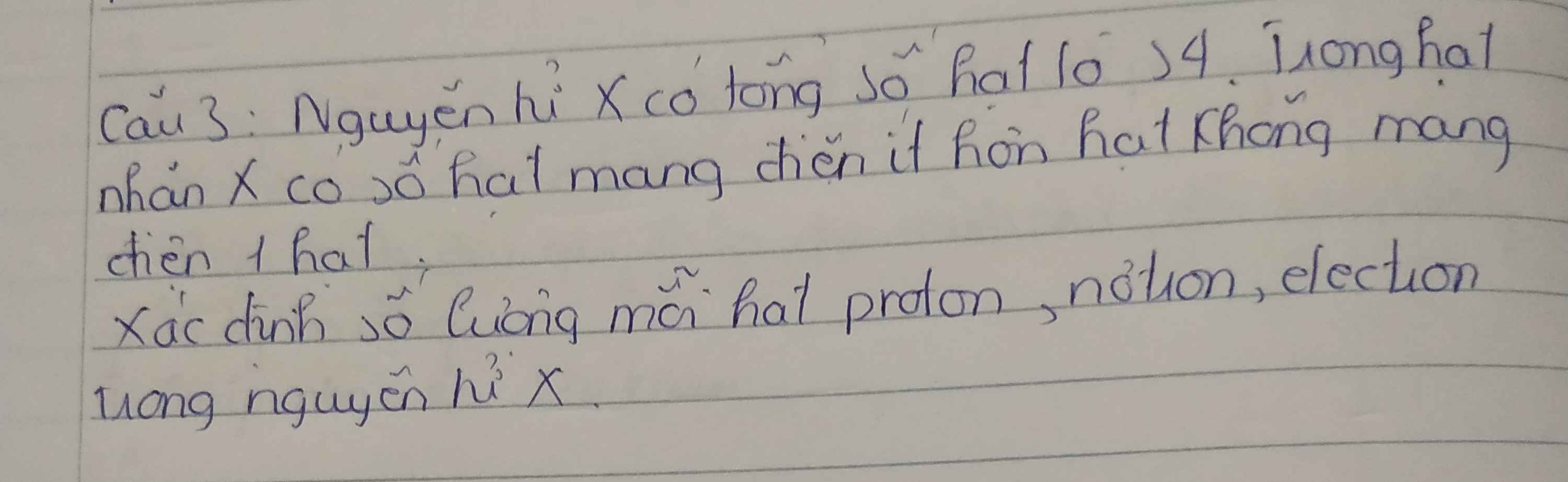
\(Tacó:\left\{{}\begin{matrix}2Z+N=34\\N-Z=1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}Z=11=P=E\\N=12\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Câu 1: Nguyên tử của nguyên tố X có tổng số hạt là 115. Số hạt mang điện nhiều hơn số hạt không mang điện là 25. Viết cấu hình electron của nguyên tử X.


















