Bài 16: Phương trình hóa học
Cái này lên gg tra cho nhanh chứ nhiều như tờ sớ này ai làm cho nổi =)))
Đúng 1
Bình luận (1)
tr pthh kiểu này dựa vào hóa trị cần bằng ra ời:v
Đúng 0
Bình luận (0)
a) \(K_2CO_3+BaCl_2\xrightarrow[]{}2KCl+BaCO_3\)
b) (mol) 1.................1...............2...............1
(mol) 0,1................0,1.............0,2............0,1
c)\(n_{BaCO_3}=\dfrac{19,7}{197}=0,1\left(mol\right)\)
\(m_{K_2CO_3}=0,1.138=13,8\left(g\right)\)
\(m_{BaCl_2}=0,1.208=20,8\left(g\right)\)
Đúng 1
Bình luận (0)
Lập PTHH cho các sơ đồ phản ứng sau và xác định tỉ lệ của các chất trong phương trình:
a, KMnO4--→K2MnO4+MnO2+O2
b,Fe+O2---→FE3O4
c,Al+H2SO4--→Al2(SO4)3+H2
d,CH4+O2--→CO2+H2O
e,SO2+O2--→SO3
g,FexOy+H2--→FeH2O
a) \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\left(2:1:1:1\right)\)
b) \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\left(3:2:1\right)\)
c) \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\left(2:3:1:2\right)\)
d) \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\left(1:2:1:2\right)\)
e) \(2SO_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\left(2:1:2\right)\)
g) \(Fe_xO_y+yH_2\xrightarrow[]{t^o}xFe+yH_2O\left(1:y:x:y\right)\)
Đúng 1
Bình luận (0)
Cách 1:
1. \(2Cu+O_2\xrightarrow[]{t^o}2CuO\)
2. \(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
3. \(2HgO\xrightarrow[]{t^o}2Hg+O_2\)
4. \(Fe_3O_4+4H_2SO_4\rightarrow FeSO_4+Fe_2\left(SO_4\right)_3+4H_2O\)
5. \(K_2O+H_2O\rightarrow2KOH\)
6. \(3KOH+AlCl_3\rightarrow Al\left(OH\right)_3\downarrow+3KCl\)
7. \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
8. \(MgSO_4+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+Na_2SO_4\)
9. \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
10. \(FeO+H_2\xrightarrow[]{t^o}Fe+H_2O\)
11. \(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
12. \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2\uparrow+H_2O\)
13. \(S+O_2\xrightarrow[]{t^o}SO_2\)
14. \(Fe+2HCl\rightarrow FeCl_2+H_2\)
15. \(Al_2O_3+2H_3PO_4\rightarrow AlPO_4\downarrow+3H_2O\)
16. \(MgSO_4+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+K_2SO_4\)
17. \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
18. \(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
19. \(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\downarrow\)
20. \(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
21. \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
22. \(2NaCl+2H_2O\xrightarrow[cmn]{đpdd}2NaOH+Cl_2+H_2\)
23. \(K_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2KCl\)
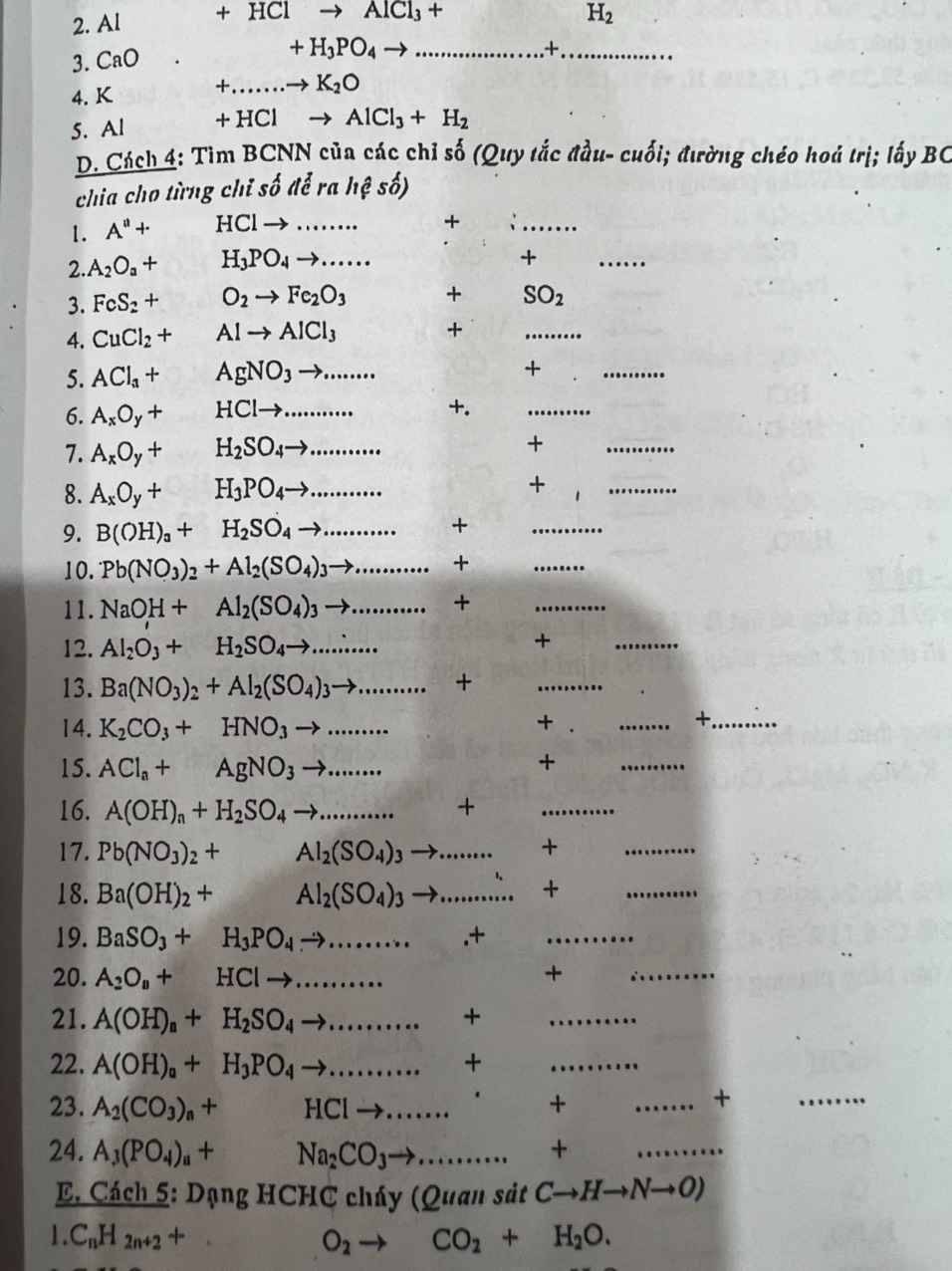
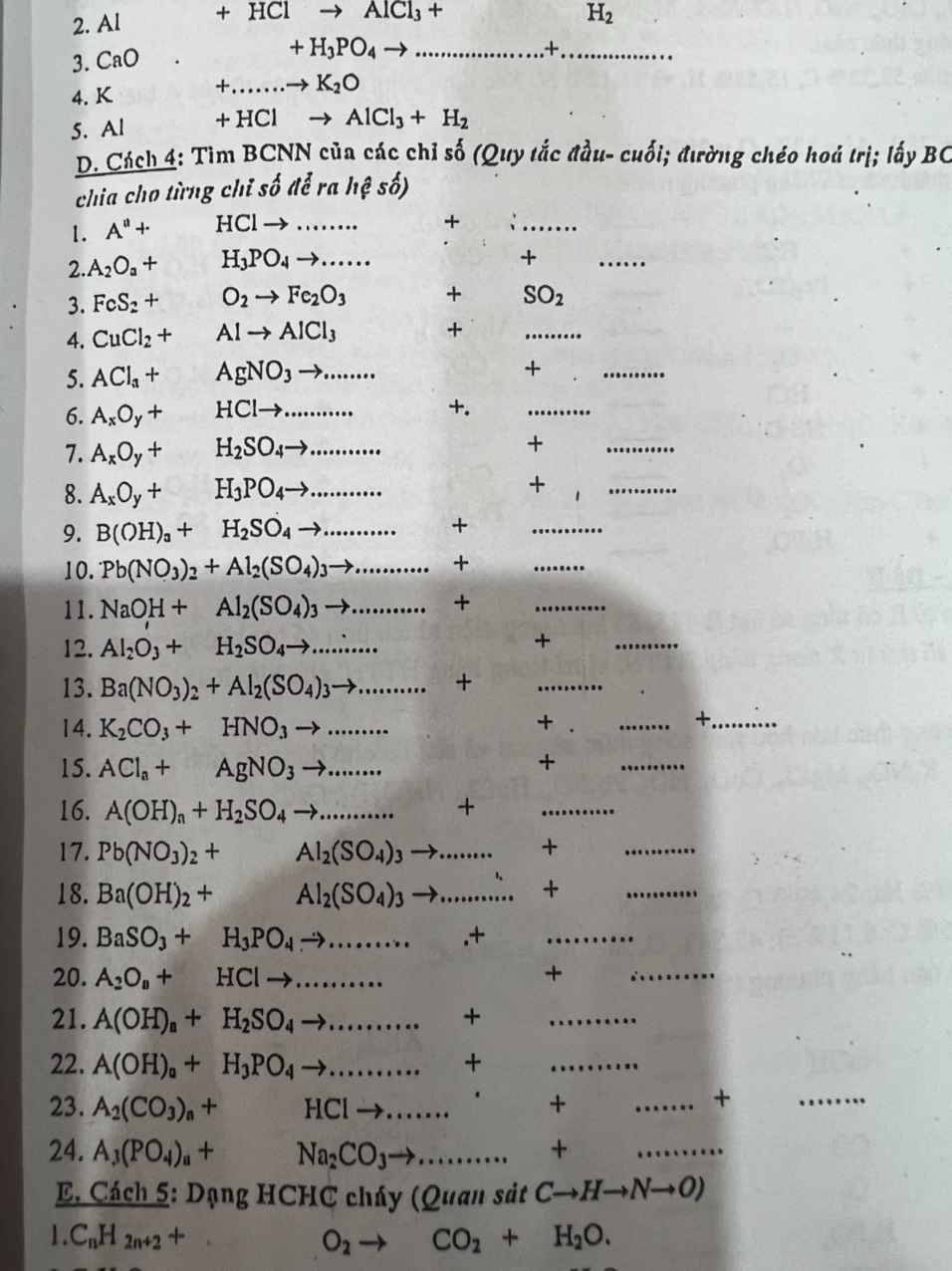
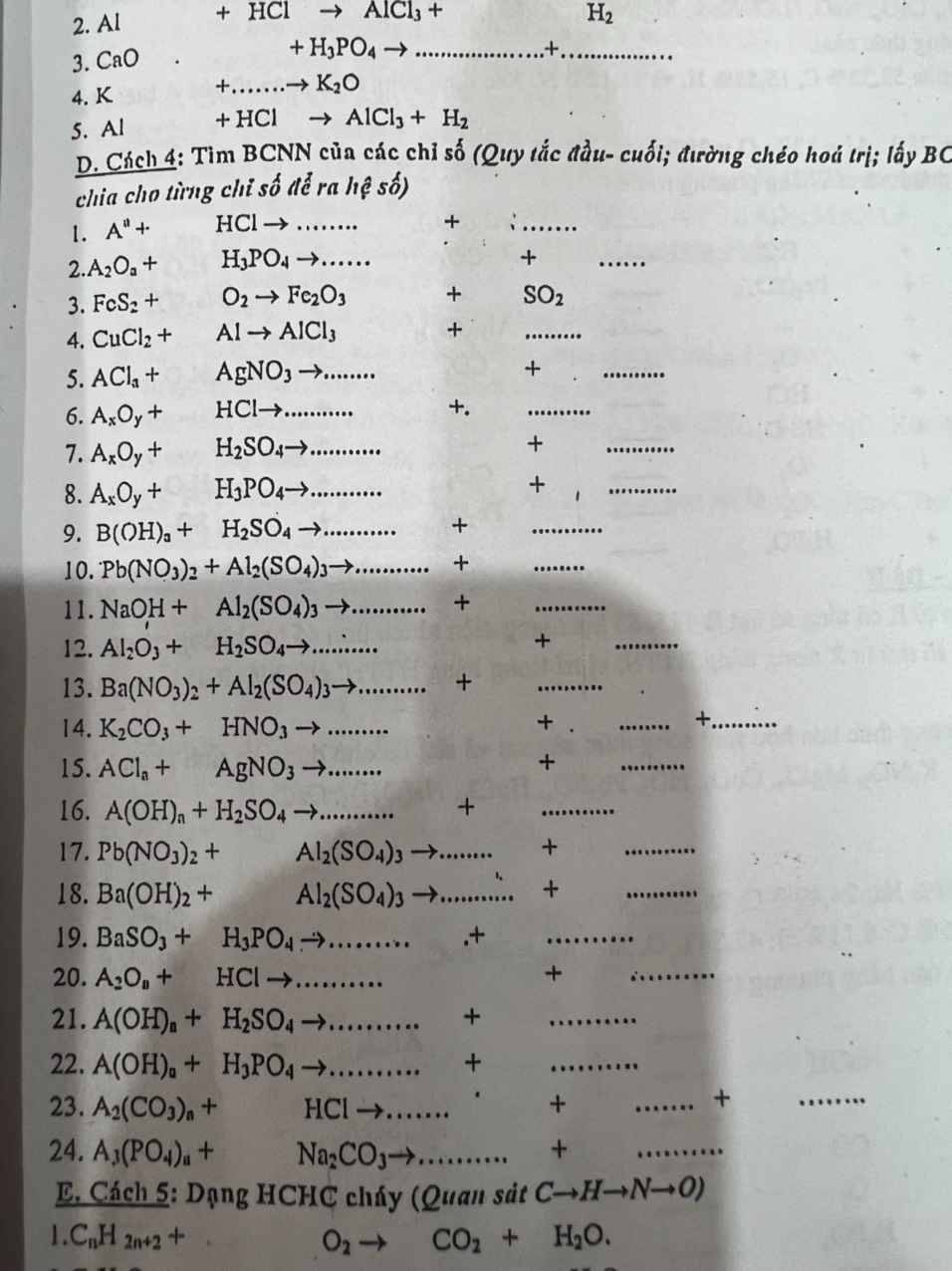
Cách 4:
1. \(2A+2aHCl\rightarrow2ACl_a+aH_2\)
2. \(3A_2O_a+2aH_3PO_4\rightarrow2A_3\left(PO_4\right)_a+3aH_2O\)
3. \(4FeS_2+11O_2\xrightarrow[]{t^o}2Fe_2O_3+8SO_2\)
4. \(3CuCl_2+2Al\rightarrow2AlCl_3+3Cu\downarrow\)
5. \(ACl_a+aAgNO_3\rightarrow aAgCl\downarrow+A\left(NO_3\right)_a\)
6. \(A_xO_y+2yHCl\rightarrow xACl_{2y/x}+yH_2O\)
7. \(A_xO_y+yH_2SO_4\rightarrow A_x\left(SO_4\right)_y+yH_2O\)
8. \(3A_xO_y+2yH_3PO_4\rightarrow A_{3x}\left(PO_4\right)_{2y}+3yH_2O\)
9. \(2B\left(OH\right)_a+aH_2SO_4\rightarrow B_2\left(SO_4\right)_a+2aH_2O\)
10. \(3Pb\left(NO_3\right)_2+Al_2\left(SO_4\right)_3\rightarrow2Al\left(NO_3\right)_3+3PbSO_4\downarrow\)
11. \(6NaOH+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3\downarrow+3Na_2SO_4\)
12. \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
13. \(3Ba\left(NO_3\right)_2+Al_2\left(SO_4\right)_3\rightarrow2Al\left(NO_3\right)_3+3BaSO_4\downarrow\)
14. \(K_2CO_3+2HNO_3\rightarrow2KNO_3+CO_2\uparrow+H_2O\)
15. \(ACl_a+aAgNO_3\rightarrow aAgCl\downarrow+A\left(NO_3\right)_a\)
16. \(2A\left(OH\right)_a+aH_2SO_4\rightarrow A_2\left(SO_4\right)_a+2aH_2O\)
17. \(3Pb\left(NO_3\right)_2+Al_2\left(SO_4\right)_3\rightarrow2Al\left(NO_3\right)_3+3PbSO_4\downarrow\)
18. \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3\downarrow+3BaSO_4\downarrow\)
19. \(3BaSO_3+2H_3PO_4\rightarrow Ba_3\left(PO_4\right)_2\downarrow+3SO_2\uparrow+3H_2O\)
20. \(A_2O_n+2nHCl\rightarrow2ACl_n+nH_2O\)
21. \(2A\left(OH\right)_a+aH_2SO_4\rightarrow A_2\left(SO_4\right)_a+2aH_2O\)
22. \(3A\left(OH\right)_a+aH_3PO_4\rightarrow A_3\left(PO_4\right)_a+3aH_2O\)
23. \(A_2\left(CO_3\right)_a+2aHCl\rightarrow2ACl_a+aCO_2\uparrow+aH_2O\)
24. \(2A_3\left(PO_4\right)_a+3aNa_2CO_3\rightarrow3A_2\left(CO_3\right)_a+2aNa_3PO_4\)
Đúng 2
Bình luận (0)
a,cho vài viên zinc vào trong ống nghiêm đựng dung dịch sulfuric acid(H2SO4) thu được dung dịch zinc sulfate và khí hydrogen.Biết rằng hóa trị của zinc là 2(la mã),nhóm sulfate(=SO4)
b'cho thanh (sắt)nóng vào lọ đựng khí chlorine thấy có khói màu nâu đó là iron(3 la mã) chloride.Biết rằng hóa trị của iron :(3 la mã);Chloride(Cl)
a) `Zn+H_2SO_4->ZnSO_4+H_2`
b) $2Fe+3Cl_2 \xrightarrow{t^o} 2FeCl_3$
Đúng 0
Bình luận (0)
FexOy ->FeO + CO2
CxHyOz + O2 -> CO2 + H2O
\(Fe_xO_y+\left(y-x\right)CO\xrightarrow[]{t^o}xFeO+\left(y-x\right)CO_2\)
\(4C_xH_yO_z+\left(4x+y-2z\right)O_2\xrightarrow[]{t^o}4xCO_2+2yH_2O\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,2 gam một hợp chất hữu cơ X cần vừa đủ 3,36 lít O2 (đktc), sau phản ứng thu được 2,24 lít CO2 (đktc) và nước. a. Hợp chất X có thể được cấu tạo từ những nguyên tố nào? Vì sao?b. Xác định công thức hóa học của X, biết khi hóa hơi 1,6 gam X thì thu được chất khí có thể tích bằng với thể tích của 1,4 gam N2 (đo ở cùng điều kiện).
Đọc tiếp
Đốt cháy hoàn toàn 3,2 gam một hợp chất hữu cơ X cần vừa đủ 3,36 lít O2 (đktc), sau phản ứng thu được 2,24 lít CO2 (đktc) và nước.
a. Hợp chất X có thể được cấu tạo từ những nguyên tố nào? Vì sao?
b. Xác định công thức hóa học của X, biết khi hóa hơi 1,6 gam X thì thu được chất khí có thể tích bằng với thể tích của 1,4 gam N2 (đo ở cùng điều kiện).
a) Hợp chất X có thể được cấu tạo từ những nguyên tố C, H, O hoặc C, H vì khí đốt cháy thu được CO2 và H2O
b) \(\left\{{}\begin{matrix}n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\end{matrix}\right.\)
ĐLBTKL:
mX + mO2 = mCO2 + mH2O
=> mH2O = 3,2 + 0,15.32 - 0,1.44 = 3,6 (g)
=> \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
1,4 gam N2 có \(n_{N_2}=\dfrac{1,4}{28}=0,05\left(mol\right)\)
=> \(M_X=\dfrac{1,6}{0,05}=32\left(g/mol\right)\)
Theo ĐLBTNT: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=0,1\left(mol\right)\\n_H=2n_{H_2O}=0,4\left(mol\right)\\n_{O\left(X\right)}=2n_{CO_2}+n_{H_2O}-2n_{O_2}=0,1\left(mol\right)\end{matrix}\right.\)
=> \(n_C:n_H:n_O=0,1:0,4:0,1=1:4:1\)
=> X có dạng (CH4O)n
=> \(n=\dfrac{32}{32}=1\)
=> X là CH4O
Đúng 2
Bình luận (0)
Hoàn thành các phương trình sau a) Mg+HCM–>MgCl2±H2 b)Fe(OH) 3–>FeO3+H2O
a) \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b) \(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H_2O\)
Đúng 1
Bình luận (1)
a, 2Fe+3Cl2 -> 2FeCl3
b, K + H2O -> KOH + \(\dfrac{1}{2}\)H2
c, Al+3HCl -> AlCl3 + \(\dfrac{3}{2}\)H2
d, CH4 + 2O2 -> CO2 + 2H2O
a, 2Cu + O2 -> 2CuO
b, MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
Đúng 1
Bình luận (0)
lập phương thức hóa học và tính phân tử khối của hợp chất tạo bởi canxi (Ca) hóa trị (2) nitrat(CO3) hóa trị (1)
nitrat là NO3 bạn nhé, còn CO3 là cacbonat hóa trị II
Gọi CTHH của hợp chất là \(Ca_x\left(NO_3\right)_y\)
Theo quy tắc hóa trị, ta có: \(x.II=y.I\)
=> \(\dfrac{x}{y}=\dfrac{1}{2}\)
=> CTHH của hợp chất là Ca(NO3)2
PTK = 40 + (14 + 16.3).2 = 164 (đvC)
Đúng 3
Bình luận (0)