
giúp em với ạ

giúp em với ạ
Câu 4: Hoà tan hoàn toàn 10 gam hỗn hợp gồm Fe2O3, MgO trong 500 ml axit H2SO4 0,4M (vừa đủ). Sau
phản ứng, hỗn hợp muối sunfat khan thu được khi cô cạn dung dịch có khối lượng là bao nhiêu? (26g)
Oxit + Axit ---------> Muối + H2O
Bảo toàn nguyên tố H: \(n_{H_2SO_4}.2=n_{H_2O}.2\Rightarrow n_{H_2SO_4}=0,5.0,4=0,2\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{oxit}+m_{H_2SO_4}=m_{muối}+m_{H_2O}\)
=> \(m_{muối}=10+0,2.98-0,2.18=26\left(g\right)\)
6. Vận dụng:
Câu 1: Oxit nào sau đây có tính bazơ?
A. CO B. CO2 C. Fe3O4 D. NO2
Câu 2: Oxit X phản ứng được với dung dịch NaOH. X không thể là
A. Al2O3 B. CO2 C. SO2 D. CuO
Câu 3: Oxit X tan trong nước tạo thành dung dịch có khả năng làm quỳ tím hóa xanh. X có thể là
A. Al2O3 B. K2O C. SO2 D. CuO
Câu 4: Nhận định nào sau đây là sai?
A. Oxit của kim loại là oxit bazơ.
B. Al2O3 tan được trong cả dung dịch HCl và dung dịch NaOH.
C. Khí SO2 là nguyên nhân gây ra hiện tượng mưa axit.
D. Khí CO2 là nguyên nhân gây hiệu ứng nhà kính.
Câu 5: Tính chất không phải của CaO là
A. hút ẩm mạnh. B. có tính bazơ.
C. trung hòa axit trong đất chua. D. tan trong nước thành dung dịch CaO.
Câu 6: SO2 không phản ứng với chất hoặc dung dịch nào sau đây?
A. CaO, t0
. B. Dung dịch H2SO4. C. dung dịch Ca(OH)2. D. H2O
Câu 7: Thí nghiệm nào sau đây thu được kết tủa không tan?
A. Dẫn khí CO2 dư vào dung dịch Ba(OH)2. B. Dẫn khí CO2 vào dung dịch Ba(OH)2 dư.
C. Nhỏ dung dịch HCl vào CuO. D. Dẫn khí CO2 vào dung dịch NaOH dư.
Câu 8: Phản ứng nào sau đây sai?
A. Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O B. Fe3O4 + 8HCl→ FeCl2 + 2FeCl3 + 4H2O
C. CO2 + CaCO3 + H2O → Ca(HCO3)2 D. CuO + H2O → Cu(OH)2
Câu 9: Trong công nghiệp, CaO được sản xuất từ
A. Ca. B. CaCO3. C. Ca(OH)2. D. CaC2O4.
Câu 10: Phản ứng dùng để điều chế SO2 trong phòng thí nghiệm là
A. S + O2
o
t
SO2 B. CaSO3 + H2SO4 → CaSO4 + SO2 + H2O
B. Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O D. 4FeS2 +11O2
o
t
2Fe2O3 + 8SO2
Câu 1: Oxit nào sau đây có tính bazơ?
A. CO B. CO2 C. Fe3O4 D. NO2
Câu 2: Oxit X phản ứng được với dung dịch NaOH. X không thể là
A. Al2O3 B. CO2 C. SO2 D. CuO
Câu 3: Oxit X tan trong nước tạo thành dung dịch có khả năng làm quỳ tím hóa xanh. X có thể là
A. Al2O3 B. K2O C. SO2 D. CuO
Câu 4: Nhận định nào sau đây là sai?
A. Oxit của kim loại là oxit bazơ.
B. Al2O3 tan được trong cả dung dịch HCl và dung dịch NaOH.
C. Khí SO2 là nguyên nhân gây ra hiện tượng mưa axit.
D. Khí CO2 là nguyên nhân gây hiệu ứng nhà kính.
Câu 5: Tính chất không phải của CaO là
A. hút ẩm mạnh. B. có tính bazơ.
C. trung hòa axit trong đất chua. D. tan trong nước thành dung dịch CaO.
Câu 6: SO2 không phản ứng với chất hoặc dung dịch nào sau đây?
A. CaO, t0
. B. Dung dịch H2SO4. C. dung dịch Ca(OH)2. D. H2O
Câu 7: Thí nghiệm nào sau đây thu được kết tủa không tan?
A. Dẫn khí CO2 dư vào dung dịch Ba(OH)2. B. Dẫn khí CO2 vào dung dịch Ba(OH)2 dư.
C. Nhỏ dung dịch HCl vào CuO. D. Dẫn khí CO2 vào dung dịch NaOH dư.
Câu 8: Phản ứng nào sau đây sai?
A. Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O B. Fe3O4 + 8HCl→ FeCl2 + 2FeCl3 + 4H2O
C. CO2 + CaCO3 + H2O → Ca(HCO3)2 D. CuO + H2O → Cu(OH)2
Câu 9: Trong công nghiệp, CaO được sản xuất từ
A. Ca. B. CaCO3. C. Ca(OH)2. D. CaC2O4.
Câu 10: Phản ứng dùng để điều chế SO2 trong phòng thí nghiệm là
A. S + O2
o
t
SO2 B. CaSO3 + H2SO4 → CaSO4 + SO2 + H2O
B. Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O D. 4FeS2 +11O2
o
t
2Fe2O3 + 8SO2

giúp em gấp với ạ
a) nK2SO4= 0,3. 0,15= 0,045(mol)
nBa(OH)2= 0,4.0,12=0,048(mol)
PTHH: K2SO4 + Ba(OH)2 -> BaSO4 + 2 KOH
Vì: 0,045/1 < 0,048/1
=> Ba(OH)2 dư, K2SO4 hết, tính theo nK2SO4
nBaSO4=nK2SO4=0,045(mol)
=> mBaSO4= 233.0,045=10,485(g)
b) CaCO3 + 2 HNO3 -> Ca(NO3)2 + CO2 + H2O
nCaCO3=5/100=0,05(mol)
=> nHNO3=2.nCaCO3=2.0,05=0,1(mol)
nCO2=nCaCO3=0,05(mol)
=> VddHNO3= 0,1/0,5= 0,2(l)=200(ml)
=>V=200(ml)
V(CO2,đktc)=0,05.22,4=1,12(l)
=>a=1,12(l)
Câu c)
nNa2CO3= 5,3/106=0,05(mol)
nH2SO4= 0,05. 1,07= 0,0535(mol)
PTHH: Na2CO3 + H2SO4 -> Na2SO4 + CO2 + H2O
Ta có: 0,05/1 < 0,0535/1
=> H2SO4 dư, Na2CO3 hết => Tính theo nNa2CO3
Ta có: nNa2SO4= nH2SO4(p.ứ)=nNa2CO3=0,05(mol)
=> nH2SO4(dư)=0,0535- 0,05= 0,0035(mol)
mNa2SO4= 0,05.142=7,1(g)
mH2SO4(dư)= 0,0035.98=0,343(g)
mddsau= mddH2SO4 + mNa2CO3= 50. 1.069+ 5,3=58,75(g)
=>C%ddH2SO4(dư) = (0,343/58,75).100=0,584%
C%ddNa2SO4= (7,1/58,75).100=12,085%
Chào em, anh không thấy nội dung em ạ?
Giúp mk với!!!
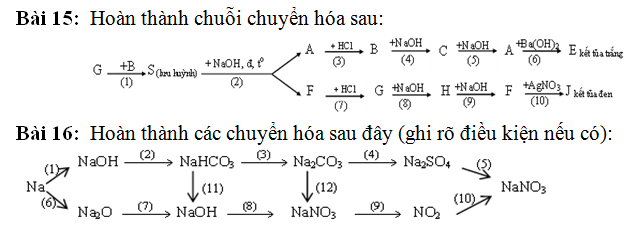
16. (1) \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
(2) \(NaOH+CO_2\rightarrow NaHCO_3\)
(3) \(NaHCO_3+NaOH\rightarrow Na_2CO_3+H_2O\)
(4) \(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+CO_2+H_2O\)
(5) \(Na_2SO_4+Ba\left(NO_3\right)_2\rightarrow BaSO_4+2NaNO_3\)
(6) \(4Na+O_2-^{t^o}\rightarrow2Na_2O\)
(7) \(Na_2O+H_2O\rightarrow2NaOH\)
(8) \(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
(9) Cu + 2NaNO3 + 4HCl → CuCl2 + 2NO2 + 2NaCl + 2H2O
(10) \(2NO_2+2NaOH\rightarrow NaNO_3+NaNO_2+H_2O\)
(11) \(NaHCO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+NaOH+H_2O\)
(12) \(Na_2CO_3+2HNO_3\rightarrow2NaNO_3+H_2O+CO_2\)
15.
\(\left(1\right)2H_2S+SO_2-^{t^o}\rightarrow3S+2H_2O\)
\(\left(2\right)\)3S + 6NaOH → 2Na2S + Na2SO3 + 3H2O
(3) \(Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\)
(4) \(SO_2+NaOH\rightarrow NaHSO_3\)
(5) \(NaHSO_3+NaOH\rightarrow Na_2SO_3+H_2O\)
(6) \(Na_2SO_3+Ba\left(OH\right)_2\rightarrow BaSO_3+2NaOH\)
(7) \(Na_2S+2HCl\rightarrow2NaCl+H_2S\)
(8) \(H_2S+NaOH\rightarrow NaHS+H_2O\)
(9) \(NaHS+NaOH\rightarrow Na_2S+H_2O\)
(10) \(Na_2S+AgNO_3\rightarrow Ag_2S+NaNO_3\)
Giúp mk với!!!
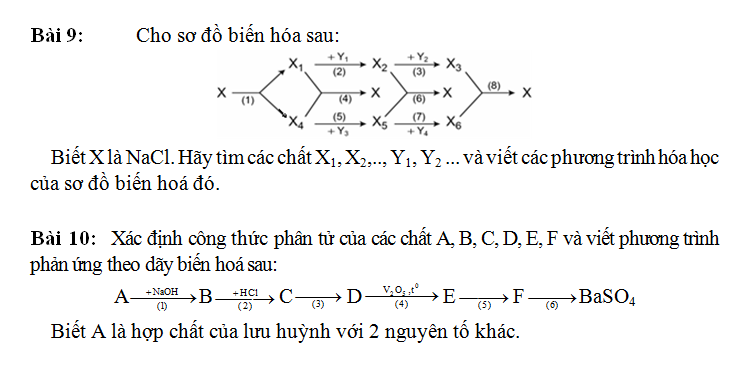
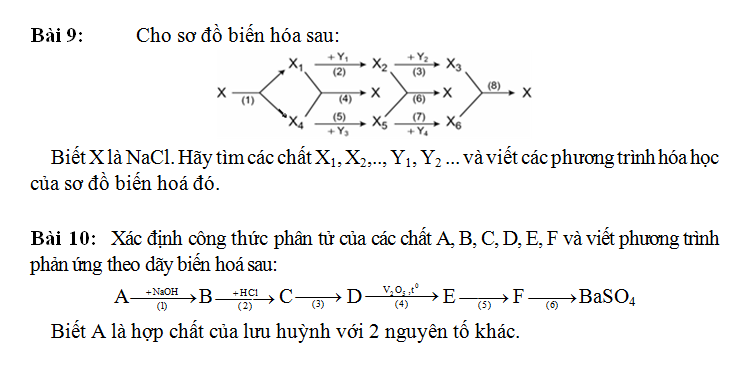
9.
(1) \(NaCl-^{đpnc}\rightarrow Na+\dfrac{1}{2}Cl_2\)
(2) \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
(3) \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
(4) \(Na+\dfrac{1}{2}Cl_2-^{t^o}\rightarrow NaCl\)
(5) \(Cl_2+H_2-^{as}\rightarrow2HCl\)
(6) \(NaOH+HCl\rightarrow NaCl+H_2O\)
(7) \(2HCl+Ba\left(OH\right)_2\rightarrow BaCl_2+2H_2O\)
(8) \(Na_2SO_4+BaCl_2\rightarrow BaSO_4+NaCl\)
A : NaHS
B : Na2S
C : H2S
D : SO2
E : SO3
F :H2SO4
(1) \(NaHS+NaOH\rightarrow Na_2S+H_2O\)
(2) \(Na_2S+2HCl\rightarrow2NaCl+H_2S\)
(3) 2H2S + 3O2 \(-^{t^o}\rightarrow\) 2SO2 + 2H2O
(4) \(SO_2+\dfrac{1}{2}O_2-^{t^o,V_2O_5}\rightarrow SO_3\)
(5) \(SO_3+H_2O\rightarrow H_2SO_4\)
(6) \(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
Giúp mình với!!!
Nhận biết các chất sau:
a) HNO3, H2SO4, HCl, K2SO4, KNO3, KOH, Ba(OH)2.
b) HCl, NaOH, Na2SO4, NaCl.
c) HCl, H2SO4, NaCl, Na2CO3
d) NaOH, BaCl2, Ba(OH)2, NaCl
e) Na2SO4, K2CO3, BaCl2, AgNO3
Nhận biết các chất sau:
a) HNO3, H2SO4, HCl, K2SO4, KNO3, KOH, Ba(OH)2.
Cho quỳ tím vào mẫu thử
+ Hóa đỏ: HNO3, H2SO4, HCl
+ Hóa xanh: KOH, Ba(OH)2
+Không đổi màu : K2SO4, KNO3
Cho dung dịch BaCl2 vào mẫu làm quỳ hóa đỏ
+ Kết tủa : H2SO4
H2SO4 + BaCl2 -------> BaSO4 + 2HCl
+ Không hiện tượng : HCl, HNO3
Cho dung dịch AgNO3 vào mẫu không hiện tượng
+ Kết tủa : HCl
AgNO3 + HCl --------> AgCl + HNO3
+ Không hiện tượng : HNO3
Cho dung dịch Na2SO4 vào 2 mẫu làm quỳ hóa xanh
+ Kết tủa : Ba(OH)2
Ba(OH)2 + Na2SO4 --------> BaSO4 + 2NaOH
+ Không hiện tượng : KOH
Cho dung dịch BaCl2 vào mẫu làm quỳ không đổi màu
+ Kết tủa : K2SO4
K2SO4 + BaCl2 -------> BaSO4 + 2KCl
+ Không hiện tượng : KNO3
b) HCl, NaOH, Na2SO4, NaCl.
Cho quỳ tím vào mẫu thử
+ Hóa đỏ: HCl
+ Hóa xanh: NaOH
+Không đổi màu : Na2SO4, NaCl
Cho dung dịch BaCl2 vào mẫu làm quỳ không đổi màu
+ Kết tủa : Na2SO4
Na2SO4 + BaCl2 -------> BaSO4 + 2NaCl
+ Không hiện tượng : NaCl
c) HCl, H2SO4, NaCl, Na2CO3
Cho quỳ tím vào mẫu thử
+ Hóa đỏ: HCl, H2SO4
+ Hóa xanh: Na2CO3
+Không đổi màu : NaCl
Cho dung dịch BaCl2 vào mẫu làm quỳ hóa đỏ
+ Kết tủa : H2SO4
H2SO4 + BaCl2 -------> BaSO4 + 2HCl
+ Không hiện tượng : HCl
BT2 : Để 1 mẩu Natri hidroxit trên tấm kính trong kk, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn trắng thấy có khí thoát ra, khí này làm đục nước vôi trong. Chất rắn màu trắng là sản phẩm phản ứng của Natri hidroxit với chất nào sau đây? Giải thích và viết phương trình hóa học minh họa.
a) Oxi trong kk
b) Hơi nước trong kk
c) Cacbon đioxit và oxi trong kk
d) Cacbon đioxit và hơi nước trong kk
e) Cacbon đioxit trong kk
mn giúp mình nha C:
Đáp án e
PTHH: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)