Help: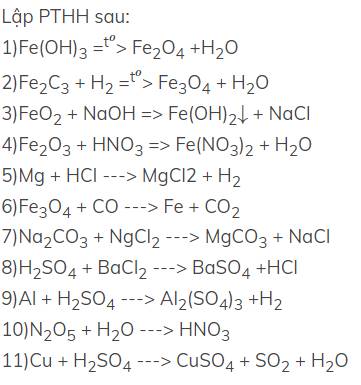
Hóa học
$\rm 1)2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
$\rm 2)3Fe_2O_3 + H_2 \xrightarrow{t^o} 2Fe_3O_4 + H_2O$
$\rm 3) FeCl_2 + 2NaOH \rightarrow Fe(OH)_2 \downarrow + 2NaCl$
$\rm 4) Fe_2O_3 + 6HNO_3 \rightarrow 2Fe(NO_3)_3 + 3H_2O$
$\rm 5) Mg + 2HCl \rightarrow MgCl_2 + H_2$
$\rm 6) Fe_3O_4 + 4CO \xrightarrow{t^o} 3Fe + 4CO_2$
$\rm 7) Na_2CO_3 + MgCl_2 \rightarrow MgCO_3 \downarrow + 2NaCl$
$\rm 8)H_2SO_4 + BaCl_2 \rightarrow BaSO_4 + 2HCl$
$\rm 9)2Al+3H_2SO_4 \rightarrow Al_2(SO_4)_3 + 3H_2$
$\rm 10)N_2O_5 + H_2O \rightarrow 2HNO_3$
$\rm 11)Cu + 2H_2SO_{4(đặc)} \xrightarrow{t^o} CuSO_4 + SO_2 \uparrow + 2H_2O$
Đúng 1
Bình luận (0)
nacl có lẫn các tạp chất là na2so4 mg(hco3)2 mgco3 hãy trình bày sơ đồ tách nacl tinh khiết và viết ptpu
- Nung nóng hh đến khối lượng không đổi thu được hh gồm NaCl, \(Na_2SO_4\), \(MgCO_3\)
\(Mg\left(HCO_3\right)_2\xrightarrow[]{t^o}MgCO_3+H_2O+CO_2\)
- Cho hh vào nước, phần tan là NaCl và \(Na_2SO_4\), phần không tan là \(MgCO_3\), lọc phần không tan ta thu đc dd gồm 2 muối
- Cho \(BaCl_2\) dư vào và lọc kết tủa ta thu được dd gồm NaCl, \(BaCl_2\)
\(Na_2SO_4+BaCl_2\xrightarrow[]{}2NaCl_{ }+BaSO_4\)
- Cho \(Na_2CO_3\) vào đến dư rồi lọc kết tủa thu được dd NaCl, \(Na_2CO_3\)
\(Na_2CO_3+BaCl_2\xrightarrow[]{}2NaCl+BaCO_3\)
- Cho dd HCl dư vào thu được dd NaCl, HCl
\(Na_2CO_3+2HCl\xrightarrow[]{}2NaCl+H_2O+CO_2\)
- Cô cạn dd thì HCl bay hơi, ta thu được NaCl tinh khiết
Đúng 2
Bình luận (0)
Nguyên tử Ca so với nguyên tử O nặng hơn hay nhẹ hơn?
\(\dfrac{NTK\left(Ca\right)}{NTK\left(O\right)}=\dfrac{40}{16}=2,5\)
Vậy nguyên tử Ca nặng hơn nguyên tử O 2,5 lần
Đúng 2
Bình luận (0)
Nung 100g CaCO3 sau 1 thời gian thu được 78g chất rắn X và V lít khi CO2
a) Tính V
b) Tìm thành phần %m các chất trong X
c) Tính hiệu suất phản ứng
\(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\)
(mol) x....................x...........x
a) Gọi x là số mol \(CaO\)
\(m_x=100-100x+56x=78\left(g\right)\)
⇒ x = 0,5
\(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
b) \(\%^m_{CaCO_3}=\dfrac{0,5.100}{78}.100=64,1\%\\ \%^m_{CaO}=100-64,1=35,9\%\)
c) \(n_{CaCO_{3\left(LT\right)}}=\dfrac{100}{100}=1\left(mol\right)\)
\(H\%=\dfrac{50}{100}.100=50\%\)
Đúng 2
Bình luận (0)
Hấp thụ hoàn toàn 6,72 (L) CO2 (đkc) vào dd chứa x mol KOH thu được dd chứa 33,8 (g) hỗn hợp 2 muối . Giá trị x là?
Cho hợp chât H2XO3,trong đó O chiếm 61,54% về khối lượng . Hỏi X là nguyên tố gì
Ta có: \(\%O=\dfrac{16.3}{2+X+16.3}.100\%=61,54\%\)
=> \(X=28\left(đvC\right)\)
=> X là nguyên tố Silic (Si)
Đúng 1
Bình luận (0)
Helpppp
\(PTHH:C+O_2->CO_2\)
ap dung DLBTKL ta co
\(m_C+m_{O_2}=m_{CO_2}\\ m_{O_2}=m_{CO_2}-m_C\\ m_{O_2}=88-24\\ m_{O_2}=64\left(g\right)\)
Đúng 3
Bình luận (0)
Helpppp
Đọc tiếp
Helpppp
\(PTHH:S+O_2->SO_2\)
ap dung DLBTKL ta co
\(m_S+m_{O_2}=m_{SO_2}\)
\(=>m_{O_2}=m_{SO_2}-m_S\\ =>m_{O_2}=96-48\\ =>m_{O_2}=48\left(g\right)\)
Đúng 3
Bình luận (1)
Lưu huỳnh + Khí oxi -> Lưu huỳnh đioxit
PTHH: S + O2 -> SO2
Áp dụng ĐLBTKL :
MS + MO2 -> MSO2
=> 48 + MO2 -> 96
=> MO2= 96-48=48
Đúng 1
Bình luận (0)
Lập phương trình hóa học của các chất phản ứng sau:
Al + O2 ----> Al2O3
Hãy cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong phản ứng
Lưu Huỳnh cháy trog oxi theo phản ứng hóa học như sau:
Lưu Huỳnh+Khí oxi \(\rightarrow\)Lưu huỳnh đioxit
Cho bt khối lượng lưu huỳnh là 48 gam,khối lượng khí lưu huỳnh đioxit thu đc là 96 gam.
Tính khối lượng khí oxi đã tham gia phản ứng.













