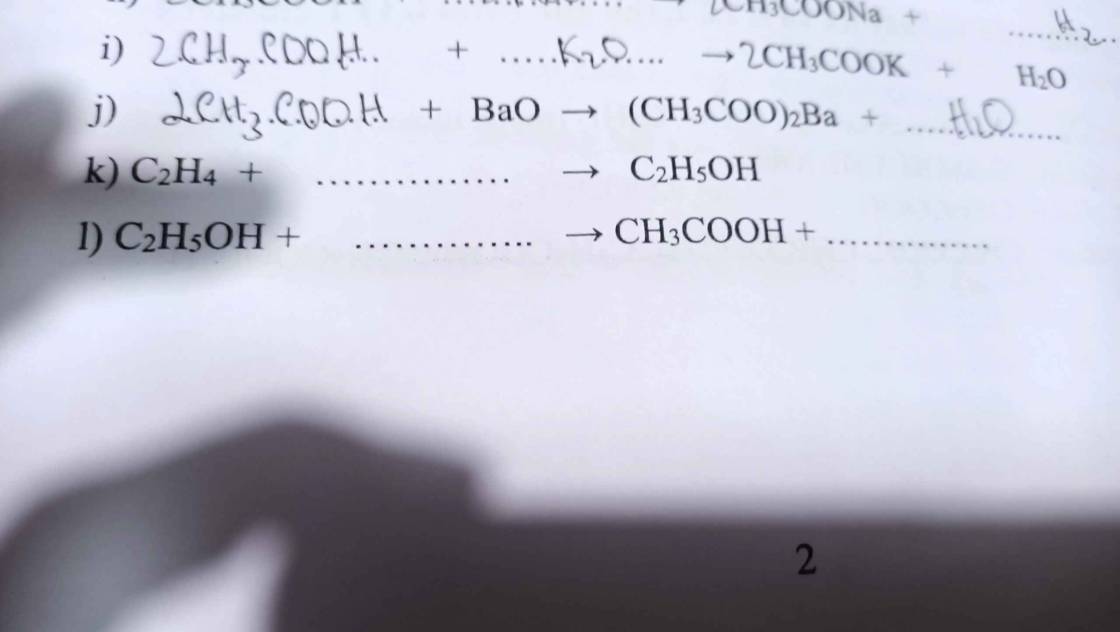đốt cháy hoàn toàn 1,38g hợp chất hữu cơ A thu được sản phẩm gồm 2,64g CO2 và 1,62g H2O . Xác định công thức phân tử của A . Biết tỉ khối hơi của A so với Oxi là 1,44
Hóa học
Tham khảo:
Để xác định công thức phân tử của hợp chất hữu cơ \(A\), ta cần thực hiện các bước sau:
1. Xác định số mol của \(CO_2\) và \(H_2O\) được tạo ra:
Số mol \(CO_2\) \(= \frac{2.64 \, \text{g}}{44.01 \, \text{g/mol}}\)
Số mol \(H_2O\) \(= \frac{1.62 \, \text{g}}{18.015 \, \text{g/mol}}\)
2. Xác định số mol của Carbon và Hydrogen trong \(A\) từ sản phẩm \(CO_2\) và \(H_2O\):
Số mol Carbon \(= \frac{2.64 \, \text{g}}{44.01 \, \text{g/mol}}\)
Số mol Hydrogen \(= \frac{2 \times 1.62 \, \text{g}}{18.015 \, \text{g/mol}}\)
3. Xác định tỉ lệ số mol giữa Carbon và Hydrogen trong hợp chất \(A\):
Tỉ lệ số mol \(C : H = \frac{\text{số mol Carbon}}{\text{số mol Hydrogen}}\)
4. Xác định tỉ lệ số mol giữa Carbon và Hydrogen trong hợp chất \(A\) so với tỉ khối hơi của \(A\) so với Oxi:
\(1.44 = \frac{\text{số mol Carbon} \times 12.01 \, \text{g/mol} + \text{số mol Hydrogen} \times 1.008 \, \text{g/mol}}{\text{số mol Carbon} \times 12.01 \, \text{g/mol} + \text{số mol Hydrogen} \times 1.008 \, \text{g/mol} + \text{số mol Oxygen} \times 16.00 \, \text{g/mol}}\)
5. Giải hệ phương trình để tìm số mol Carbon, Hydrogen và Oxygen trong hợp chất \(A\).
6. Xác định công thức phân tử của \(A\) từ số mol của Carbon, Hydrogen và Oxygen.
Hãy thực hiện các bước trên để xác định công thức phân tử của hợp chất \(A\).
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn 8,96 l C2H4
a) thể tích khí O2 cần dùng
b) thể tích không khí cần dùng cho phản ứng trên biết oxi chiếm 20% thể tích không khí. Các khí đo ở đktc
c) dẫn toàn bộ khí CO2 qua dd Ca(OH)2 dư , tính khối lượng kết tủa thu được
\(n_{C_2H_4}=\dfrac{V}{22,4}=\dfrac{8,96}{22,4}=0,4mol\)
PTHH: C2H4 + 3O2 \(\rightarrow\) 2CO2 + 2H2O
TL: 1 3 2 2
mol: 0,4 \(\rightarrow\) 0,12 \(\rightarrow\) 0,8
\(a.V_{O_2}=n.22,4=0,12.22,4=2,7l\)
\(b.V_{CO_2}=n.22,4=0,8.22,4=17,92l\)
\(V_{KK}=\dfrac{17,92.100\%}{20\%}=89,6l\)
c. Ta có \(n_{CO_2}=0,8mol\left(pt1\right)\)
PTHH: CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O
TL: 1 1 1 1
mol: 0,8 \(\rightarrow\) 0,8
\(m_{CaCO_3}=n.M=0,8.74=59,2g\)
Đúng 0
Bình luận (0)
giúp câu 1 pt cuối vs qạ cảm ơn nhìu ạ
\(1.\)
\(c.2CH_3COOH\rightarrow CH_3COOCH_3+CO_2+H_2O\)
Đúng 0
Bình luận (0)
\(CH_3COOH+CH_3OH\xrightarrow[đặc,t^0t]{H_2SO_4}CH_3COOCH_3+H_2O\)
Đúng 1
Bình luận (0)
\(k.C_2H_4+H_2O\xrightarrow[axit]{}C_2H_5OH\\ l.C_2H_5OH+O_2\xrightarrow[giâms]{men}CH_3COOH+H_2O\)
Đúng 1
Bình luận (0)
cho 5,6 lít hỗn hợp khí metan và etilen đi qua bình đựng brom , người ta thu được 9,4g đi brometan
a) viết phương trình phản ứng xảy ra
b) khối lượng brom tham gia phản ứng
c) xác định thành phần phần trăm theo thể tích của hỗn hợp khí ban đầu
\(a.C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ b.n_{C_2H_4Br_2}=\dfrac{9,4}{188}=0,05mol\\ n_{Br_2}=n_{C_2H_4}=n_{C_2H_4Br_2}=0,05mol\\ m_{Br_2}=0,05.160=8g\\ c.\%V_{C_2H_4}=\dfrac{0,05.22,4}{5,6}\cdot100\%=20\%\\ =>\%V_{CH_4}=100-20=80\%\%0\)
Đúng 0
Bình luận (0)
Có cách nào để biết hoá trị qua khối lượng mol không ạ? VD oxygen thì mình có thể suy ra hoá trị khi biết O = 16 không ạ?
Đốt cháy hoàn toàn m gam hỗn hợp CH4,CxHy,CnH2n cần dùng vừa đủ 12,395 lít khí 0xy đktc thu đc CO2 và 7,2 gam nươc
Dẫn 0,4958 lít khí carbon dioxide ở đkc vào dung dịch sodium hydroxide (lấy vừa đủ) thu được sodium carbonate Na2CO3 và nước.a) Viết công thức hóa học của carbon dioxide và sodium hydroxide.b) Carbon dioxide và sodium hydroxide thuộc loại chất nào trong 4 loại chất oxide, base, acid, muối?c) Khí carbon dioxide nặng hay nhẹ hơn không khí? Giải thích?d) Viết PTHH của phản ứng và xác định sản phẩm tạo thành.Lưu ý: HS cần trình bày rõ kí hiệu, công thức, phép tính, đơn vị và làm tròn đến 3-4 chữ số...
Đọc tiếp
Dẫn 0,4958 lít khí carbon dioxide ở đkc vào dung dịch sodium hydroxide (lấy vừa đủ) thu được
sodium carbonate Na2CO3 và nước.
a) Viết công thức hóa học của carbon dioxide và sodium hydroxide.
b) Carbon dioxide và sodium hydroxide thuộc loại chất nào trong 4 loại chất oxide, base, acid, muối?
c) Khí carbon dioxide nặng hay nhẹ hơn không khí? Giải thích?
d) Viết PTHH của phản ứng và xác định sản phẩm tạo thành.
Lưu ý: HS cần trình bày rõ kí hiệu, công thức, phép tính, đơn vị và làm tròn đến 3-4 chữ số thập phân –
nếu cần khi tính toán ở câu e,f,g bên dưới.
e) Tính số mol ứng với 0,4958 lít khí carbon dioxide ở đkc.
f) Tính khối lượng sodium hydroxide cần dùng để phản ứng đủ với 0,4958 lít khí carbon dioxide ở đkc.
g) Tính khối lượng sodium carbonate thu được sau phản ứng.
a: CTHH của carbon dioxide là CO2
CTHH của sodium hydroxide là NaOH
b: CO2 là oxit
NaOH là bazo
c: \(\dfrac{M_{CO_2}}{M_{kk}}=\dfrac{12+16\cdot2}{29}=\dfrac{44}{29}>1\)
=>CO2 nặng hơn không khí
d: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
e: \(n_{CO_2}=\dfrac{0.4958}{22,4}\simeq0,022\left(mol\right)\)
f: \(n_{NaOH}=2\cdot n_{CO_2}\simeq0,044\left(mol\right)\)
\(m_{NaOH}\simeq0,044\cdot40=1,76\left(g\right)\)
d: \(n_{Na_2CO_3}=n_{CO_2}\simeq0,022\left(mol\right)\)
=>\(m_{Na_2CO_3}\simeq0,022\cdot106=2,332\left(g\right)\)
Đúng 0
Bình luận (0)
đặt cốc A đựng dd HCl và cốc B đựng dd H2SO4 loãng vào 2 đĩa cân sao cho cân ở ví trí cân bằng ,sau đó làm thí nghiệm như sau : -Cho 25,44 g Na2CO3 vào cốc đựng dd HCl -Cho 3,24 g kim loại M hoá trị 3 vào cốc đựng dd H2SO4 a, M là kim loại nào? b,Tính n...
Đọc tiếp
đặt cốc A đựng dd HCl và cốc B đựng dd H2SO4 loãng vào 2 đĩa cân sao cho cân ở ví trí cân bằng ,sau đó làm thí nghiệm như sau : -Cho 25,44 g Na2CO3 vào cốc đựng dd HCl -Cho 3,24 g kim loại M hoá trị 3 vào cốc đựng dd H2SO4 a, M là kim loại nào? b,Tính nồng độ phần trăm các muối thu được ,nếu khối lượng của mỗi dd HCl và H2SO4 khi cân thăng bằng là 160 g .Biết phản ứng xảy ra hoàn toàn
1. Phản ứng giữa Na2CO3 và HCl:
Na2CO3 + 2HCl -> 2NaCl + H2O + CO2
2. Phản ứng giữa kim loại M và H2SO4:
M + H2SO4 -> MSO4 + H2
a) Để xác định kim loại M, chúng ta cần biết rằng nó phải có hoá trị 3. Trong trường hợp này, M phải là kim loại nhóm IA vì chúng có hoá trị +1, +2, hoặc +3. Trong nhóm này, kim loại duy nhất có thể có hoá trị +3 là nhôm (Al).
b) Bây giờ, chúng ta tính nồng độ phần trăm của các muối thu được.
- Đối với muối thu được từ Na2CO3 và HCl (muối NaCl):
Khối lượng Na2CO3 = 25,44 g
Khối lượng HCl = 160 g - 25,44 g = 134,56 g
Tính khối lượng muối NaCl thu được từ phản ứng Na2CO3 và HCl: 25,44 g Na2CO3 * (1 mol Na2CO3 / 105,99 g Na2CO3) * (2 mol NaCl / 1 mol Na2CO3) * (58,44 g NaCl / 1 mol NaCl) = 59,04 g NaCl
- Đối với muối thu được từ kim loại M và H2SO4 (muối MSO4):
Khối lượng kim loại M = 3,24 g
Khối lượng H2SO4 = 160 g - 3,24 g = 156,76 g
Tính khối lượng muối MSO4 thu được từ phản ứng kim loại M và H2SO4: 3,24 g M * (1 mol M / 26,98 g M) * (1 mol MSO4 / 1 mol M) * (120,37 g MSO4 / 1 mol MSO4) = 14,98 g MSO4
Cuối cùng, tính phần trăm khối lượng của mỗi muối:
- Phần trăm NaCl: (59,04 g NaCl / (59,04 g NaCl + 14,98 g MSO4)) * 100% ≈ 79%
- Phần trăm MSO4: (14,98 g MSO4 / (59,04 g NaCl + 14,98 g MSO4)) * 100% ≈ 21%
Vậy nồng độ phần trăm của muối NaCl là khoảng 79%, và của muối MSO4 là khoảng 21%.
Đúng 1
Bình luận (1)
Cho 20g hỗn hợp gồm rượu etylic và axit axetic tham gia phản ứng hết 14,84g muối Na2CO3. Tính thành phần phần trăm khối lượng ancol, axit trong hỗn hợp ban đầu
Ta có: \(n_{Na_2CO_3}=\dfrac{14,84}{106}=0,14\left(mol\right)\)
PT: \(Na_2CO_3+2CH_3COOH\rightarrow2CH_3COONa+CO_2+H_2O\)
Theo PT: \(n_{CH_3COOH}=2n_{Na_2CO_3}=0,28\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_3COOH}=\dfrac{0,28.60}{20}.100\%=84\%\\\%m_{C_2H_5OH}=16\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)