Câu 7: Hiện tượng nào sau đây là hiện tượng vật lý? *
A. Thức ăn để lâu bị ôi thiu
B. Cho vôi sống CaO hòa tan vào nước tạo thành vôi tôi
C. Đinh sắt để lâu ngoài không khí bị gỉ
D. Cồn để trong lọ không kín bị bay hơi
Câu 7: Hiện tượng nào sau đây là hiện tượng vật lý? *
A. Thức ăn để lâu bị ôi thiu
B. Cho vôi sống CaO hòa tan vào nước tạo thành vôi tôi
C. Đinh sắt để lâu ngoài không khí bị gỉ
D. Cồn để trong lọ không kín bị bay hơi
Câu 7: Hiện tượng nào sau đây là hiện tượng vật lý? *
A. Thức ăn để lâu bị ôi thiu
B. Cho vôi sống CaO hòa tan vào nước tạo thành vôi tôi
C. Đinh sắt để lâu ngoài không khí bị gỉ
D. Cồn để trong lọ không kín bị bay hơi
mình đang cần gấp ạ, cho mình cảm ơn trước
biết \(NTK_{Ca}=40\left(đvC\right)\)
vậy \(PTK\) của hợp chất \(=2.40=80\left(đvC\right)\)
ta có:
\(1.Z+3O=80\)
\(Z+3.16=80\)
\(Z+48=80\)
\(Z=80-48=32\left(đvC\right)\)
\(\Rightarrow Z\) là \(S\) (lưu huỳnh)
Câu 36. Hoà tan hoàn toàn 7,8 g kim loại X vào dung dịch HNO3 thu được 0,672 lít khí N2O (đktc). Vậy X có thể là
A. Cu B. Fe C. Zn D. Al
Câu 37. Trộn 100ml dung dịch H2SO4 0,1M với 100ml dung dịch NaOH 0,1M thu được dung dịch Y. pH của dung dịch Y là
A. 2 B. 1,7 C. 12 D. 3
Câu 38. Dung dịch X gồm a mol Na+; 0,15 mol K+; 0,1 mol HCO3-; 0,15 mol CO32- và 0,1 mol SO42-. Tổng khối lượng muối trong dung dịch X là
A. 33,8 gam B. 48,5 gam. C. 29,5 gam. D. 40,9 gam.
Câu 39. Hoà tan m gam Fe vào dung dịch HNO3 loãng, dư thu được 1,344 lit khí NO duy nhất (đktc). Giá trị của m là:
A. 1,12 gam. B. 3,36 gam. C. 0,56 gam. D. 5,6 gam.
Câu 40. Cho 13,9 gam hỗn hợp hai kim loại Al và Fe vào dung dịch HNO3 loãng dư, thu được 6,72 lit khí NO (đktc) duy nhất. Phần trăm khối lượng của Al trong hỗn hợp ban đầu là
A. 49,1% B. 21,15 % C. 19,42 % D. 65,9 %
Cho C=12, H=1, O=16, N=14, Zn=65, Al=27, Fe=56, Cu =64, S=32, Na=23, K=39.
có giải bài làm rõ ràng càng tốt ạ . mình cảm ơn
1. Nhiệt phân 18,9g Zn(NO3)2 một thời gian thu được hỗn hợp khí X (biết h = 80%).
a. Tính thể tích khí thoát ra (đktc).
b. Khối lượng chất rắn thu được sau phản ứng.
\(n_{Zn\left(NO_3\right)_2}=\dfrac{18,9}{189}=0,1mol\)
\(2Zn\left(NO_3\right)_2\underrightarrow{t^o}2ZnO+4NO_2+O_2\)
0,1 0,1 0,2 0,05
a) \(\Sigma n_{\uparrow}=0,2\cdot22,4+0,05\cdot22,4=0,224\left(l\right)\)
b) \(m_{ZnO\left(líthuyết\right)}=0,1\cdot81=8,1g\)
Do H=80%\(\Rightarrow\) \(m_{ZnO}=\dfrac{8,1\cdot100}{80}=10,125g\)
Cho hh gồm Fe2O3 CuO Fe Ag hãy dùng pp hoá học tách riêng Ag tinh khiết ra khỏi hỗn hợp
Nguyên tố X có nguyên tử khối bằng 2 lần nguyên tử khối của oxi. Xác định tên và kí hiệu hóa học của X. ai giúp mình vs, mình đang cần gấp .Camon trc ạ
Đáp án
Theo đề bài, ta có :
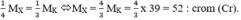
Theo đề bài, ta có: M X = 3 , 5 M O = 3 , 5 x 16 = 56 : sắt (Fe).
biết \(NTK\) của \(O=16\left(đvC\right)\)
\(\Rightarrow\) \(NTK\) của \(X=16.2=32\left(đvC\right)\)
\(\Rightarrow X\) là lưu huỳnh,kí hiệu là \(S\)
hòa tan hết m(g) Al cần vừa đủ V ml dung dịch HCl 2M , sau phản ứng thu được 3,36 l khí (ĐKTC) và dung dịch X có chứa a (g ) muối
a) tính m ,V ,a
b)tính nồng độ mol/lít của chất có trong dung dịch X![]()
cặp chất nào sao đây, phản ứng tạo thành sản phẩm có chất khí?
A..Na2SO4 và BaCl2
B..Na2SO3 và HCl
C..KCl và AgNO3
D..KOH và BaCl2
Cặp chất nào sau đây , phản ứng tạo thành sản phẩm có chất khí :
A Na2SO4 và BaCl2
B Na2SO3 và HCl
C KCl và AgNO3
D KOH và BaCl2
Pt : \(Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\)
Chúc bạn học tốt